トップページ > 広報活動 > プレスリリース > 希少がんに対するオンライン治験を開始
希少がんに対するオンライン治験を開始地域に居ながらにして中央病院が実施する医師主導治験へ参加することが可能に
2023年6月27日
国立研究開発法人国立がん研究センター
発表のポイント
- 希少がんを対象とした2つの医師主導治験でオンライン治験を開始し、これまで中央病院(東京)まで来院することが難しかった遠隔地在住の患者さんでも、近隣の医療機関を通じて当該治験へ参加することが可能となりました。
- オンライン治験の導入によって、地方在住の患者さんの治験アクセスが劇的に改善するのみならず、患者登録スピードの加速による早期の治験完了、治験全体のコスト削減が期待されます。
- 全国のがんゲノム医療中核拠点病院・拠点病院・連携病院と連携し、希少がんのオンライン治験を推進するネットワークを構築し、希少がん治療開発の効率化、迅速化を行っていきます。
概要
国立研究開発法人国立がん研究センター(理事長:中釜 斉、東京都中央区)中央病院(病院長:島田和明)は、国立研究開発法人日本医療研究開発機構(AMED)臨床研究・治験推進研究事業「希少がんプラットフォーム試験へのDCT導入に関する研究開発(研究代表者:中村 健一)」を通じて、希少がんに対する産学共同の治療開発プラットフォームであるMASTER KEYプロジェクトで実施されている2つの医師主導治験において、全国の患者さんが地域に居ながらにして中央病院が実施する治験へ参加することを可能とするオンライン診療等の体制を構築しました。
このことにより、これまで治験への参加が困難であった遠隔地に居住している患者さんが、一度も東京都の中央病院へ来院することなく、オンラインで治験へ参加することが可能となります。遠隔地在住の患者さんにとっての治験アクセスが劇的に改善するとともに、希少がんに対する有効な治療法の開発が加速することが期待されます。
背景
2023年3月末時点で、中央病院で実施中の治験数は525課題ありましたが、地方の大学病院のがん治験数は一桁ということも珍しくありません。また、遠隔地から中央病院で実施している治験に参加することを希望したとしても、移動のための時間的、経済的負担によって断念するケースも多く、治験へのアクセスの地域間差は、地方在住の患者さんにとって大きな課題となっています。特に希少がんの治験は都市部に偏在しており、地方在住患者さんの治験へのアクセスの改善について希少がんの患者団体からも強い要望が寄せられていました。
希少がんについては、中央病院が中心となって全国の7施設と15の製薬企業が参画するMASTER KEYプロジェクトを実施しており、この中で希少がんの治験を積極的に実施しています。2023年6月時点で27の医師主導治験・企業治験をプロジェクトとして実施していますが、治験実施施設が都市部に限られていることから、治験に参加したい患者側の視点、治験への参加を勧めたい医療機関側の視点の双方から、さらなる治験アクセスへの改善策が求められてきました。
一方、コロナ禍をきっかけに、わが国でも条件付きで初診からのオンライン診療が可能となり、治験に関しても「オンライン治験」の可能性が模索されるようになってきました。このオンライン治験は、海外でもDecentralized Clinical Trial(DCT)と呼ばれ、主に良性疾患に対して適用が進みつつあります。わが国でも厚生労働省でオンライン治験に関連した通知が発出されるなど、導入に向けた動きが進んでいましたが、がん領域での導入事例はまだ限られていました。
こうした背景をもとに、今回中央病院ではMASTER KEYプロジェクトで実施されている2つの医師主導治験でオンライン治験を開始し、全国の患者さんが地域に居ながらにして中央病院が実施する治験へ参加することを可能とする体制整備を行いました。
実施体制
従来、中央病院で実施する治験へ参加するためには、決められたスケジュールで東京都の中央病院まで毎回来院する必要がありましたが、今回のオンライン治験では一度も中央病院に来院することなく、治験へ参加することが可能になります。
オンライン治験へ参加するためには、近隣の医療機関(パートナー病院と呼びます)へ受診していただき、治験へ参加する条件を満たすかどうかを検査する必要があります。条件を満たした場合、パートナー病院と中央病院をオンラインでつなぎ、パートナー病院の主治医同席のもと、中央病院の医師から患者さんに治験に関する説明を行い、治験参加への同意を得ます。治験薬(経口薬)は、中央病院から患者さんの自宅へ直接郵送し、患者さんには中央病院の医師の指示のもとで内服を行っていただきます。治験期間中の検査については、決められたスケジュールでパートナー病院にて検査を受けていただき、検査結果はパートナー病院から中央病院に共有されます。こうした仕組みによって、患者さんは一度も中央病院へ来院することなく、治験へ参加することが可能となります。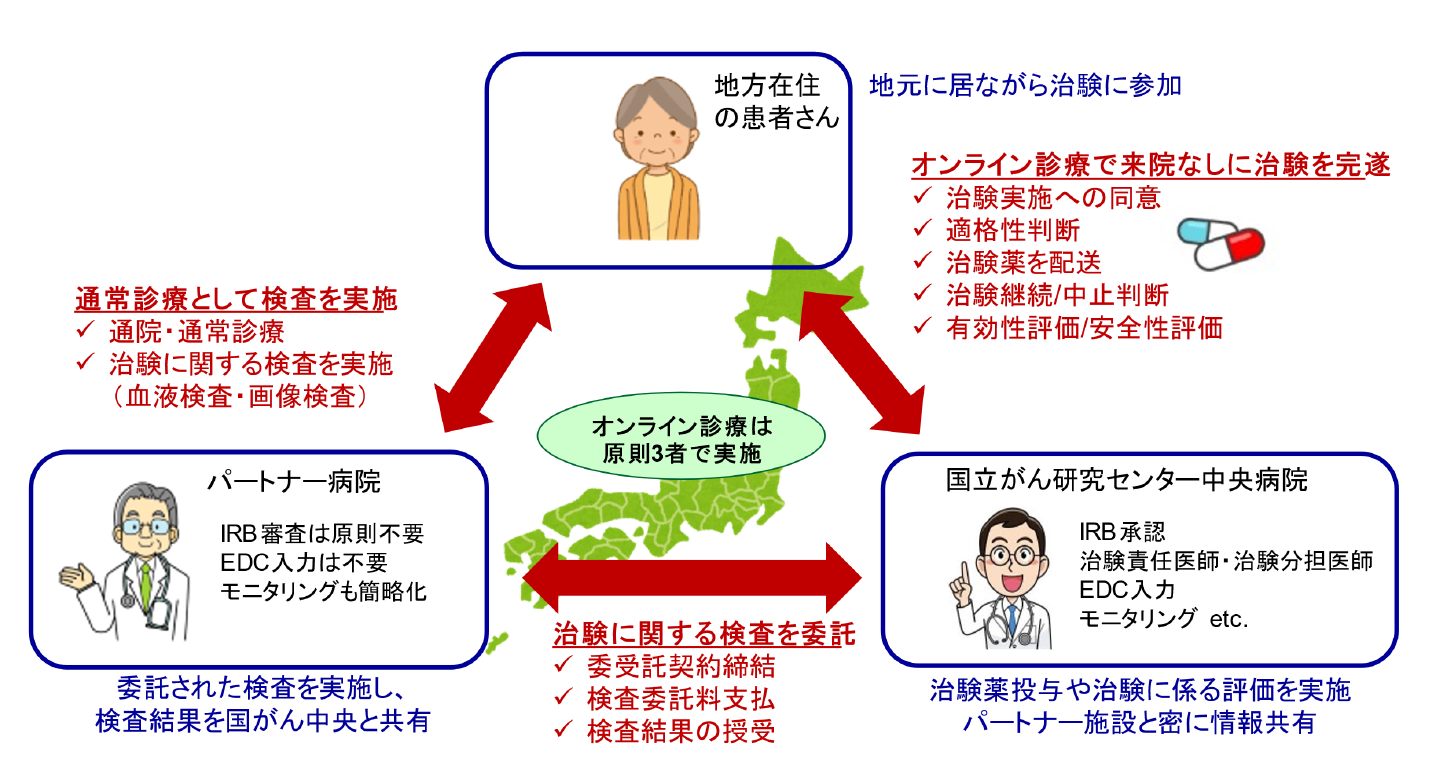
なお、パートナー病院は、がんゲノム医療中核拠点病院・拠点病院・連携病院のいずれかである必要があります。中央病院とパートナー病院との間で、あらかじめ、あるいは患者さんから申し出があった時点で施設間契約を締結します。現在のパートナー病院は国立病院機構四国がんセンターと島根大学医学部附属病院の2施設ですが、今後パートナー病院を全国に拡大し、希少がんオンライン治験ネットワークを整備していきます。
参考)がんゲノム医療中核拠点病院・拠点病院・連携病院のリスト
https://for-patients.c-cat.ncc.go.jp/hospital_list/(外部サイトにリンクします)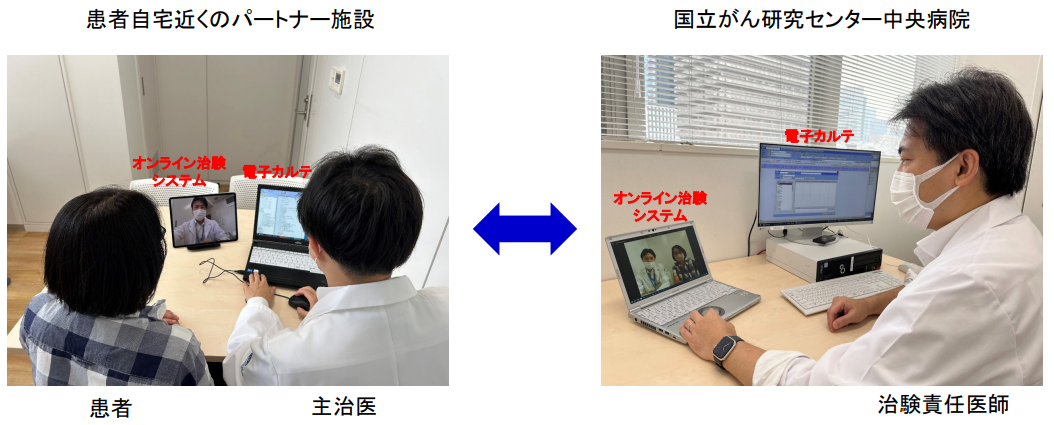
オンライン治験の意義と将来展望
オンライン治験の主なメリットは以下の3点です。
- 地方在住の患者さんの治験アクセスが劇的に改善し、居住地を問わず中央病院で実施している治験への参加が可能になります。
- 中央病院にとっても全国の患者さんが治験参加可能となれば、治験完了に必要な患者数を早期に集めることができます。
- 予定より早期に治験が終了することや、モニタリングをリモートで行う体制を同時に構築することで、治験にかかるコストを削減することができます。
今回、オンライン治験を開始するのは、希少がんに対する2つの医師主導治験ですが、今後はMASTER KEYプロジェクトで実施される医師主導治験・企業治験にも積極的にオンライン治験の導入を進めていきます。また、希少がん以外への拡大や、患者さんの来院とオンライン診療を組み合わせたハイブリッド型のオンライン治験の実施など、患者さんのニーズや研究の特徴にあわせ、治験へのアクセスを改善する取り組みを進めていきます。
また、日本だけでなくアジア全体においても効率的な治験実施体制の構築を行っていきます。
対象となる医師主導治験
今回、オンライン治験による登録の準備をしている医師主導治験の一つは以下のとおりです。
局所進行・再発類上皮肉腫に対するタゼメトスタットの第II相医師主導治験(NCCH2107/MK012)
https://jrct.niph.go.jp/latest-detail/jRCT2031220523(外部サイトにリンクします)
「MASTER KEYプロジェクト」について
「MASTER KEYプロジェクト」は、国立がん研究センター中央病院が有する先端的な研究開発のノウハウと研究支援機能、製薬企業が有するシーズと開発戦略を融合させ、網羅的かつ効率的に希少がんの治療開発を進めるための産学共同の研究基盤の構築を目指したプロジェクトです。2017年5月より国内で、また2021年10月からはアジア地域とも連携し、現在、15企業と国立がん研究センター中央病院を含めて国内7施設、アジア地域では6か国15施設が参加しています(MASTER KEY Asia)。参加企業は、「MASTER KEYプロジェクト」のプラットフォームを利用することで、開発戦略に応じたデータベースの活用、症例リクルートの促進、前臨床研究での国立がん研究センター研究所との協業など多くのメリットが得られる仕組みとなっており、現在27件の治験(医師主導治験16、企業治験11)が進んでいます。
研究費
令和5-8年度 国立研究開発法人日本医療研究開発機構(AMED) 23lk0221182h0001
「希少がんプラットフォーム試験へのDCT導入に関する研究開発」
臨床研究・治験推進研究事業(研究代表者:中村 健一)
問い合わせ先
研究に関する問い合わせ
国立がん研究センター中央病院
国際開発部門/臨床研究支援部門 中村 健一
Eメール:kennakam●ncc.go.jp
広報窓口
国立がん研究センター
企画戦略局 広報企画室
Eメール:ncc-admin●ncc.go.jp
