トップページ > 研究組織一覧 > 基盤的臨床開発研究コアセンター > 免疫創薬部門 > 研究プロジェクト > 担がん生体内におけるがん・免疫相互作用メカニズムの解明と画期的ながん治療法の開発(工藤担当)
担がん生体内におけるがん・免疫相互作用メカニズムの解明と画期的ながん治療法の開発(工藤担当)
がん組織は、がん細胞だけでなく、血管系、間質系、免疫系など多様な細胞集団で構成されています。つまり、がん細胞の性質や能力は、それ自身の変異や増幅、欠失などの遺伝子や形質の変化だけではなく、それら周囲の様々な細胞によって外部修飾を受け、それらの細胞群もまたがん細胞との相互作用によって影響を受けて、その分だけさらにがん細胞は修飾されていると考えられます。さらに、患者さん個々人に依る体質や生活習慣、治療などの違いが加わることで、がん細胞の生物学的特性はより一層多様化し、がん進展を支持するこの負の連鎖反応によって体内環境はますます複雑化して、がんは治療による攻撃から逃避していると考えられます。
このような難治性のがんでも効果的に治療できる画期的な治療法を開発することを目標に、動物モデルや患者検体を用いて、がん細胞の生物学的特性が免疫機能に与える影響と、宿主免疫の変化ががん細胞機能に与える影響を様々な最先端技術を駆使して網羅的に解析し、担がん生体内全体で繰り広げられるがん・免疫間の複雑で多様な相互作用の解明に取り組んでおり、独自の手法で創薬のターゲット分子を絞り込み、病院や製薬企業に臨床開発を提案しています。
医学研究成果を患者救済に橋渡しする『Translational Research』からの創薬を目指すこの取り組みは、機関内外から受け入れた若手研究者や臨床医らにも受け継がれており、学位取得、国際学会での発表、論文発表、海外留学など、多くの次世代研究者の育成・活躍に繋がっています(工藤論文業績参照)。
我々は、この負の連鎖反応の分子メカニズムを解明しており、そこで中心的役割を果たす分子群を標的とした新たながん治療薬を企業と共に開発しています。将来的には、がんの進展を根本から断ち切って効率よく効果的に感を治療できる薬剤の開発を目指しています。
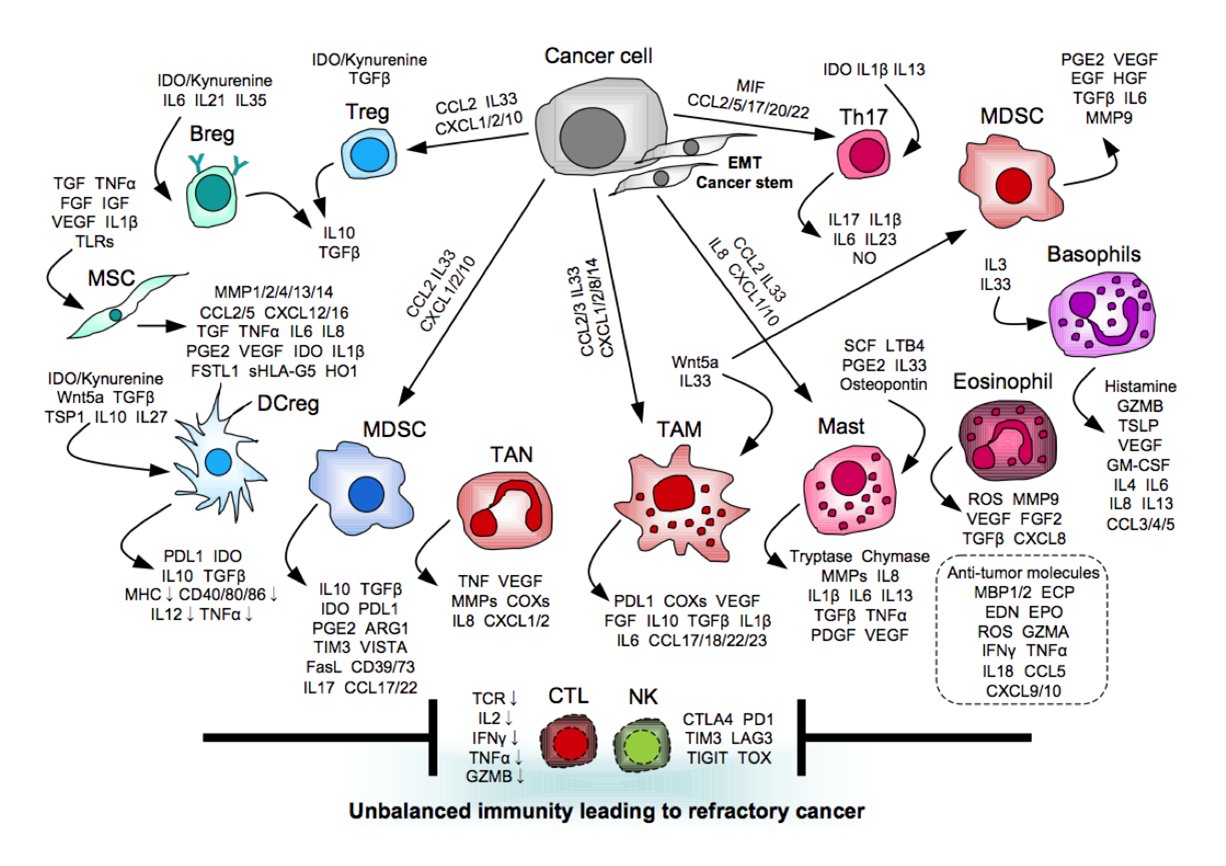
我々は、その主な作戦として、好中球やマクロファージなどを含む『ミエロイド細胞』に特に焦点を当て、これを不活化・阻害・排除する免疫治療法を開発しています(下図:fimmu-13-1009701, 2022より引用)。ミエロイド細胞は、ヒトの免疫系で大半を占めていますが、臨床解析などではサンプリング工程でロスしたり、凍結保存によって死滅さしてしまったりする場合が多く、その実態的な詳細は未だ国際的にもよく分かっていません。我々は、独自に開発した細胞分離技術を用いて、赤血球以外の白血球分画全てを回収し、生体内を反映した状態のままFlow Cytometry解析や各種オミックス解析などに供して免疫系をプロファイリングしています。
また、生活環境の多様な要因(加齢、喫煙、生活習慣病など)は、免疫系の質(各種細胞の比率、数、機能活性など)に大きく影響し、がんの発症にも寄与していることが分かっています。我々は、このようなバックグラウンド要因も全て考慮した解析を行うことで、個々人の免疫状態とリンクする遺伝子・分子をいくつか同定しており、これらを標的とした精度の高いprecision medicineの開発を目指しています。
最大の特徴は、独自の免疫学的観点によって膨大なデータの中から創薬ターゲットを選出し、可能な限り臨床治療での実用化に結び付けようとしている点です。解析したデータと患者の診療情報との関係性を統計学的に解析することで、がん治療でターゲットとする臨床的意義を明確にしつつ、動物モデルを使ったin vivo薬効試験によって有力候補を絞り込み、臨床試験を見据えて様々な薬剤を組み合わせる有効な治療レジメも開発し、病院や製薬企業に臨床開発を提案しています。
一例として、中央病院・消化管内科とともに進めてきたWJOG10417GTR多施設共同研究では、100症例のニボルマブ治療胃がん患者から採取した新鮮な腫瘍組織と末梢血を網羅的に解析し、PD1抗体治療に対する不応答規定キー要因をいくつか同定することに成功しており、その成果の一部は既に多くの国際学会で発表しています。一部のターゲット分子については、企業と共同で抗体医薬品の開発を進めています。
このような難治性のがんでも効果的に治療できる画期的な治療法を開発することを目標に、動物モデルや患者検体を用いて、がん細胞の生物学的特性が免疫機能に与える影響と、宿主免疫の変化ががん細胞機能に与える影響を様々な最先端技術を駆使して網羅的に解析し、担がん生体内全体で繰り広げられるがん・免疫間の複雑で多様な相互作用の解明に取り組んでおり、独自の手法で創薬のターゲット分子を絞り込み、病院や製薬企業に臨床開発を提案しています。
医学研究成果を患者救済に橋渡しする『Translational Research』からの創薬を目指すこの取り組みは、機関内外から受け入れた若手研究者や臨床医らにも受け継がれており、学位取得、国際学会での発表、論文発表、海外留学など、多くの次世代研究者の育成・活躍に繋がっています(工藤論文業績参照)。
1. 難治性がんを効果的に排除するがん治療法の研究開発
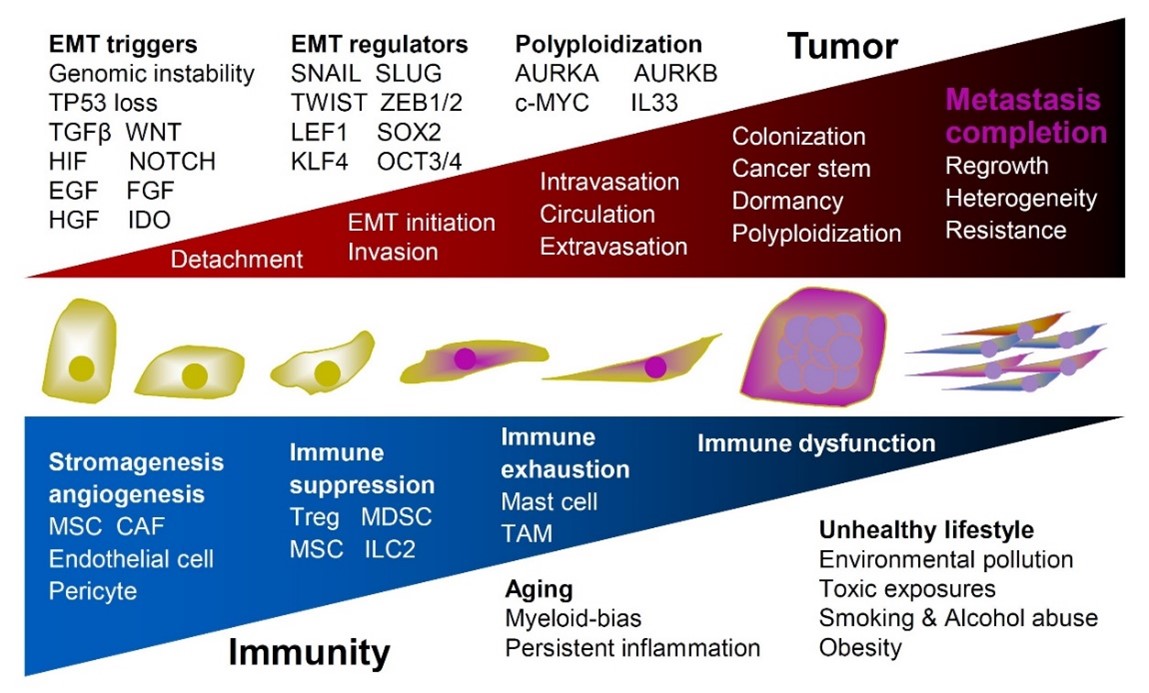
がん細胞は、『上皮間葉転換(Epithelial-to-Mesenchymal Transition, EMT)』を生じることで、転移性やがん幹細胞性を獲得して難治性に転じますが、自らの変化に留まらず、様々な可溶分子の産生を介して近隣のがん細胞にも同様の様の特性を賦与したり、強い免疫抑制活性を有す間葉系幹細胞や免疫制御性T細胞 (Treg)、炎症性のミエロイド細胞などを誘導して、免疫機能を抑制・疲弊・不全化させたりして、難治性をより一層強化することが知られています。我々は、この負の連鎖反応の分子メカニズムを解明しており、そこで中心的役割を果たす分子群を標的とした新たながん治療薬を企業と共に開発しています。将来的には、がんの進展を根本から断ち切って効率よく効果的に感を治療できる薬剤の開発を目指しています。

2. 免疫異常を効果的に修正し得るがん治療法の研究開発
免疫系を抑制性に傾けてしまう『免疫チェックポイント』を制御する分子群が多数同定され、その機能を阻害する抗体医薬品の開発が世界中で活発化していますが、臨床治療での有効性は一部の患者に限定的なのが現状です。これは、がん患者の免疫機能はがん細胞との相互作用によって極端に低下・破綻している場合が多いためで、非常に複雑で多様な分子・細胞から構成される免疫ネットワークでは、1分子のみを阻害しても代替となる免疫抑制機構が多数存在するためです。つまり、がん側の難治性獲得機構を根本から遮断する作戦と同様に、がんを適切に攻撃・排除できるように異常な免疫系を根本から修正して立て直す作戦が必要です。我々は、その主な作戦として、好中球やマクロファージなどを含む『ミエロイド細胞』に特に焦点を当て、これを不活化・阻害・排除する免疫治療法を開発しています(下図:fimmu-13-1009701, 2022より引用)。ミエロイド細胞は、ヒトの免疫系で大半を占めていますが、臨床解析などではサンプリング工程でロスしたり、凍結保存によって死滅さしてしまったりする場合が多く、その実態的な詳細は未だ国際的にもよく分かっていません。我々は、独自に開発した細胞分離技術を用いて、赤血球以外の白血球分画全てを回収し、生体内を反映した状態のままFlow Cytometry解析や各種オミックス解析などに供して免疫系をプロファイリングしています。
また、生活環境の多様な要因(加齢、喫煙、生活習慣病など)は、免疫系の質(各種細胞の比率、数、機能活性など)に大きく影響し、がんの発症にも寄与していることが分かっています。我々は、このようなバックグラウンド要因も全て考慮した解析を行うことで、個々人の免疫状態とリンクする遺伝子・分子をいくつか同定しており、これらを標的とした精度の高いprecision medicineの開発を目指しています。

3. Translational researchに基づいた創薬研究
中央病院、東病院、医薬基盤・健康・栄養研究所、東京大学、慶應義塾大学、製薬企業、IT企業など、機関内外の様々な研究機関の臨床医らと連携し、Flow Cytometry解析やELISA解析、病理学的解析などの標準的な解析手法に加え、RNAseq解析やProteomics解析などの最先端技術も駆使して、患者検体のがん・免疫プロファイリングを広く行っています。最大の特徴は、独自の免疫学的観点によって膨大なデータの中から創薬ターゲットを選出し、可能な限り臨床治療での実用化に結び付けようとしている点です。解析したデータと患者の診療情報との関係性を統計学的に解析することで、がん治療でターゲットとする臨床的意義を明確にしつつ、動物モデルを使ったin vivo薬効試験によって有力候補を絞り込み、臨床試験を見据えて様々な薬剤を組み合わせる有効な治療レジメも開発し、病院や製薬企業に臨床開発を提案しています。
一例として、中央病院・消化管内科とともに進めてきたWJOG10417GTR多施設共同研究では、100症例のニボルマブ治療胃がん患者から採取した新鮮な腫瘍組織と末梢血を網羅的に解析し、PD1抗体治療に対する不応答規定キー要因をいくつか同定することに成功しており、その成果の一部は既に多くの国際学会で発表しています。一部のターゲット分子については、企業と共同で抗体医薬品の開発を進めています。

