世界初のDDS抗がん剤のイメージングにより、実用化にさらなる期待質量顕微鏡で“がんに集まる抗がん剤”の薬剤分布が明らかに
2013年11月6日
独立行政法人国立がん研究センター
本プレスリリースのポイント
- DDS(Drug Delivery System:薬物送達システム)抗がん剤は、既存の抗がん剤の分子サイズや性状を変えることにより、薬剤をがん組織に集積させ、治療効果を高める薬剤。
- 質量顕微鏡を用いたDDS抗がん剤の薬剤分布の高精細画像化は世界初の試み。
- イメージングにより、"がん組織に多く長く集まり、かつ正常組織への移行が少ない"DDS抗がん剤の創薬コンセプトが証明された。
独立行政法人国立がん研究センター(所在地:東京都中央区、理事長:堀田知光)は、質量顕微鏡注1を用いてDDS抗がん剤(パクリタキセル内包ナノ粒子、NK105)の薬剤分布を高精細画像化し、創薬コンセプトの通り、DDS抗がん剤が通常の抗がん剤よりもがん組織に多く長く集まり、かつ正常組織にはほとんど移行しないことを明らかにしました。本研究は、東病院臨床開発センター(所在地:千葉県柏市、センター長:大津敦)新薬開発分野 安永正浩ユニット長・松村保広分野長らと株式会社島津製作所(所在地:京都市、代表取締役社長:中本晃)の共同研究によるもので、英科学誌Nature姉妹誌のオープンアクセスジャーナル「Scientific Reports」誌に10月25日付けで掲載されました。
NK105はパクリタキセルをナノ粒子に内包したDDS抗がん剤で、転移・再発乳がんを対象に第III相臨床試験が行われています。パクリタキセルの副作用には手足のしびれ・痛みなどの末梢神経障害がありますが、悪化すると患者さんのQOLが著しく低下するため、効果があっても治療を中断しなくてはならない場合もあります。NK105はがんに集まる抗がん剤として設計され[図1]、効果増強や副作用の軽減が想定されていましたが、実際の薬剤分布を視覚的に直接確認することはできていませんでした。
図1
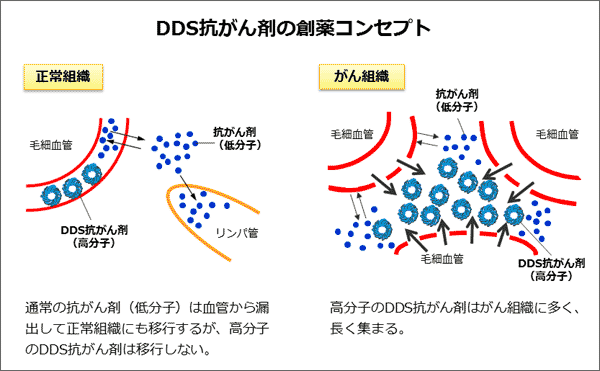
本研究では、島津製作所製の質量顕微鏡を用いて、NK105を投与したマウスのがん組織と正常組織を画像で評価しました[図2]。その結果、NK105ががんの塊(かたまり)の奥深くまで長時間集まっていること、また正常な組織にはほとんど移行していないことが確認されました[図3]。DDS抗がん剤の創薬コンセプトがマウスにおいて証明されたことで、現在進行中の第III相臨床試験の結果が期待されます。さらに、前臨床の段階で詳細な薬剤分布を確認できることは、次世代DDS抗がん剤のドラッグデザインにおいても強力な武器となります。
図2
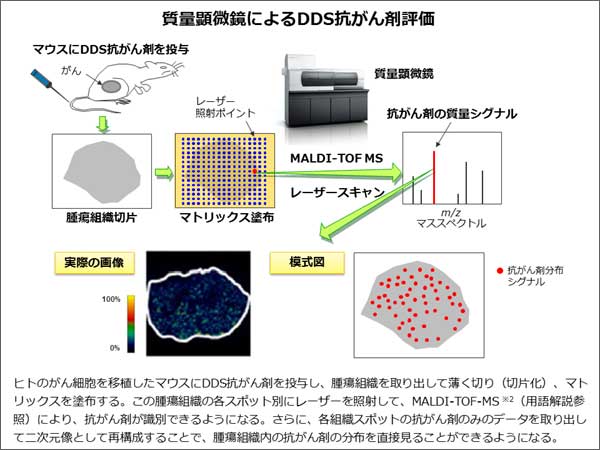
図3
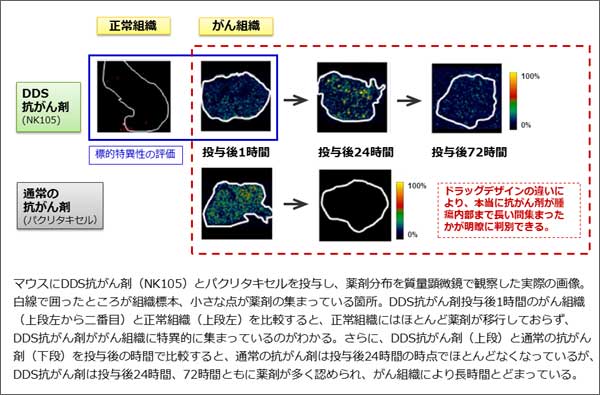
国立がん研究センターと島津製作所は2011年に包括共同研究契約(関連ファイルをご覧ください)を結び、世界をリードするがんの高度先駆的医療技術の開発を目指しています。本研究は包括契約の目標のひとつである"創薬プロセス革新のための薬物動態解析"の成果であり、今後も緊密な連携を図りながら、より効果的で副作用の少ない、患者さんにやさしい抗がん剤開発に取り組んでまいります。
注:本研究は国立がん研究センターがん研究開発費(特別枠)「がんナノテクノロジー研究プラン」により行われました。
原論文情報
問い合わせ先・報道担当
- 問い合わせ先
独立行政法人国立がん研究センター東病院 臨床開発センター
新薬開発分野 分野長 松村 保広
Eメール:yhmatsum●east.ncc.go.jp(●は@に置き換えてください)
電話番号:04-7134-6857 - 報道担当
独立行政法人国立がん研究センター 広報企画室
電話番号:03-3542-2511(代表)
ファクス番号:03-3542-2545
Eメール:ncc-admin●ncc.go.jp(●は@に置き換えてください)
用語解説・補足情報
- 注1 質量顕微鏡:科学技術振興機構「先端計測分析技術・機器開発プログラム」の支援を受けて、光学顕微鏡と質量分析計を融合した日本オリジナルの分子イメージング装置。従来の質量分析法では、生体組織を破砕・分離してから目的分子を測定するため、分子が生体試料のどの部位に分布しているか評価することが不可能でしたが、質量顕微鏡は、見ているものや、見ている場所に含まれている分子をそのまま質量分析することが可能です。これまでの分子イメージング装置では、通常100ミクロンから200ミクロンであった解像度が、質量顕微鏡では最小5ミクロンでの細胞レベルを判別できる高解像度イメージングを可能とするため、これまで判別できなかった細胞内薬物分布を解析する手法として期待されます。本研究はプロトタイプ機を用いて得られた成果で、本年4月に製品化されています。
- 注2 MALDI-TOF MS(マルディ・トフマス):MALDIとは、Matrix Assisted Laser Desorption/Ionization(マトリックス支援レーザー脱離イオン化法)の略称です。サンプルはイオン化されやすい性質をもつマトリックスと均一に混合された状態にあります。ここにレーザー光を当てると、サンプルとマトリックスは熱エネルギーにより気化されます。同時にサンプルとマトリックス間でプロトンの授受が行われ、サンプルがイオン化されます。TOFMSとは、Time of Flight Mass Spectrometry(飛行時間型質量分析法)の略称です。イオン化された分子の一定距離内での飛行時間は、分子の質量とイオン化された電荷数に依存します。分子が軽いほど、あるいは電荷が多いほどスピードが速くなるため、飛行時間は短くなります。これらは質量電荷比m/z値として測定され、各分子に特徴的な値をとります。したがって、質量電荷比m/z値がわかれば、その分子を特定することができます。
- 注:NK105の治験について
NK105は現在、日本化薬株式会社が国際共同第III相治験を実施しています。国立がん研究センター東病院と日本化薬株式会社は、高分子ミセルの研究分野で研究受託契約を結んでいます。
