不必要な薬の投与を回避し、本当にその薬を必要とする患者さんに投与する、より高い精度の個別化治療を実現大腸がんの複数のRAS遺伝子変異を同時検出する日本発の体外診断用医薬品の開発に成功
2015年2月23日
独立行政法人国立がん研究センター
G&Gサイエンス株式会社
成果のポイント
- KRAS遺伝子(エクソン2領域)に変異のある大腸がんでは、抗EGFR抗体薬の効果が期待できないため、投与前に変異の有無を調べる検査が行われる。
- 近年、抗EGFR抗体薬が無効な複数のRAS遺伝子変異が報告されたが、これらの変異は従来の体外診断用医薬品では測定できない。
- アカデミアと企業が連携し、複数のRAS遺伝子変異を同時に検出可能な、簡便かつ低コストの体外診断用医薬品の開発に成功。本年1月27日付で日本国内の製造販売承認を取得。
- 一人ひとりのがんの遺伝子の状態に合わせた、より高い精度での個別化治療が実現可能に。
独立行政法人国立がん研究センター(理事長:堀田知光、東京都中央区、略称:国がん)とG&Gサイエンス株式会社(外部サイトにリンクします)(代表取締役:阿部由紀子、本社:福島市、以下G&Gサイエンス)は、切除不能進行・再発大腸がんにおける抗EGFR抗体薬(注1)の新たなコンパニオン診断薬(注2)の開発に成功しました。
この診断薬は、複数のRAS遺伝子(KRAS遺伝子(注3)エクソン(注4)2、3、4領域およびNRAS遺伝子(注3)エクソン2、3、4領域)の変異を同時に検出できる体外診断用医薬品(以下診断薬)です。G&Gサイエンスの親会社である株式会社医学生物学研究所(外部サイトにリンクします)(代表取締役:佐々木淳、本社:名古屋市、以下MBL)により製品化され、2014年6月には欧州での販売に必要なCEマーク(注5)を世界に先駆けて登録、本年1月27日付で日本国内の製造販売承認を取得いたしました。
研究グループは、抗EGFR抗体薬の投与を受けた大腸がん患者さんの臨床検体を収集して網羅的ゲノム解析を行い、KRAS遺伝子エクソン2領域の変異以外の新たなバイオマーカーの探索・同定を試みました。その結果、海外の報告と同様、KRAS遺伝子エクソン2領域以外のRAS遺伝子変異を有する大腸がんにおいても抗EGFR抗体薬が無効であることを確認しました。この研究成果をもとに、G&GサイエンスがこれらのRAS遺伝子変異を同時検出できる体外診断薬の開発に着手し、従来の遺伝子検査法と高い相関を示す診断キット「MEBGENTM(メブジェン)RASKET(ラスケット)キット」(以下RASKET)が誕生しました。
これにより、従来の検査では調べられなかったRAS遺伝子変異型の患者さんに対しても適切な治療を選択することが可能となり、より精度の高い個別化治療が実現できます。
本成果は、早期・探索臨床研究センター大津敦センター長、土原一哉トランスレーショナルリサーチ分野長、東病院 吉野孝之消化管内科長を中心とする多施設共同研究グループとG&Gサイエンスによるもので、独立行政法人科学技術振興機構(JST)(外部サイトにリンクします)研究成果最適展開支援プログラム(A-STEP)(外部サイトにリンクします)実用化挑戦タイプ「中小・ベンチャー開発」(平成23年度)の支援を受けて行われました。
背景
近年、患者さん一人ひとりの生理学的・病理学的特性を考慮し、最適な医療を提供する「個別化医療」の重要性が認識されています。がんの分子標的治療においても、治療薬を投与する前に、治療効果や副作用を予測する各種バイオマーカーにより適切な患者さんを選択することで、治療効果の最大化と副作用の最小化が期待されています。
大腸がんに対する抗EGFR抗体薬の治療効果予測においては、KRAS遺伝子のエクソン2領域(コドン(注6)12、13)に変異のある患者さんには無効であることがわかっており、抗EGFR抗体薬の投与は推奨されていません。2013年には複数の大規模臨床試験の解析結果から、KRAS遺伝子(エクソン3、4領域)、NRAS遺伝子(エクソン2、3、4領域)に変異のある患者さんも治療効果が期待できないとの報告がなされました。大腸がんの薬物療法専門医の間では「RAS遺伝子変異のある患者さんには抗EGFR抗体薬を投与すべきでない」ことが共通認識となったものの、日常臨床でこれらのRAS遺伝子変異を測定できる体外診断薬はありませんでした。
時を同じくして、本研究グループで実施した網羅的ゲノム解析においても、KRASエクソン2領域(コドン12、13)以外のRAS遺伝子変異が抗EGFR抗体薬の治療効果予測マーカーとなることが同定され、世界に先駆けてRAS遺伝子変異を検出する診断キットの開発に着手しました。
研究・開発の方法
臨床検体の収集とバイオマーカーの探索・同定(BREAC試験)
国内7医療機関において、抗EGFR抗体薬であるセツキシマブの投与を受けた切除不能・進行再発大腸がん患者さんの臨床検体(がん組織標本)を収集し、信頼性の高い臨床情報が付随し、かつゲノム解析に適した検体86例について、網羅的ゲノム解析(全エクソン解析(注7))を実施しました。
全エクソン解析によって得られた遺伝子変異の情報と、各施設から提供された患者さんの臨床情報を統計解析し、抗EGFR抗体薬の有効性や安全性にかかわる可能性が高い遺伝子変異を探索しました。この解析によって得られたバイオマーカー候補を、新たに収集した150例において検証した結果、抗EGFR抗体薬による治療が無効であった患者さんには、KRAS遺伝子エクソン3、4領域およびNRAS遺伝子エクソン2、3、4領域のRAS遺伝子変異があることを確認しました。
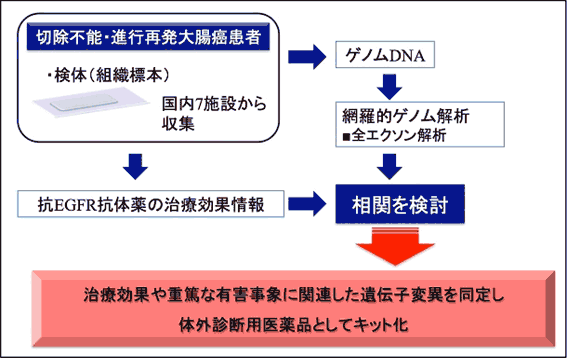
図1:研究方法の概略(BREAC試験)
- セツキシマブを投与された大腸がん患者さんのがん組織標本を国内の7医療機関から収集。
- 並行して、抗EGFR抗体薬の治療効果等の臨床情報も収集し、管理。
- 収集した組織からDNAを抽出し、網羅的ゲノム解析を実施。
- 2と3の情報を合わせて解析を実施。治療薬の効果と関連のある遺伝子変異を特定。これらを検出する診断キットの開発に着手した。
診断キット「RASKET」の開発と臨床性能試験
BREAC試験の成果から得られたバイオマーカーとなる遺伝子変異を測定するため、G&Gサイエンスでは、xMAP®技術(注8)を用いたPCR-rSSO法(注9)により、簡便かつ低コストで、対象変異をマルチに検出可能な体外診断薬の開発に取り組みました。その結果、48種類の変異をわずか50ナノグラムのDNAで同時検出可能なキット「RASKET(ラスケット)」の開発に成功しました。
その後、MBL社がRASKETの開発を引き継ぎ、薬事申請に必要なデータを取得するための臨床性能試験(RASKET試験(注10))を国内6医療機関にて実施。従来の遺伝子検査法(ダイレクトシークエンス法およびScorpion-ARMS法)と比較し、高い相関を示しました。これらのデータをもとに、2014年1月に製造販売承認を申請、本年1月27日付で承認されました。
RASKETは、日常臨床で測定が望まれるKRASおよびNRAS遺伝子のエクソン2領域(コドン12、13)、エクソン3領域(コドン59、61)、エクソン4領域(コドン117、146)領域の変異の有無を一度に測定することが可能な日本発の体外診断薬になります。
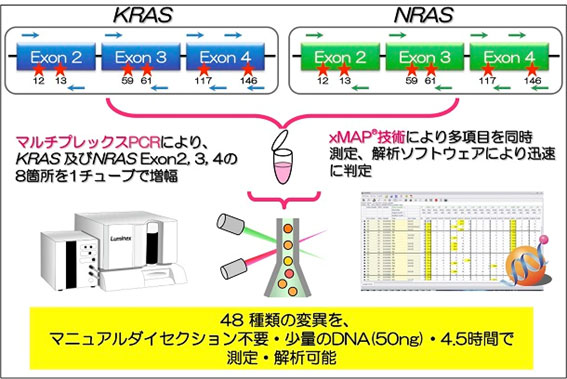
図2:MEBGENTM RASKET キットの特徴
マルチプレックスPCR(一度に複数の遺伝子領域を増幅可能な技術)とxMAP®(Luminex®)テクノロジーを用いることにより、既存のKRAS遺伝子診断キット(注)と同等のDNA量と時間で、48種類の変異の測定・解析が可能。
注:MBL「MEBGENTMKRAS遺伝子変異検出キット」との比較。KRAS遺伝子エクソン2領域の変異12種類を検出する体外診断薬。
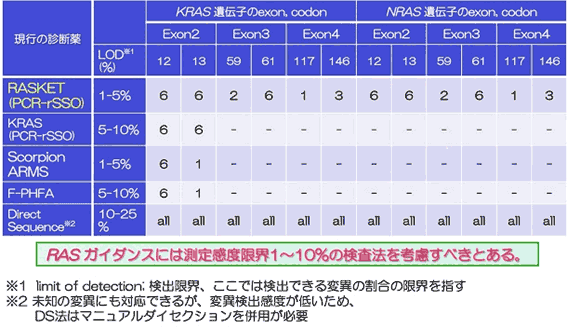
表1:RASKETキットと既存の検査方法との比較
は日本臨床腫瘍学会の「大腸がん患者におけるRAS遺伝子(KRAS/NRAS遺伝子)変異の測定に関するガイダンス」で測定を推奨しているRAS遺伝子変異の種類と、現存の検査法で測定可能な変異をまとめたもの。測定が推奨されるRAS遺伝子変異をすべてカバーしている体外診断薬はRASKETのみ。
期待される医療経済的効果
現在、国内外で切除不能進行・再発大腸がんに対して使用可能な抗EGFR抗体薬にはセツキシマブ、パニツムマブの2剤がありますが、いずれも他の分子標的薬と同様に高額であり、治療開始1ヵ月の薬剤費は約60万円から80万円(注)にのぼります。過去の複数の報告から、KRAS遺伝子(エクソン2遺伝子領域)検査で変異がないと判定された患者さんのうち、約15%から20%に何らかのRAS遺伝子変異があることが明らかになっています。RAS遺伝子検査の導入によって、こうしたRAS遺伝子変異型の患者さんに対する抗EGFR抗体薬の費用を削減することができます。
注:身長170センチメートル、体重60キログラムとして算出。保険適用前の金額。
今後の展望
日本のアカデミアとバイオベンチャー企業の連携のもと、網羅的ゲノム解析により大腸がんの治療効果予測にかかわるバイオマーカーを同定し、臨床現場の声を取り入れた新しいキットを開発、体外診断薬として製造販売承認の取得・発売に成功しました。アカデミアの先進的な研究とベンチャー企業の迅速な開発力を生かした連携体制を構築することで、従来とは比較にならない速さで診断薬の開発が可能となりました。今後もアカデミアと企業が緊密に連携しながら開発を進めていくことで、いち早く臨床現場の要望に応え、患者さんが望む治療を提供できると信じております。
なお、BREAC試験では本発表以外にも有力なバイオマーカー候補が発見されており、現在解析を進めております。これにより、さらなる適切な治療選択が可能になることが期待されます。
論文情報
Takayuki Yoshino, Kei Muro, Kensei Yamaguchi, Tomohiro Nishina, Tadamichi Denda , Toshihiro Kudo, Wataru Okamoto, Hiroya Taniguchi, Kiwamu Akagi, Takeshi Kajiwara, Shuichi Hironaka, Taroh Satoh. Clinical Validation of a Multiplex Kit for RAS Mutations in Colorectal Cancer: Results of the RASKET (RAS KEy Testing) Prospective, Multicenter Study. EBioMedicine. in press. doi:10.1016/j.ebiom.2015.02.007
http://www.sciencedirect.com/science/article/pii/S2352396415000559(外部サイトにリンクします)
研究参加施設・企業と役割
- 検体収集(BREAC試験):国立がん研究センター東病院、静岡県立静岡がんセンター、愛知県がんセンター中央病院、埼玉県立がんセンター、北海道大学病院、がん研究会有明病院、国立病院機構四国がんセンター
- 解析:国立がん研究センター早期・探索臨床研究センター、国立国際医療研究センター肝炎・免疫研究センター(ゲノムワイド関連解析)、東京大学大学院新領域創成科学研究科(データ解析)
- 診断薬開発、臨床評価:G&Gサイエンス、医学生物学研究所
- RASKET試験:国立がん研究センター東病院、愛知県がんセンター中央病院、埼玉県立がんセンター、国立病院機構四国がんセンター、大阪大学医学部附属病院、千葉県がんセンター
用語解説
- 注1 抗EGFR(イージーエフアール)抗体薬:
EGFR(Epidermal Growth Factor Receptor,上皮成長因子受容体)と呼ばれる受容体タンパク質に結合し、その働きを阻害するモノクローナル抗体。EGFRは細胞膜上に存在し、EGF(上皮成長因子)と結合することにより、細胞増殖のスイッチを入れる役割を果たす。EGFRは正常な細胞にも存在するが、一部のがんにおいて多く発現しており、がん治療の標的となっている。 - 注2 コンパニオン診断薬(CoDX):
特定の医薬品の投与を判断するのに欠かせない、治療の有効性・安全性向上のために用いられる体外診断用医薬品または医療機器。 - 注3 KRAS(ケーラス)遺伝子、NRAS(エヌラス)遺伝子:
EGFRからの細胞増殖シグナルを受け取り、下流へ伝達する役割を果たすタンパク質。 - 注4 エクソン:
遺伝子のうち、タンパク質の遺伝情報をコードしている領域。最終的にタンパク質に翻訳される。エキソンとも呼ばれる。 - 注5 CEマーク:
EU地域で販売(上市)される指定の製品に貼付が義務づけられている基準適合マーク。「EU指令」の必須安全要求事項(ESR’s:Essential Safety Requirements)に適合したことを示す。 - 注6 コドン:
タンパク質をコードする遺伝子上に存在する3個1組の塩基配列。大腸がんの一部では、この塩基配列が変化することで本来とは異なるアミノ酸に翻訳される「ミスセンス変異」がみられる。 - 注7 全エクソン解析:
ゲノム中のエクソン領域のみを抽出して解析する方法。多くのがんの原因となる変異は、ゲノム全体の1%から2%に相当するエクソンで検出されている。 - 注8 xMAP®(エックスマップ)技術:
2種類の蛍光色素を異なる比率で配合し染色した100種類のビーズに、個別の解析対象と結合するプローブを固定させることにより、少量サンプルから最大数100種類の解析対象の検出を可能とする技術(下図参照)。2色のレーザーにより、変異型に対応したビーズの同定と、そのビーズ上に結合した変異型の量を高速に測定するのが特徴。米国Luminex社の登録商標。
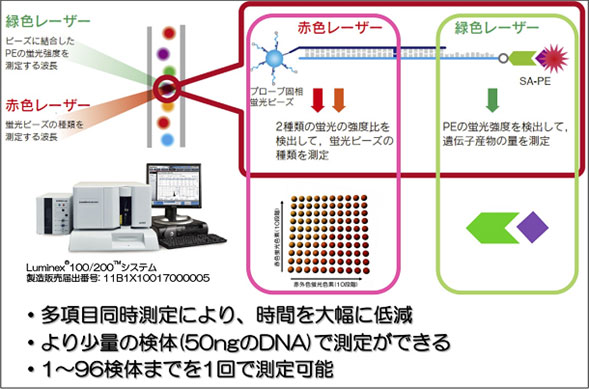
- 注9 PCR-rSSO法:
Polymerase Chain Reaction - Reverse Sequence-Specific Oligonucleotide法を原理とした測定方法。PCRとハイブリダイゼーションにより遺伝子変異を検出する。検出にフローサイトメトリーを基盤とする技術(xMAP®)を用いる。最大500種類の解析対象の検出が同時に可能。 - 注10 RASKET試験:
UMIN試験ID UMIN000011784「Luminex技術を用いた新規RAS遺伝子変異検査試薬の臨床性能試験」
UMIN臨床試験登録システム(外部サイトにリンクします)
プレスリリース
- 大腸がんの複数のRAS遺伝子変異を同時検出する日本発の体外診断用医薬品の開発に成功
関連ファイルをご覧ください。
問い合わせ先
研究内容のお問い合わせ
東病院 消化管内科 吉野 孝之
早期・探索臨床研究センター トランスレーショナルリサーチ分野 土原 一哉
郵便番号:277-8577 千葉県柏市柏の葉6-5-1
電話番号:04-7133-1111(代表)
取材のお申し込み・お問い合わせ
企画戦略局 広報企画室(柏キャンパス)
電話番号:04-7133-1111(代表)、04-7134-6945(直通)
Eメール:ncc-admin●ncc.go.jp(●を@に置き換えください)
RASKETキットに関するお問い合わせ
株式会社G&Gサイエンス 担当:岡田、阿部
郵便番号:960-1242 福島県福島市松川町美郷4-1-1
電話番号:024-537-2350(代表)
ファクス番号:024-537-2386
Eメール:info●gandgscience.co.jp(●を@に置き換えください)
