血小板活性化因子(PAF)生合成遮断による未解決な神経因性疼痛の緩和 次世代鎮痛薬開発のターゲット候補
次世代鎮痛薬開発のターゲット候補
2017年3月28日
国立研究開発法人 国立国際医療研究センター
国立研究開発法人 国立がん研究センター
国立研究開発法人 日本医療研究開発機構
要旨
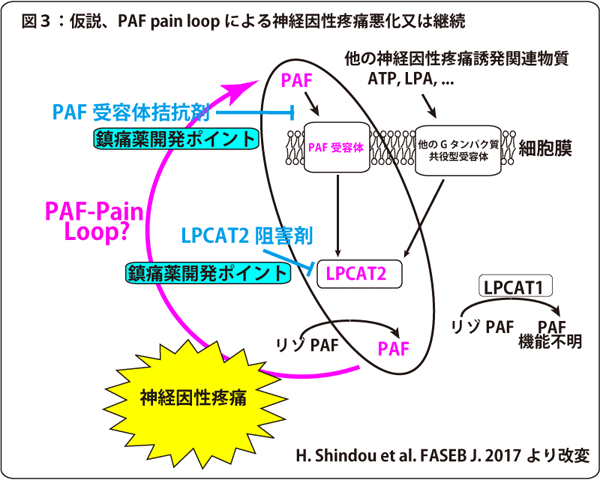
現在、鎮痛薬としてアスピリン等の非ステロイド系鎮痛薬やオピオイド等の医療用麻薬が存在しています。しかし、これらでは解決できない痛みに神経因性疼痛があり、まだ決定的な鎮痛薬が存在しません。この痛みは糖尿病やがんに伴っても発生します。近年、神経因性疼痛(注1)の分子メカニズム研究も進展し、アデノシン三リン酸(ATP)(注2)や血小板活性化因子(PAF)(注3)が神経因性疼痛の発症や持続の関連分子として報告されてきました。今回、私たちはPAFを生合成できないマウス(リゾホスファチジルコリンアシル転移酵素2(LPCAT2)(注4)欠損マウス)を作製しました。このモデルで神経因性疼痛モデル(坐骨神経部分損傷モデル)を作成し疼痛解析を行ったところ、マウス脊髄中のPAFはほとんど検出されず、神経因性疼痛症状であるアロデニア(注5)はほぼ発症しませんでした。神経因性疼痛モデルでは脊髄後角のミクログリア(注6)が増加し、ミクログリアにはLPCAT2発現していることを確認いたしました。PAFはリン脂質メディエーターであり、細胞外刺激により急激に産生されその分解も調節を受けています。細胞をPAFで刺激してもPAFが産生される事から、PAFがPAFを作るというPAF産生ループが存在し、そのため神経因性疼痛を悪化または持続させているのではないかと推測しました。そこでPAFの刺激をブロックするPAF受容体拮抗剤でマウスマクロファージを処理し、PAF産生を誘導するATPで刺激したところ、刺激後5分程度でATPによるPAF産生はピークに達したものの、刺激後10分程度ではPAF産生の低下が認められました。これはPAF産生にループがあることを示唆しています。ここから「PAF Pain Loop」の存在を推測しました。このループを遮断する薬剤は、非ステロイド系鎮痛薬やオピオイド以外の新規カテゴリーの鎮痛薬になり得ると考えています。従いまして、LPCAT2の阻害剤の新規開発、ならびに既に開発済みの多くのPAF受容体拮抗薬を改めて鎮痛薬として見直すことが、神経因性疼痛などの難治性疼痛に悩む患者へ届ける新規鎮痛薬の創薬へとつながると考えています。
研究の背景
神経因性疼痛は既存の鎮痛薬では取り除けません。この神経因性疼痛の発症の持続の分子メカニズムは完全には解明されていませんが、ATPやPAFが関連分子として報告されています。しかし、まだ有効な薬剤は開発されていません。私達は生体膜リン脂質の多様性形成と細胞機能について研究をしており、その中でリン脂質メディエーターであるPAFの生合成酵素(LPCAT2)も研究対象としています。今回、LPCAT2遺伝子欠損マウスを作製し神経因性疼痛との関連を調べました。
本研究の概要・意義
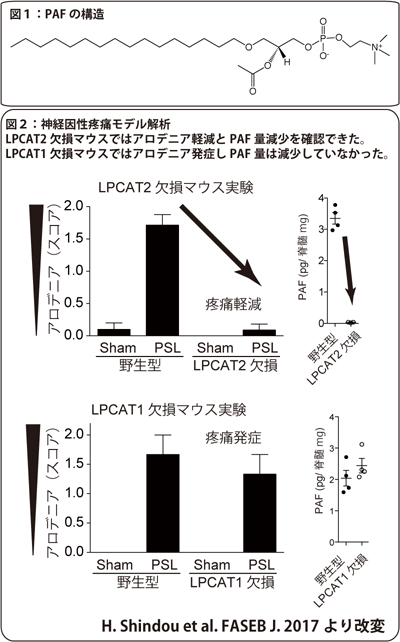
血小板活性化因子(PAF)(図1)はリン脂質メディエーターで、細胞外の刺激に応じて合成されます。現在、PAFの生合成酵素としてLPCAT1とLPCAT2の2種類が知られています。今回、それぞれの酵素欠損マウスを作製し神経因性疼痛を評価しました。疼痛モデルは坐骨神経部分損傷モデルです。LPCAT1欠損マウスは神経因性疼痛の症状の1つであるアロデニアを示しましたが、LPCAT2欠損マウスはアロデニアが軽減していました(図2)。このモデルでは脊髄後角でミクログリアが増加します。LPCAT2も脊髄ミクログリアに発現している事を確認できました。また、脊髄中のPAFの存在はLPCAT1欠損マウスでは確認できましたが、LPCAT2欠損マウスでは検出できませんでした(図2)。細胞をPAFやATP(神経因性疼痛を誘発する)で刺激するとPAFが産生されます。ATP刺激によるPAF産生は、PAF受容体拮抗薬でPAFシグナルを遮断すると減少しました。これは産生されたPAFが再びPAFを産生するフィードバックループの存在を示唆しています。このループが神経因性疼痛を悪化や持続させるPAF pain loopではないかと推測しています(図3)。このループの遮断による新規カテゴリー鎮痛薬開発へ発展させたいと思います。
今後の展望
本成果により、がんの難治性疼痛や慢性疼痛など、神経因性疼痛をターゲットとした新規カテゴリーの鎮痛薬開発への発展が期待されます。既存の薬剤では効かない患者さんの未解決な痛みを少しでも取り除ける可能性があります。
用語解説
注1 神経因性疼痛
神経の損傷や機能異常で起こる慢性の痛み。NSAIDs(非ステロイド性抗炎症薬)やオピオイドなどの医療用麻薬では鎮痛効果が期待できない。
注2 アデノシン三リン酸(ATP)
生体におけるエネルギー伝達体。神経因性疼痛とも関与している。
注3 血小板活性化因子(PAF)
リン脂質の一種。炎症時など細胞外刺激に応じて急激に産生される。Gタンパク質共役型受容体であるPAF受容体を介してシグナルを伝える。
注4 LPCAT2
PAF生合成酵素の一つ。主に炎症性細胞で働き、細胞外刺激により活性化(リン酸化)や発現誘導を受ける。
注5 アロデニア
異痛症と呼ばれる神経因性疼痛の症状の一つ。普段痛みと感じない、触れる様な刺激でも激痛に感じる症状
注6 ミクログリア
脳脊髄に存在する。免疫機能を担うグリア細胞の一種。
論文情報
雑誌名:FASEB Journal(外部サイトにリンクします)
論文名:Relief from neuropathic pain by blocking of platelet-activating factor-pain loop
掲載日:米国東部標準時間3月24日に、先行してオンライン版に掲載
研究グループ・研究支援
本研究は国立国際医療研究センター、国立がん研究センター、東京大学、理化学研究所の共同研究です。日本医療研究開発機構(AMED)「次世代がん医療創生研究事業(P-CREATE)」および「革新的先端研究開発支援事業(AMED-CREST)「疾患における代謝産物の解析および代謝制御に基づく革新的医療基盤技術の創出」研究開発領域」、日本学術振興会科研費、武田科学振興財団、細胞科学財団、小野医学研究財団、中冨健康科学振興財団の支援を受けています。東京大学大学院医学系研究科リピドミクス社会連携講座は株式会社島津製作所、国立国際医療研究センター脂質シグナリングプロジェクトは小野薬品工業株式会社に支援を受けています。なお、AMED-CRESTにおける本研究開発領域は、2015年4月の日本医療研究開発機構の発足に伴い、国立研究開発法人科学技術振興機構(JST)より移管されたものです。
国立国際医療研究センターは本研究全体の総括、疼痛モデルマウスを用いた実験、PAF生合成解析、脂質解析、国立がん研究センターは疼痛実験計画、疼痛モデル作成および実験、東京大学は脂質解析、理化学研究所はLPCAT2欠損マウス作成を行いました。
プレスリリース
- 血小板活性化因子(PAF)生合成遮断による未解決な神経因性疼痛の緩和 次世代鎮痛薬開発のターゲット候補
関連ファイルをご覧ください。
報道関係からのお問い合せ先
国立研究開発法人国立がん研究センター 企画戦略局 広報企画室
郵便番号:104-0045 東京都中央区築地5-1-1
電話番号:03-3542-2511(代表)
Eメール:ncc-admin●ncc.go.jp(●を@に置き換えください)
