個別化医療を推し進める研究基盤構築を促進産学連携全国がんゲノムスクリーニング「SCRUM-Japan」第二期プロジェクトを開始
2017年8月8日
国立研究開発法人 国立がん研究センター
国立研究開発法人国立がん研究センター(理事長:中釜 斉、東京都中央区、略称:国がん)は、肺がん、消化器がんを対象としたわが国初の産学連携がんゲノムスクリーニングプロジェクトSCRUM-Japan(プロジェクト代表者:東病院長 大津 敦)の第二期プロジェクトを4月より開始しました。
2015年2月に開始したSCRUM-Japanは、第一期プロジェクトでは製薬企業15社、国内245医療機関との共同研究により、2017年3月に登録(速報値時4800分例)を完了しました。前身のプロジェクト(肺がん:LC-SCRUM-Japan 2013年開始、大腸がん:GI-SCREEN-Japan 2014年開始)とあわせ、すでに150例以上の患者さんが、遺伝子解析結果に基づいて、分子標的治療薬の医師主導治験や企業治験に参加しています。さらに、複数の分子標的治療薬の臨床応用に貢献しており、中でもROS1融合遺伝子陽性の非小細胞肺癌の遺伝子診断薬および治療薬の国内製造販売承認では大きな成果をあげました。
第二期プロジェクトでは、製薬企業16社との新たな共同研究により、2019年3月までに肺がん2,500例、消化器がん3,000例で、計5,500例の登録を見込んでいます。また、
- 治験への登録を明確化した研究計画書、説明同意文書の作成
- 治験の対象となる進行がんや未治療例の登録の推進
- 治療開始直前のサンプル収集の推進
- 新しい遺伝子解析システムの導入による対象遺伝子の増加と検査期間の短縮
- 臨床ゲノムデータベースを利用した疾患レジストリの作成
などにより、製薬企業とデータ共有を行いながら、国内の新薬開発体制をさらに強力にサポートする予定です。さらに、LC-SCRUM-IBISをはじめとした複数の個別研究が既に開始となっており、SCRUM-Japanは第一期にひき続き有効な治療薬を患者さんに届けることを目標として活動を続けます。
背景
近年、一度に多くの遺伝子を解析できるパネルが開発され、包括的遺伝子診断が可能となったことから、新薬開発試験においてもいわゆるBasket/Umbrella type(注)の試験が多数実施されるようになりました。その一方で、アメリカの先端施設を中心に多遺伝子診断パネルによる遺伝子解析結果に基づいて患者さんに最適な分子標的治療薬を選択するいわゆる「クリニカルシーケンス」が多数行われ、世界的にも急速に普及しつつあります。しかし、臓器横断的にみられる同一遺伝子異常で、必ずしも同様な治療効果が得られないこともわかっています。
SCRUM-Japanは、2012年に同センター研究所で発見されたRET融合遺伝子陽性の非小細胞肺癌の治療開発を行うため、2013年より全国規模での遺伝子スクリーニング(LC-SCRUM-Japan:研究代表者 後藤功一)を開始し、RET阻害剤の医師主導治験を行いました。また、大腸がんを中心とした消化器がんにおいても、拡大RAS遺伝子解析キットの臨床性能試験などを多施設共同研究グループ(GI-SCREEN:研究代表者 吉野孝之)で実施してきました。さらに、多遺伝子解析パネルの開発が進み、疾患にかかわらず包括的な遺伝子診断が可能となり、2つのグループを統合し、2015年2月よりSCRUM-Japanとして同一の多遺伝子解析パネルによる診断と新薬開発試験をわが国全体で効率的に実施する体制を構築しました。SCRUM-Japanの理念は、各種規制案件を満たした先端的な診断・治療薬開発試験を最大限実施することで、わが国のがん患者さんへいち早く有効な薬剤を届けるとともに、海外に負けない競争力を持ったわが国全体の先端的診断・治療薬開発研究基盤を構築することです。
第一期プロジェクトの成果
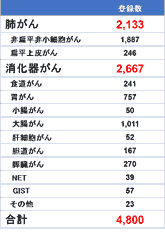
表1:第1期 SCRUM-Japan
疾患別登録数
(2015年2月から2017年3月)
がんゲノム疫学データの構築
2015年2月の登録開始から2017年3月末までに、非小細胞肺がん2,133例と消化器がん2,667例の合計4,800例の登録が終了しており(表1)、現在臨床データの収集と整合性の確認作業を進めています。今後大規模な臨床ゲノムデータの詳細を報告する予定です。
臨床・ゲノムデータの共有化
AMEDで採択された研究事業(代表者:土原一哉)により、SCRUM-Japanに登録された症例の臨床・ゲノム情報は各種セキュリティーガイドラインに準拠した上でデータベース化を行い、2016年6月よりすべての参加製薬企業および施設内セキュリティー確保体制が確認された医療機関から順次オンラインでのデータ共有を開始しています(図2)。このシステムにより疾患ごとの日本人遺伝子異常頻度や施設分布などが閲覧可能となり、各企業および施設での研究に自由に使用できる体制を確立しています。データベースへの1か月あたりのアクセス件数は5,000件を超え、既に多くのアカデミア・企業研究者に利用されています。データの利用は制限を設けず、わが国全体での創薬や各種TR研究の促進につながることを期待しています。
図2:臨床・ゲノムデータのオンライン共有
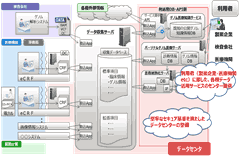
高セキュリティーデータストレージシステム
(国内IT企業との共同開発:AMED土原班)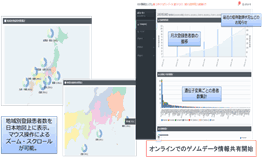
ゲノム情報のオンラインデータ共有開始
(2016年6月
企業・医師主導治験での成果
LC-SCRUM-JapanRET融合遺伝子陽性非小細胞肺がんに対するバンデタニブの医師主導治験(研究代表者:後藤功一)にて、奏効率53%と良好な成績を得て、現在、適応拡大承認申請に向けて準備を進めています。さらに、企業治験として実施されたROS1融合遺伝子陽性例に対するクリゾチニブ、BRAF変異陽性例に対するダブラフェニブ+トラメチニブの試験でもそれぞれ77%、63%と高い奏効率が得られた結果、2017年5月にクリゾチニブのROS1融合遺伝子陽性肺癌への適応拡大が承認され、ダブラフェニブ+トラメチニブも当該企業により適応拡大の承認申請中です。
GI-SCREEN-JapanGI-SCREEN-Japan単独時代に実施した拡大RAS遺伝子変異測定キットの臨床性能試験を国内ベンチャー企業と実施し、すでに日欧での承認取得により実臨床で普及しています。また、大腸がんBRAF変異陽性例に対する企業治験への登録が終了し、次の医師主導治験を2017年度に開始予定です。
第二期SCRUM-Japanの新規プロジェクト
第一期との主な変更点は、遺伝子診断パネルの更新、治験への組み入れ目的であることの明確化、遺伝性腫瘍関連遺伝子の偶発的発見(incidental findings)が発生した際の患者さんへの情報開示に関する希望の有無を含めたIC文書の改訂と、その後の遺伝相談体制の構築などです。さらに、下記を始めとしたプロジェクトが同時進行で構築・実施されています。
新薬承認審査時に活用するための疾患レジストリの構築
SCRUM-Japanで対象としている遺伝子異常は極めて低頻度であるため、新薬開発は大規模な症例数でのスクリーニングが必要となり、比較試験での有効性評価は現実的に困難です。それに対応するため疾患レジストリを活用した新薬承認審査の効率化が世界的に期待されています。2016年度からAMEDの研究事業として4つの疾患レジストリが採択されているが、がん領域では唯一の研究グループ(研究代表者:大津敦)として採択されSCRUM-Japanレジストリ構築を開始しています。国際的互換性を持った臨床ゲノムデータとして、わが国がこの領域で国際的にリードすることが期待されています。
臨床ゲノム統合データベースへのデータ提供
ゲノム情報と疾患特異性や臨床特性等の関連について日本人を対象とした検証を行い、臨床及び研究に活用することができるデータベースの整備を開始しました。現在、がん領域のクリニカルシーケンスに関する分野では共通フォーマットの作成が行われています。第2期プロジェクト終了後に公開用のデータを提供予定で、わが国全体の研究者への利用が期待されます。
人材育成システムの構築
SCRUM-Japanにおいてはすでに4,800例に及ぶ解析経験の中で、遺伝子解析に適した病理検体の固定・保管法の標準化、遺伝子解析結果の臨床的意義付けを進めるための専門家パネルの構築法、遺伝性腫瘍の相談体制等に関する情報提供や教育を主として拠点施設に実施してきました。今後ゲノム医療を実臨床へ実装するため、SCRUM-Japanを利用したe-learningを含む教育資材・ガイドラインの作成や研修プログラムの整備を急ピッチで進めています。今後、拠点施設からの医師、CRCなどの研修受け入れを国立がん研究センター東病院で開始する予定です。
実施予定期間
2017年4月から2019年3月31日(更新の可能性あり)
対象症例
肺がん、消化器がん(大腸がん(直腸がん、結腸がん含む)、胃がん、食道がん、肝細胞がん、胆道がん(胆のうがん、肝内胆管がん含む)、膵がん、小腸がん(十二指腸がん含む)、虫垂がん、肛門管がん、消化器原発の神経内分泌腫瘍/癌(NET、NEC、MANEC)、消化管間質腫瘍GIST)
目標症例数
肺がん2,500例
消化器がん3,000例
参加企業(2017年7月現在)
アステラス製薬株式会社、アストラゼネカ株式会社、エーザイ株式会社、MSD株式会社、小野薬品工業株式会社、協和発酵キリン株式会社、第一三共株式会社、大鵬薬品工業株式会社、武田薬品工業株式会社、中外製薬株式会社、日本イーライリリー株式会社、日本ベーリンガーインゲルハイム株式会社、ノバルティス ファーマ株式会社、ファイザー株式会社、ブリストル・マイヤーズ スクイブ株式会社、メルクセローノ株式会社
参加医療機関(2017年7月1日現在)
LC-SCRUM-Japan:273施設
GI-SCREEN-Japan:20施設
用語解説
注:Basket/Umbrella type:バスケット試験 共通する遺伝子変異の種類をもつ、複数のがん種を1つのグループとし、その共通する遺伝子異常に対して効果がある薬剤を使用する試験。
アンブレラ試験 1種のがんでドライバー遺伝子を複数特定し、その遺伝子を標的とする薬剤を投与すること。バスケット・アンブレラは、その2つの試験を組み合わせた試験で、国内ではSCRUM-Japanが関連する付随治験が先駆けとなっており、希少な遺伝子異常をもつ患者さんに治療を届ける取り組みです。
お問い合わせ先
研究内容についてのお問い合わせ
国立研究開発法人国立がん研究センター(柏キャンパス)
LC-SCRUM-Japan 担当:後藤功一
GI-SCREEN-Japan 担当:吉野 孝之
SCREEN-Japanデータセンター 担当:土原 一哉
取材・報道関係からのお問い合わせ
国立研究開発法人国立がん研究センター
企画戦略局 広報企画室(柏キャンパス)
電話番号:04-7133-1111(代表) 04-7134-6945(直通)
Eメール:ncc-admin●ncc.go.jp(●を@に置き換えください)
