食道がんを早期から検出できる血液中マイクロRNAの組み合わせ診断モデル作成
本研究のポイント
- 過去最多の数で食道がんを有する方と有さない方の血清マイクロ RNA 網羅的発現解析を行った。
- 食道がん患者で有意に変化する複数のマイクロRNAを同定し、それらの組み合わせにより食道がんを早期から高精度で検出できる診断モデルの作成に成功。
- 食道がん診断血液スクリーニングの実現に大きな前進をもたらす成果である。
- 「体液中マイクロRNA測定技術基盤開発プロジェクト」の研究成果で、今後、実用化に活用される。
概要
国立研究開発法人国立がん研究センター(理事長:中釜 斉、東京都中央区)研究所と中央病院の研究チームは、血液により高い精度(感度(注1)96%、特異度(注1)98%)で食道がんを検出する診断モデルの作成に成功しました。
本研究では、国立がん研究センターバイオバンク(注2)などより収集した血液検体を用いて、食道がんを有する方566名と有さない方4965名の血液(血清)中のマイクロRNAを網羅的に解析し、食道がんで有意に変化する複数のマイクロRNAを同定し、そのうち6種のマイクロRNAを組み合わせることで食道がんを早期から検出可能であることを確認しました。
本研究は、13種のがんについて血液による診断システム開発を産官学で目指す「体液中マイクロRNA測定技術基盤開発プロジェクト(2019年3月終了)」(国立研究開発法人日本医療研究開発機構 次世代治療・診断実現のための創薬基盤技術開発事業)の研究成果のひとつで、今後、プロジェクト参加企業による実用化と、前向き臨床研究での検証を経て新たな検査法としての確立が期待されます。
また、本研究成果は米国科学誌「JAMA Network Open」に5月24日掲載されました。
本研究成果について、国立がん研究センター中央病院消化管内科 医長の加藤健は次のように述べています。「食道がんは早期診断で根治を目指した治療ができる病気です。微量の血液検査で症状がない段階から食道がんを早期発見できる可能性を示した点で大きな意義があると考えます。今後、さらに検証を重ねて、マイクロ RNA検査による一次スクリーニング、そして二次スクリーニングには内視鏡検査というプログラムにより、食道がんの早期発見と治療成績向上に寄与するような、実際の現場で役立つ診断マーカーとなることを期待しています。」
研究背景
食道がんは予後不良ながんですが、薬物療法、手術、放射線治療の進歩により治療成績は向上しています。しかし、転移性の腫瘍では根治は難しく、また局所のみの病変で見つかっても、腫瘍の進行によっては手術や放射線治療といった局所治療と薬物治療を組み合わせた比較的負担が大きい治療が必要となります。一方、早い段階で診断された食道がんは内視鏡を用いた負担の少ない治療での治癒を目指すことができますが、早期には自覚症状がないことがほとんどのため、簡便で有用かつ早期診断が可能な診断マーカーの開発は本腫瘍の治療成績向上、および患者さんの生活の質の向上に急務の課題です。
マイクロ RNA は、血液や唾液、尿などの体液に含まれる 22 塩基程度の小さな RNA のことで、近年の研究で、がん等の疾患にともなって患者の血液中でその種類や量が変動することが明らかになっています。そのため、患者さんの負担が少ない診断バイオマーカーとして期待されています。本研究は、食道がん(扁平上皮がん)に特異的なバイオマーカーを同定することを目指し実施しました。
研究概要
本研究では、食道がん566例と、がんを有さない4965例の計5531例全例の血液(血清)中マイクロRNAを網羅的に解析し、食道がん患者で有意に変化する多くのマイクロRNAを同定し、それらの組み合わせを利用した統計的解析により食道がん患者を特異的に判別できる判別式(診断モデル)を作成しました。
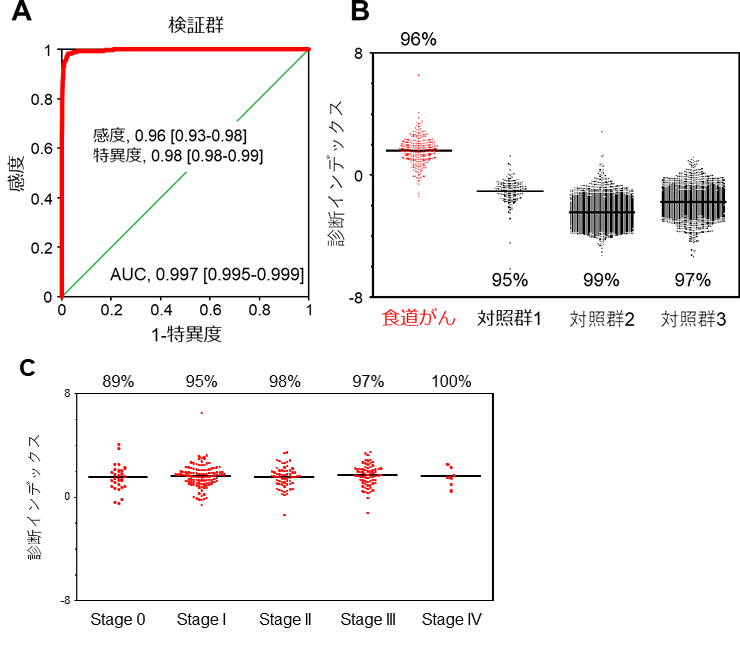
解析対象例を探索群と検証群の2つに分け、その精度を検証した結果、同モデルは検証群の食道がん患者全体の96%を正しくがんであると判別することができ(図A、B)、診断精度の極めて高い(感度96%、特異度98%)診断モデルの作成に成功したことを確認しました。
ステージ別の検証においては、ステージ0、ステージI、ステージII、ステージIII、ステージIVの患者群それぞれを89%、95%、98%、97%、100%の感度で陽性と診断できました(図C)。
展望
本研究により作成された診断モデルは、過去に類を見ない、極めて高い診断精度であり、かつその精度を血液からの情報のみで実現できたことは大変意義の大きい成果です。本研究成果を今後、実際の患者さんで確認する前向きの臨床研究でさらに検証および最適化を重ねることで、食道がんスクリーニング検査確立の実現に向けて大きな前進が強く期待できます。血液検査による食道がんスクリーニング検査の確立は、食道がん診療にパラダイムシフトをもたらす試金石となり得るもので、その実現に向けて今後も研究を継続します。
共同研究者
本研究は、以下の施設を含む、研究グループによる取り組みの成果です。また、研究に使用した血清は、国立がん研究センターバイオバンク、国立長寿医療センターバイオバンク等から提供いただきました。試料提供にご協力・ご賛同してくださった患者・家族の皆様へも深く御礼を申し上げます。引き続き、生体試料を用いた研究に対するご理解とご支援をお願いいたします。
- 国立がん研究センター
中央病院 乳腺・腫瘍内科 医員 須藤 一起(筆頭著者)
中央病院 消化管内科 医長、バイオバンク・トランスレーショナルリサーチ支援室 室長 加藤 健
研究所 客員研究員 落谷孝広[前 分子細胞治療分野 プロジェクトリーダー、現 東京医科大学 医学総合研究所 分子細胞治療部門 教授](責任著者)
研究所 特任研究員 松崎潤太郎 - 国立長寿医療研究センター
メディカルゲノムセンター センター長 新飯田俊平 - 東レ株式会社
- 株式会社ダイナコム
発表論文
雑誌名
JAMA Network Open
タイトル
Development and Validation of an Esophageal Squamous Cell Carcinoma Detection
Model by Large-Scale MicroRNA profiling
著者
Kazuki Sudo, Ken Kato, Juntaro Matsuzaki, Narikazu Boku, Seiichiro Abe, Yutaka Saito,Hiroyuki Daiko, Satoko Takizawa, Yoshiaki Aoki, Hiromi Sakamoto, Shumpei Niida,Fumitaka Takeshita, Takahiro Fukuda, Takahiro Ochiya
DOI
10.1001/jamanetworkopen.2019.4573
URL
https://jamanetwork.com/journals/jamanetworkopen/fullarticle/2734072?resultClick=3
用語解説
注1:感度・特異度
感度と特異度は、診断技術の信頼性を示す指標で、病気に罹っている人を検査したとき正しく病気と判定する(陽性)確率を感度、逆に、特定の病気に罹っていない人を検査したとき正しく陰性と判定する確率を特異度と呼びます。陽性判定のしきい値を下げれば検査の感度を上げ患者の発見率を高めることができますが、その場合、特異度は下がり正常の方を患者と誤る偽陽性が増えることになります。正確な診断を実現するには、特異度を高く維持したまま感度を高める技術革新が必要です。
注2:バイオバンク
参考
2014年6月13日プレスリリース
13種類のがんを1回の採血で発見できる次世代診断システム開発が始動2018年10月17日プレスリリース
卵巣がんを早期から検出できる血液中マイクロRNAの組み合わせ診断モデル作成2019年3月28日プレスリリース
骨軟部腫瘍の良悪性を高精度に識別可能なマイクロRNAの診断バイオマーカー同定報道関係のお問い合わせ先
国立研究開発法人国立がん研究センター
企画戦略局 広報企画室
郵便番号:104-0045
東京都中央区築地5-1-1
電話番号:03-3542-2511(代表)
ファクス番号:03-3542-2545
E-mail:ncc-admin●ncc.go.jp(●を@に置き換えてください)
