オンライン治験に関する実務手順書の公開とDCTコンサルテーション開始国立がん研究センターのノウハウを全国の医療機関へ展開し、医薬品の開発促進とドラッグラグ・ドラッグロス解消に貢献
2025年8月26日
国立研究開発法人国立がん研究センター
発表のポイント
- 遠隔診療技術を活用した治験(オンライン治験)は、治験実施機関へのアクセスが困難で治験に参加できない患者さんの障壁を解消する有効な手段であり、特に患者さんが少なく、医薬品の開発が進みにくい希少疾患や小児疾患に対して、ドラッグラグ・ドラッグロス解消に貢献することが期待されています。
- 国立がん研究センター中央病院では希少がんを対象とした医師主導治験においてオンライン治験を導入してきました。この実績を基に、がん領域を対象にしたオンライン治験の導入を目指す研究者向けに、オンライン治験実施のための実務手順書やマニュアル等必要書類の公開とDCTコンサルテーションを開始しました。
- オンライン治験実施のための実務手順書等の公開は、オンライン治験の導入経験が少ない医療機関にとっての指針となることが期待されます。さらに、オンライン診療に関するコンサルテーションも行い、国内のオンライン治験の普及をサポートします。
概要
国立研究開発法人国立がん研究センター(理事長:間野 博行、東京都中央区)中央病院(病院長:瀬戸 泰之、以下「中央病院」)は、オンライン治験(分散型治験:Decentralized Clinical Trial, DCT注1)の導入を目指す医療機関向けに、オンライン治験の実務に必要な手順書やマニュアル、書式などの書類の提供を行い、オンライン治験に関する支援業務(DCTコンサルテーション)を2025年8月26日より無料で開始しました。
オンライン治験では、患者さんが自宅あるいは自宅近隣の医療機関(パートナー施設)から治験実施医療機関にオンラインでアクセスできるようになります。治験登録の促進や治験コストの削減を通じて、医薬品の開発が進み、特に患者さんが少ない希少疾患や小児疾患の領域でドラッグラグ・ドラッグロスの解消につながることが期待されています。一方で、多くの医療機関にとってオンライン治験の立ち上げは初めての試みとなり、多くの労力がかかり導入に躊躇する医療機関が多いのが現状です。
中央病院ではこれまで、希少がんを対象とした2つの経口薬による医師主導治験(TAZETTA試験:NCCH2107/MK012、Perfume試験:NCCH2101/MK011)においてオンライン治験を実施し1、2)、その手法を確立するとともに、治験実施医療機関に求められる実務に関する手順書やマニュアル、書式などを整備しました。中央病院は、オンライン治験の導入を目指す医療機関に必要な書類の提供とコンサルテーションにより支援し、わが国全体でのオンライン治験の推進を図り、速やかな医薬品の開発を進めることによりドラッグラグ・ドラッグロスの解消を目指します。
本取り組みは、国立研究開発法人日本医療研究開発機構(AMED)臨床研究・治験推進研究事業「希少がんプラットフォーム試験へのDCT導入に関する研究開発(研究代表者:中村 健一)」の研究成果です。
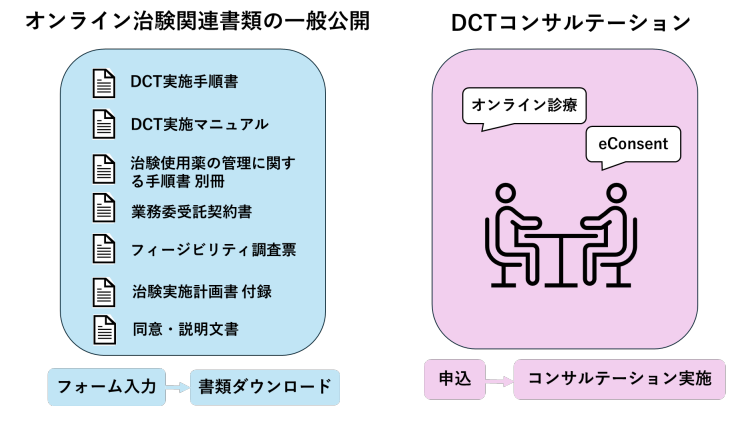
オンライン治験関連書類の入手方法とDCTコンサルテーションの概要
オンライン治験について
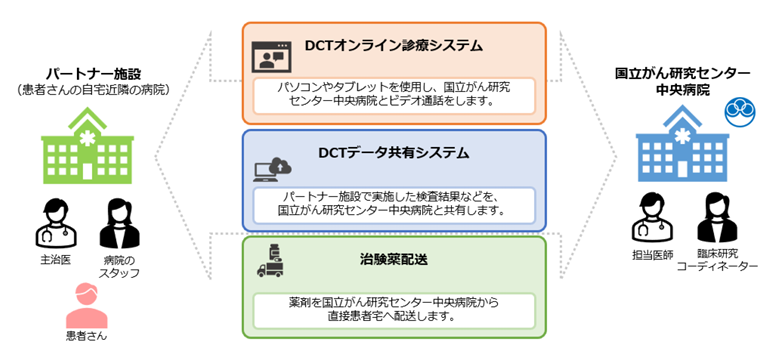
治験の実施にあたっては、患者さんにあらかじめ定められたスケジュールに従い、治験実施医療機関へ繰り返しご来院いただく必要があり、特に遠隔地在住の患者さんにとっては、通院に伴う時間的・経済的・体力的な負担が大きな障壁となっていました。一方、オンライン治験では、遠隔診療技術を活用して、実施医療機関へ来院する負担を軽減します。中央病院が実施するオンライン治験では、血液検査、心電図、胸部X線、CT/MRIなどの各種検査をパートナー施設へ委託し、検査結果はクラウド型システムを通じて中央病院へ共有、その結果を見た中央病院の医師が遠隔地在住の患者さんにオンライン診療を行い、治験薬(経口薬)は中央病院から患者さんのご自宅へ直接配送し、患者さんは中央病院の医師の指示に基づいて服用します。
このような仕組みにより、患者さんは地理的な制約を受けることなく、全国どこからでも治験への参加が可能となり、通院の負担を大きく減らすことができます。また、医療機関にとっても、全国から患者さんが参加可能になることによって、患者登録スピードの加速による早期の治験完了、治験全体のコスト削減に繋がります。さらに、国内の医師主導治験で作成した手順書等を国際共同試験用に応用し、日本とタイの間で国境を越えたオンライン治験”Cross-border DCT”を行う実証プロジェクトも開始しました3)。
一方で、オンライン治験を初めて導入する場合は、病院内外の多くの関係者を巻き込んだ体制づくりや、関連規制への対応、さらにはオンライン診療やデータ転送のためのシステム導入など多くの労力がかかるため、導入を躊躇する医療機関が多いのが現状です。中央病院では、オンライン治験の普及促進を図るため、オンライン治験の導入を検討している医療機関や導入経験が少ない医療機関向けに、これまでの中央病院の実績に基づいた手順書等を公開するとともに、DCTコンサルテーションを実施することといたしました。
オンライン治験の実施体制
国立がん研究センター中央病院による支援の内容
実務書類の提供(無料)
主に以下7点の書類を提供します。
- DCT実施手順書
- DCT実施マニュアル
- 治験使用薬の管理に関する手順書_別冊
- 医師主導治験に関する業務委受託契約書・覚書
- フィージビリティ調査票(施設版)
- 治験実施計画書 付録
- 同意・説明文書
DCTコンサルテーション(無料)
書類の提供に加え、オンライン治験の導入および運用経験が豊富なスタッフによる無料のコンサルテーションを実施します。中央病院ではこれまでに、医師主導治験および企業主導治験、特定臨床研究において、10の医療機関とオンライン治験のパートナー施設としての委受託契約を締結し、実際の運用を行ってきました(2025年7月現在)。これまでに培った知見をもとに、オンライン診療や、eConsent注2、ePRO注3に関するシステムやウェアラブルデバイス等の適切な選定、データ転送のためのシステムの構築、医薬品の臨床試験の実施の基準に関する省令および各種ガイドライン等の規制対応、運用面での課題解決など、多岐にわたるご相談に対応します。
申込方法
書類のダウンロードおよびコンサルテーションは以下の特設ページから申込可能です。
URL:https://www.ncc.go.jp/jp/ncch/division/clinical_research_support/research_management/DCTconsultation/index.html
今後の展望
中央病院は、希少がんでのオンライン治験の導入実績をもとに、全国の医療機関へのオンライン治験の普及を支援していきます。さらに今後、対象領域を拡大して、オンライン治験の普及とその支援に取り組んでまいります。
研究費
令和5-8年度 国立研究開発法人日本医療研究開発機構(AMED)
臨床研究・治験推進研究事業
「希少がんプラットフォーム試験へのDCT導入に関する研究開発」
研究代表者名:中村 健一
参考情報
- 希少がんに対するオンライン治験を開始(2023年6月27日プレスリリース)
- BRAF融合遺伝子陽性の膵がんまたは低悪性度神経膠腫を対象とした 医師主導オンライン治験を開始(2025年2月12日プレスリリース)
- 国立がん研究センターとタイ保健省医療サービス局の間で国境を越えたオンライン治験推進に関する協力覚書を締結(2023年6月27日プレスリリース)
用語解説
注1:Decentralized Clinical Trial(DCT)
オンライン診療などのデジタル技術を用いて、被験者が医療機関に来院しない、あるいは来院する頻度を減らすことを意図した臨床試験のことです。
注2:eConsent
タブレットなどの電子機器を用いて治験の内容を説明し、その内容に対する同意を電子署名として記録する手法・手順のことです。
注3:ePRO
患者さんに電子機器を使用していただき、自らの健康状態や症状、生活の質について報告するシステムです。
お問い合わせ先
オンライン治験の書類およびDCTコンサルテーションに関するお問い合わせ
国立研究開発法人国立がん研究センター中央病院
DCTコンサルテーション事務局
Eメール:dct_ctm●ml.res.ncc.go.jp
広報窓口
国立研究開発法人国立がん研究センター
企画戦略局 広報企画室
電話番号:03-3542-2511(代表)
Eメール:ncc-admin●ncc.go.jp
