ピロリ菌除菌者での初発胃がんリスク診断に成功胃の細胞に溜まったエピゲノム異常で正確にリスク判定できることを確認 実用化に向け検討を開始
星薬科大学
国立研究開発法人国立がん研究センター
発表のポイント
- 胃がんの原因であるヘリコバクター・ピロリ菌(ピロリ菌)の除菌治療を受ける人は、2013年の保険適用以来急増しています。除菌後の人には、現在、対策型検診として2年に1回の胃がん検診が推奨されています。しかし、画一的な検診は胃がんを早期で発見する機会を逃したり、逆に過剰な検診負担が生じたりします。よって、個人のリスクに応じた検診を行うことが重要です。
- がんの原因となるDNAメチル化異常は発がん前の組織にも蓄積しており、健康人でもその蓄積量と胃がんリスクが相関することは、これまでに横断的研究により示されていました。しかし、実際に診療で使える高い信頼性をもつ大規模な前向き研究による証明はありませんでした。
- 今回、ピロリ菌除菌後開放型胃粘膜萎縮をもつ高リスクな健康人を対象とした前向き研究で、発がん前の胃粘膜における胃がんリスクマーカーのDNAメチル化レベルを測定することで、初発胃がんリスクを精密に予測できることが証明されました。また、高リスクな人の中でも特にリスクの高い超高リスクな人を特定することに成功しました。
- 今回の研究で特定された超高リスクな人に対しては、検査間隔を短くすることで胃がんの早期発見および内視鏡的治療が効率的に可能となり、患者さんのQOL向上が期待されます。将来的には、このDNAメチル化異常を用いて、検診が不要な低リスク集団を特定できる可能性もあります。
概要
星薬科大学(牛島俊和 学長)、国立研究開発法人国立がん研究センター中央病院(阿部清一郎 内視鏡科医長ら)からなる研究チームは、ピロリ菌除菌後健康人において、発がん前の胃粘膜組織のDNAメチル化異常を測定することにより、初発胃がんリスクを精密に予測できることを多施設共同前向き研究により明らかにしました。
本研究の成果は、4月16日に国際総合学術雑誌「Gut」に発表されました。
背景
ピロリ菌除菌により発がんリスクは低下するが、ゼロにはならない
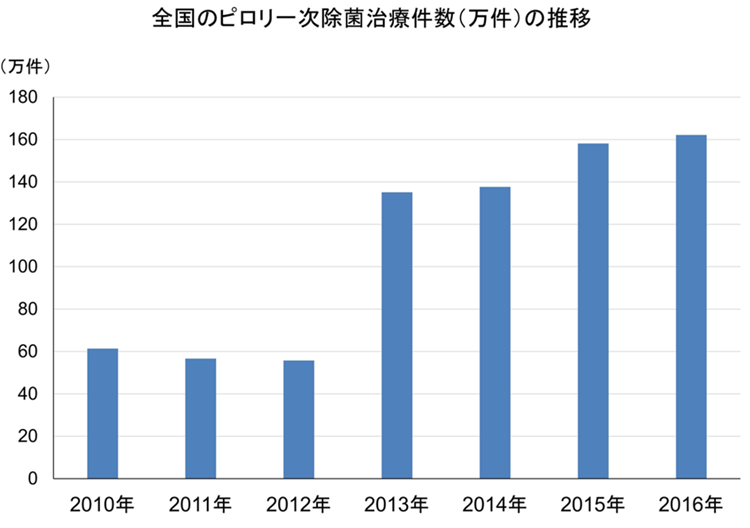
ヘリコバクター・ピロリ菌(ピロリ菌)は胃がんの原因として重要であり、その除菌により胃がんリスクが低下することが知られています。日本では2013年からピロリ菌除菌が保険適用になり、これまでに1,000万人を超える多くの人々が除菌治療を受けています(図1)。除菌後も年率0.5-1.2%程度胃がんが発生するため、2年に1回の胃がん検診が推奨されていますが、画一的な検診は患者さんにとっても医療経済にとっても負担が大きく、個人のリスクに応じた検診を行う必要があります。
2013年のピロリ菌除菌の保険適用以来、
これまでに1,000万人を超える人がピロリ菌除菌を受けたと計算される。
がん前の組織にもDNAメチル化異常が存在し、発がんリスクと関係している
がんは突然変異やDNAメチル化異常注1など、細胞が分裂しても消えない遺伝子の異常により、がん遺伝子が異常に働くことや、がん抑制遺伝子が働かなくなることで発生します。これらの異常は、病原菌や発がん物質などへの曝露により様々な遺伝子に誘発され、がんが発生する前の正常組織に徐々に蓄積しています。
がんが発生する前の組織では、突然変異の蓄積はとても少なくて測定が困難でした。一方、DNAメチル化異常は胃や大腸などに多く蓄積注2している場合があり、その測定が容易でした。そこで、古くから、がんが発生する前の胃粘膜組織に蓄積したDNAメチル化異常の量と胃発がんリスクが相関することが横断的研究により示されてきました。しかし、この知見を臨床で使用する根拠となる高い信頼性をもつ、大規模な前向き研究による証明がありませんでした。
研究内容
発がん前の組織のDNAメチル化異常の測定により、初発胃がんリスクを予測
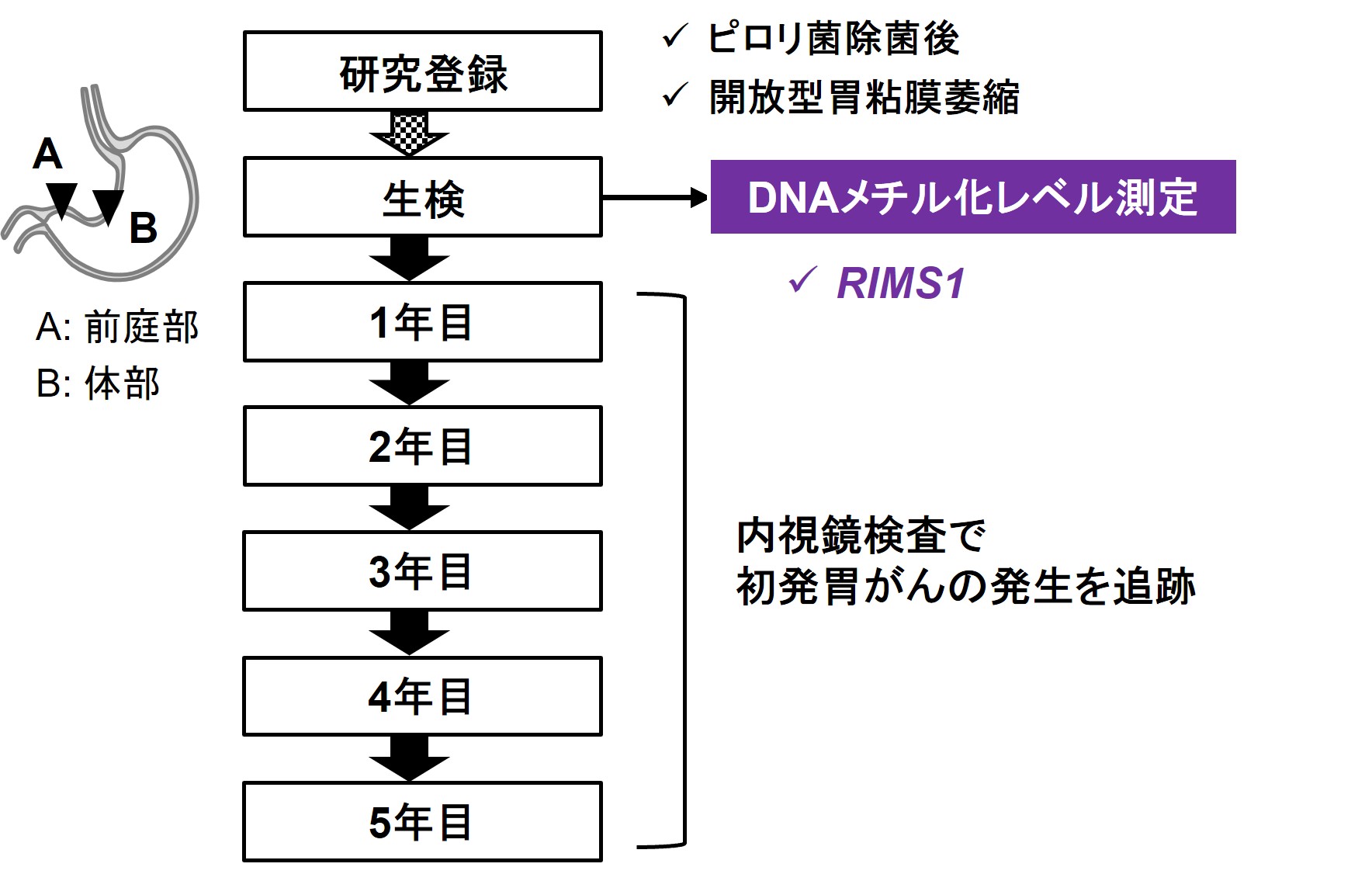
DNAメチル化異常の測定により、健康人で初発胃がんリスクを予測できることを証明するために、ピロリ菌除菌後健康人を対象として多施設共同前向き研究を行いました(UMIN-CTR000016894に登録)。今回の研究では、ピロリ菌除菌後でも臨床的に胃がん高リスクと考えられ、新たな対策が必要とされる可能性がある開放型胃粘膜萎縮を持つ健康人を対象としました。参加者の方に研究内容について説明しご同意いただいた後、胃前庭部および体部の2か所から胃粘膜の生検をさせていただきました。生検自体は、保険診療での組織検査の際に普通に実施されている手法です。採取した検体由来DNAを用いて、胃がんリスクマーカーRIMS1遺伝子のDNAメチル化レベルの測定を行いました。その後、5年間、毎年内視鏡検査により胃がんの検査を行いました(図2)。
同意をいただいて研究参加登録をしたのち、生検を採取させていただいいて観察を開始、
その後、毎年の内視鏡検査を受けていただいた。
生検検体でのDNAメチル化レベルと胃がん発生率との関連を証明することを目的とした。
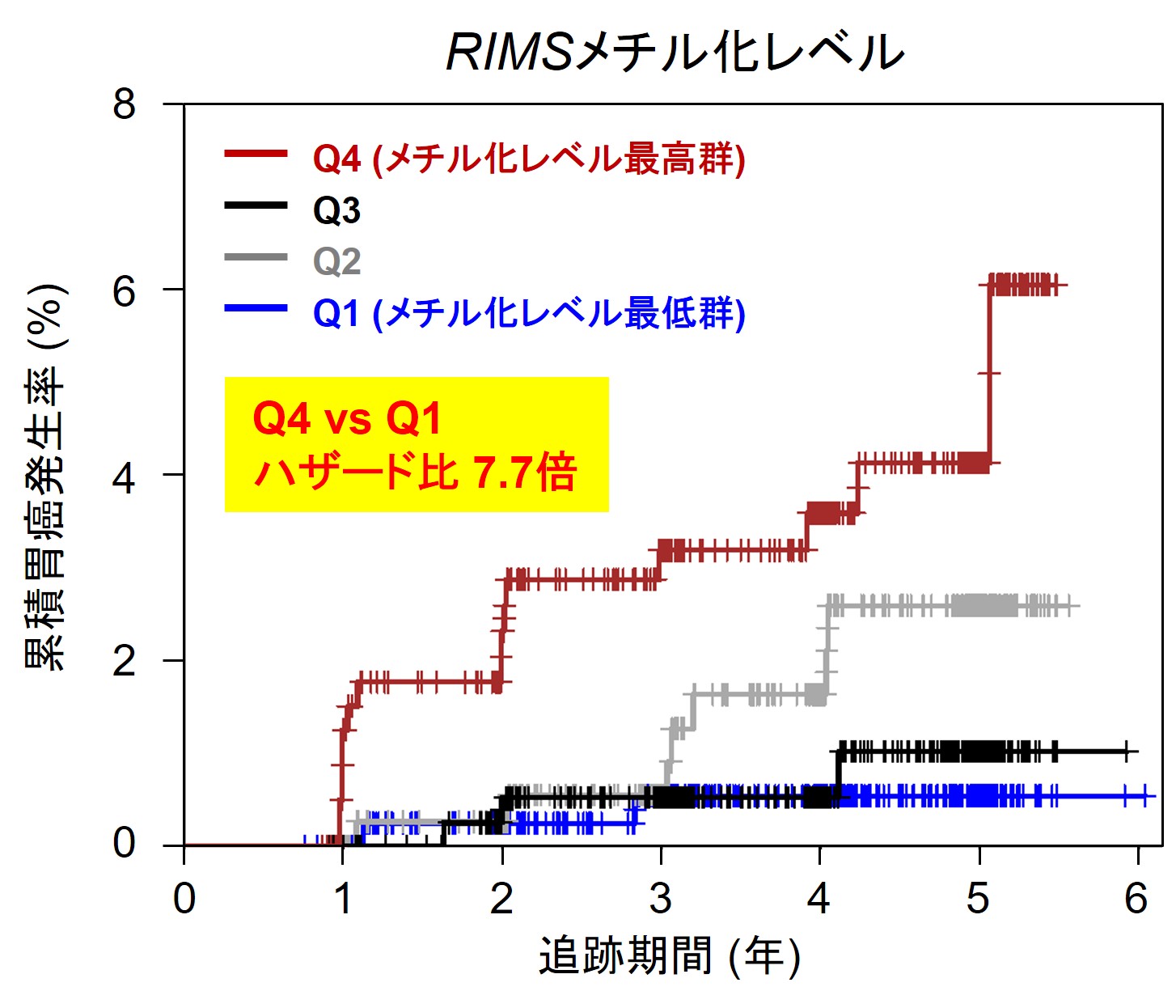
1,757名の方について生検を行い、内視鏡観察が始まり、そのうち1,624名が1回以上の追跡を受けてくださいました(追跡期間の中央値 = 4.05年)。このうち27名の方に胃がんが発生しました。1回以上の追跡を受けた1,624名の方をRIMS1メチル化レベルにより4つの群に分け、胃がんとの関連について解析を行ないました。その結果、メチル化レベルが最も高かった1/4の人たち(Q4)は、最も低かった1/4の人たち(Q1)に比べて、初発胃がん発生リスクが7.7倍高いことがわかりました(図3)。
メチル化レベルが最も低かった1/4の人たちに比べて、
最も高かった1/4の人たちは7.7倍胃がん発生のリスクが高かった。
高リスクな集団の中でもさらに超高リスクな集団を特定
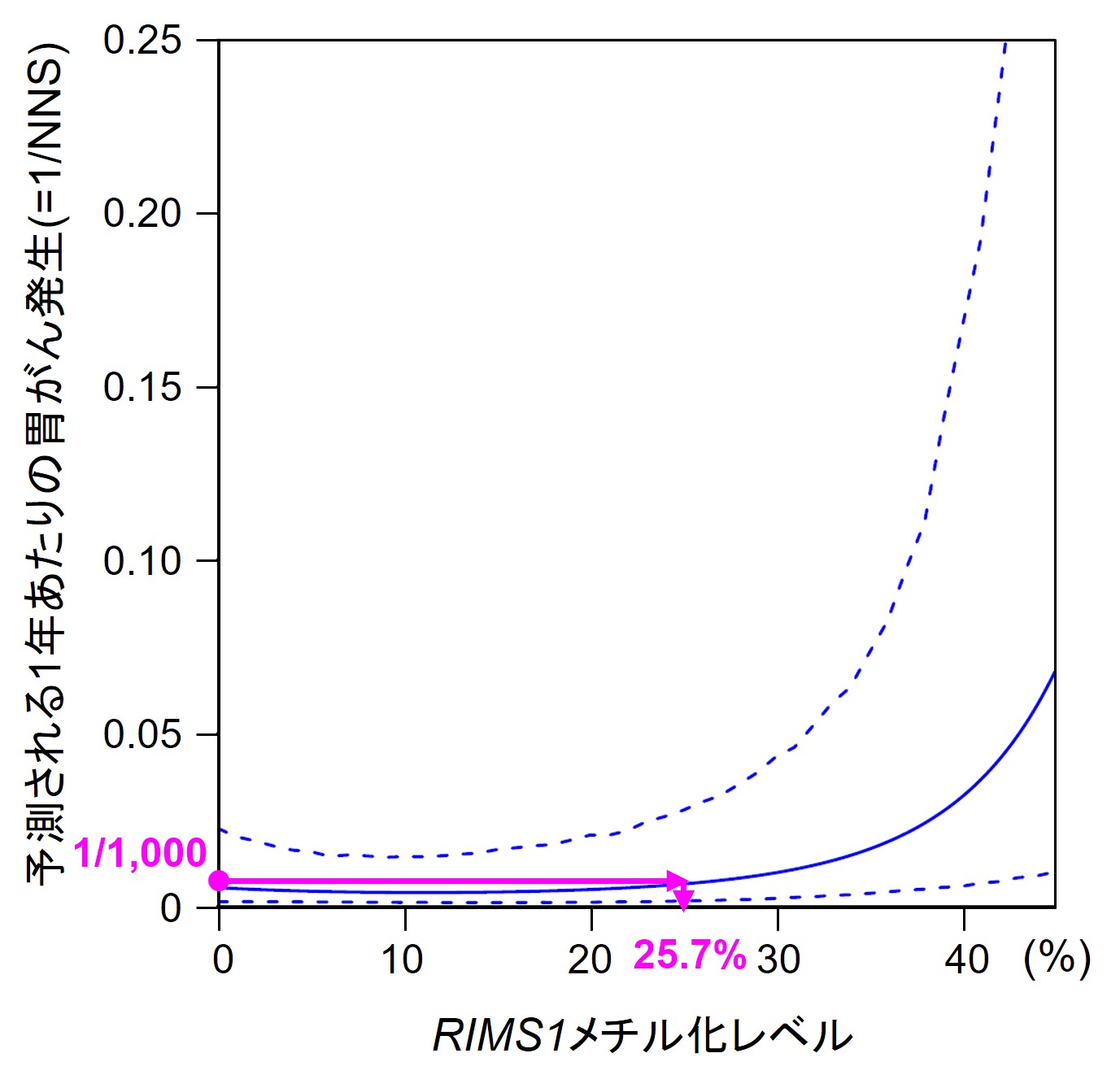
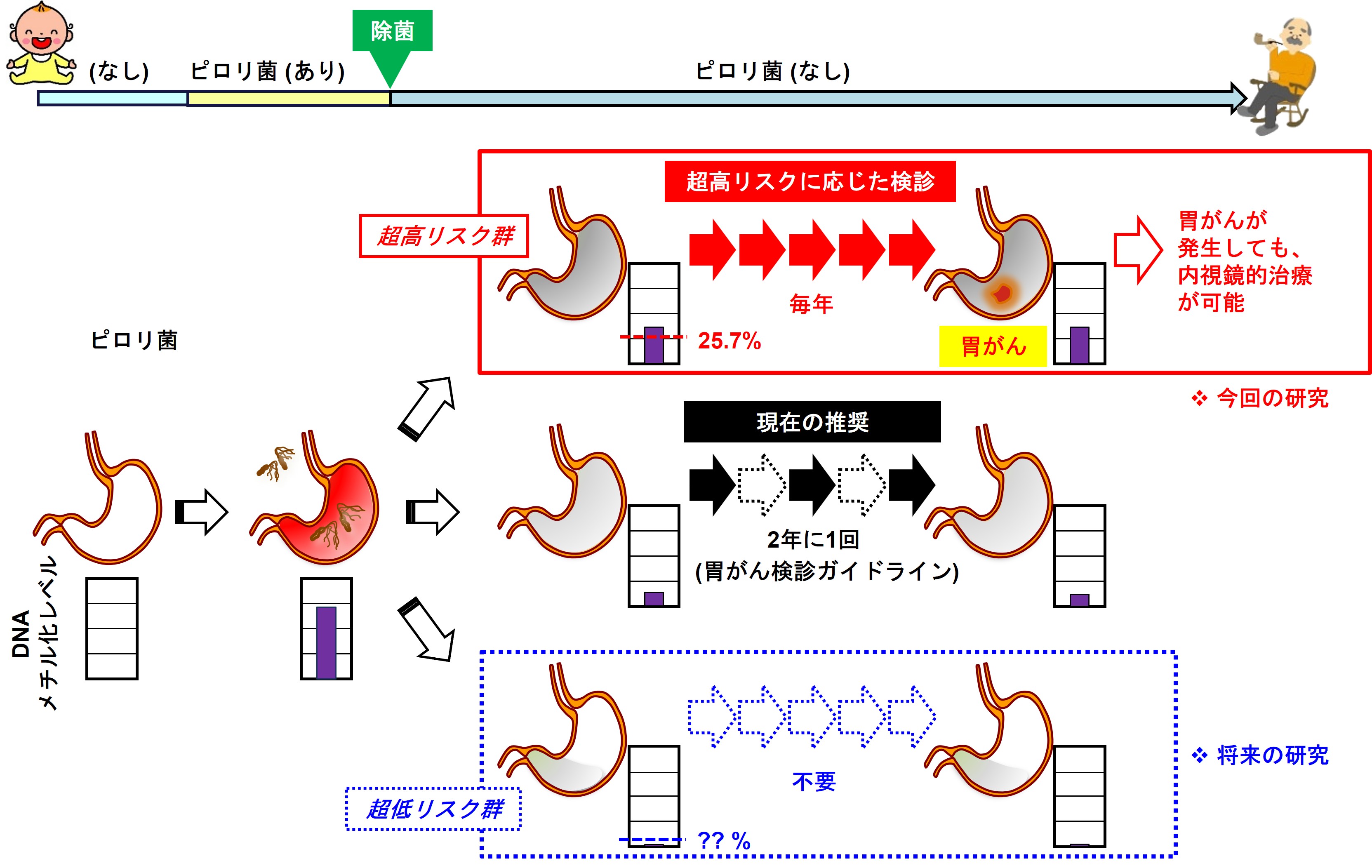
本研究の対象者は全員、臨床的に高リスクとされる開放型胃粘膜萎縮を有する健康人です。その中でも特にリスクの高い超高リスク群を特定することを試みました。対象者におけるRIMS1メチル化レベルと胃がん発生率の関係を計算し、RIMS1のメチル化レベルが25.7%を超えると、1年間で胃がんを発生する頻度が急速に増加しており、超高リスクと考えられました(図4)。この超高リスクの人たちには、2年に一度の経過観察よりも、がんが発生したとしても内視鏡治療が可能なうちに発見が可能になると予測されるため毎年の経過観察が推奨される可能性が高いと考えられます。
RIMS1のメチル化レベルの上昇に従い、一年間に胃がんが発生する人の人数を計算した。
実線は計算値で、点線が95%信頼区間。
胃がんリスクマーカーRIMS1のメチル化レベルが25.7%を超えると急激にリスクが高くなる。
詳細には、1,000人が内視鏡検査を受けると1人が胃がんという頻度が、急激に高くなる。
今後の展望
本研究により、ピロリ菌除菌後の健康人において、発がん前の胃粘膜組織におけるDNAメチル化レベルを測定することで初発胃がんのリスクを予測できることが、世界で初めて前向き研究により証明されました。また、超高リスク集団を同定するためのメチル化レベルを決定することにも成功しました。
これらの研究成果より、以下のことが、直接的、間接的に期待されます。
- 胃がん超高リスクな人に関しては、検査間隔を短くすることで胃がんの早期発見および内視鏡的治療が効率的に可能となり、患者さんのQOL向上が期待されます。
- 今後、胃発がんリスクの低い(胃粘膜萎縮がない、または、閉鎖型胃粘膜萎縮を有する)健康人も対象に含む研究により、検診不要な低リスク集団の同定が可能となる可能性があります。このことにより、多くの方の心配が軽減され、検診費用も削減されると期待されます(図5)。
- 日本以外のピロリ菌による胃がんが多い外国(特に東アジア)でも、DNAメチル化リスク診断による個別化医療が実現できると期待されます。
- 胃以外でも、慢性炎症によりがんが発生する臓器(子宮、肝臓など)でも、DNAメチル化リスク診断により発がんリスクを予測できると考えられます。外国では、子宮頸がんについて実用化されつつあります。
今回の研究で同定に成功した超高リスク群の人たちには検査間隔を短くすることで、
がんが発生したとしても内視鏡治療が可能なうちに発見が可能になると予測される。
将来的には、DNAメチル化異常がほとんどない低リスク群を同定することで、
経過観察の間隔を延ばすことができる人たちも特定することができるようになると期待される。
本研究結果の迅速な社会実装に向けて、シスメックス株式会社と検討を開始しています。
発表論文
雑誌名
Gut
タイトル
Precision risk stratification of primary gastric cancer after eradication of H. pylori by a DNA methylation marker: a multicenter prospective study
著者
Harumi Yamada, Seiichiro Abe, Hadrien Charvat, Takayuki Ando, Masahiro Maeda, Kazunari Murakami, Shiro Oka, Takao Maekita, Mitsushige Sugimoto, Takahisa Furuta, Mitsuru Kaise, Nobutake Yamamichi, Hiroyuki Takamaru, Akiko Sasaki, Ichiro Oda, Sohachi Nanjo, Nobuhiro Suzuki, Toshiro Sugiyama, Masaaki Kodama, Kazuhiro Mizukami, Masanori Ito, Takahiro Kotachi, Taichi Shimazu, Seiichiro Yamamoto, Toshikazu Ushijima
掲載日
2024年4月16日
URL
https://gut.bmj.com/content/early/2025/03/27/gutjnl-2025-335039(外部サイトにリンクします)
研究費
国立研究開発法人日本医療研究開発機構(AMED) 革新的がん医療実用化研究事業
「ピロリ菌除菌後健康人を対象とした世界初エピゲノム発がんリスク診断の実用化(JP23ck0106804, JP20ck0106552, JP17ck0106267, JP15ck0106023)」
用語説明
注1 DNAメチル化異常
DNAメチル化自体は遺伝子のスイッチオン・オフを決めている生理的なメカニズム(エピゲノム制御)です。しかし、そのオン・オフの状態が異常になることがあり、その異常は一度おこると通常はもとには戻らないことが知られています。このDNAメチル化異常によりがん抑制遺伝子(細胞増殖を抑えてがん化を抑制する遺伝子)の機能がなくなることが、がん化に重要であると知られています。
注2 DNAメチル化異常の蓄積
一つの細胞の中にDNAメチル化異常により不活化される遺伝子は沢山あります。また、正常な組織には沢山の正常な細胞があります。これら、沢山の正常な細胞の中のごく少数の遺伝子に異常がおきても、組織全体としては何の変化もおきません。しかし、その小さな異常が蓄積することで、細胞の機能を変化させ、がん化に繋がることになります。がん化に繋がるようなことが起きる前の、少量の蓄積を測定することで、発がんリスクが測定できます。
お問い合わせ先
研究に関するお問い合わせ
星薬科大学
〒142-8501 東京都品川区荏原2-4-41
学長 牛島俊和
Eメール:tushijima142●hoshi.ac.jp
電話番号: 03-5498-5838 (学長室)
国立研究開発法人国立がん研究センター
中央病院 内視鏡科 医長 阿部清一郎
Eメール:seabe●ncc.go.jp
広報窓口
星薬科大学
総務部
電話番号: 03-5498-5978 (総務部)
Eメール: somu●hoshi.ac.jp
国立がん研究センター 企画戦略局 広報企画室
電話番号: 03-3542-2511(代表)
Eメール: ncc-admin●ncc.go.jp
