がん組織のみを用いたがん遺伝子パネル検査の結果から
遺伝性腫瘍に関わる生殖細胞系列バリアントを高精度に予測する
機械学習モデル・ノモグラムを開発、Webアプリとして公開~日本人大規模データベース(C-CAT)を活用し、国際ガイドラインを上回る精度を実現~
2025年12月18日
国立研究開発法人国立がん研究センター
国立大学法人東京大学
地方独立行政法人東京都立病院機構東京都立駒込病院
独立行政法人国立病院機構九州がんセンター
発表のポイント
- 本研究では、がん組織のみを用いて行うがん遺伝子パネル検査(Tumor-onlyパネル)において、検出された遺伝子バリアントが「生まれつきのもの(生殖細胞系列バリアント)」か「がん細胞で起きたもの(体細胞バリアント)」か、高精度に区別する予測モデルを開発しました。
- 国立がん研究センターがんゲノム情報管理センター(C-CAT)に蓄積された日本人約7,000例のデータを用い、腫瘍の細胞含有率などを考慮した新指標(TAR、rVAF)を考案しました。
- 本モデルの予測精度(AUC96–0.97)は、現在標準的に用いられている欧州臨床腫瘍学会(ESMO)の規準(0.85)を大きく上回ることを実証しました。
- 開発した予測モデルは研究者が学術利用のために容易にアクセスできるよう、Webアプリケーションとして無償公開しました。
概要
国立研究開発法人国立がん研究センター研究所 細胞情報学分野 池上 政周主任研究員、高阪 真路分野長、間野 博行特別研究員らは、国立がん研究センター中央病院 遺伝子診療部門 平田 真部門長、東京大学医学部附属病院整形外科・脊椎外科 張 劉哲助教、小林 寛講師、東京都立駒込病院 遺伝子診療科 山口 達郎部長、骨軟部腫瘍科 平井 利英医長、九州がんセンター臨床研究センター腫瘍遺伝学研究室 織田 信弥室長と協力し、がん遺伝子パネル検査注1のデータを用いて、遺伝性腫瘍症候群注2の原因となる「生殖細胞系列バリアント注3(生まれつきの遺伝子の変化)」を高精度に予測する数理モデルおよびAIモデルを開発し、2025年11月にWebアプリケーションとして公開しました( https://www.felis-portal.com/U3Nomogram (外部サイトにリンクします))。
標準治療注4が終了したがん患者さんに、がん細胞がもつ遺伝子バリアントに対応する有効性の高い治療法がないかを探索するため、がん遺伝子パネル検査が年間25,000例に対して実施されています。その約8割で実施されている「がん組織のみ」を用いたがん遺伝子パネル検査(Tumor-onlyパネル)では、見つかった遺伝子バリアントが「がんの原因となった生まれつきのバリアント」なのか、それとも「がん細胞の中で後天的に生じたバリアント(体細胞バリアント)」なのかを区別できない場合があり、真に遺伝学的検査や遺伝カウンセリングを必要とする患者さんを事前に判断することが難しいという課題があります。本研究では、国立がん研究センターがんゲノム情報管理センター(C-CAT)に登録された日本人の大規模ながん遺伝子パネル検査のデータを解析し、腫瘍の純度とバリアントのアレル頻度注5を組み合わせた新しい指標を導入することで、日本人の患者さんに最適化された生殖細胞系列バリアントの予測モデル「U3-Nomogram」を構築しました。このモデルは、既存の欧州臨床腫瘍学会(ESMO)の規準(以下、「ESMO規準」)よりも正確に遺伝性腫瘍の可能性を判定できることが確認されました。
本研究成果は、米国科学雑誌「Clinical Cancer Research」に2025年12月17日付で掲載されました。
背景
がん遺伝子パネル検査(がんゲノムプロファイル検査)は、がん細胞の多数の遺伝子を一度に調べ、検出された遺伝子バリアントに基づいて、患者さん一人ひとりに適した治療薬を探す検査です。この検査により、本来の目的である薬の選択だけでなく、遺伝性乳がん・卵巣がん症候群注6やLynch(リンチ)症候群注7といった遺伝性腫瘍症候群の可能性が偶然見つかること(二次的所見)があります。日本で行われているがん遺伝子パネル検査の約8割は、がん組織のみを解析する「Tumor-onlyパネル」です。この方法では正常細胞(血液など)との比較を行わないため、検出されたバリアントが「生殖細胞系列バリアント」なのか、「体細胞バリアント」なのかを区別できません。そのため、遺伝性腫瘍の確定診断には、別途、血液を用いた確認検査が必要となります。 しかし、全ての患者さんに確認検査を行うことは医療経済的・心理的負担が大きく現実的ではありません。これまではESMO規準などを参考に、確認検査を推奨する対象者を絞り込んでいましたが、日本人データに基づいて策定された規準ではないため、日本人での精度に課題がありました。
研究成果の詳細
研究グループは、C-CATに蓄積されたゲノム元情報に基づき、解析を行うための仮想環境「C-CAT CALICO」を使用し、がん組織と血液の両方を検査することで体細胞バリアントと生殖細胞系列バリアントの区別が可能な検査「NCCオンコパネル」の受検者データから、日本人7,078例の解析を行いました。
1. 日本人特有の傾向と既存規準の限界を解明
解析の結果、日本人のデータにおいて、遺伝性腫瘍に関連する32の遺伝子の病的バリアントのうち、実際に生殖細胞系列バリアントであった割合(Germline conversion rate)は全体の約10%でした。しかし、がんの種類や遺伝子の種類によってこの割合は大きく異なり、既存のESMO規準では見逃しや過剰な検査推奨が生じる可能性があることが分かりました(図1)。
遺伝子ごとの、病的異変が生殖細胞系列変異であった割合
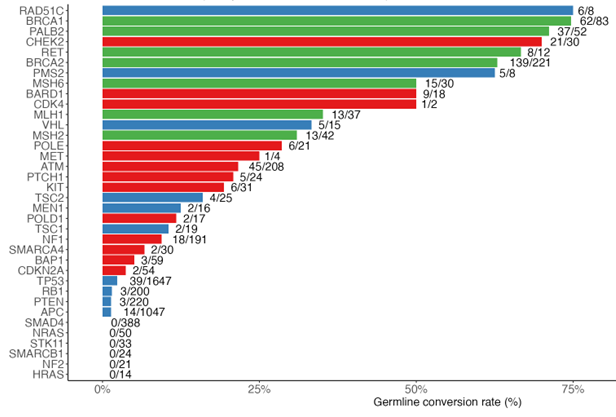 図1:遺伝子ごとに、病的バリアントの検出率とGermline conversion rateが大きく異なっていました。
図1:遺伝子ごとに、病的バリアントの検出率とGermline conversion rateが大きく異なっていました。
2. 新しい予測指標「TAR」と「rVAF」の開発
腫瘍組織に含まれるがん細胞の割合は検体ごとに異なります。研究グループは、この割合を考慮に入れた2つの新しい指標を開発しました。
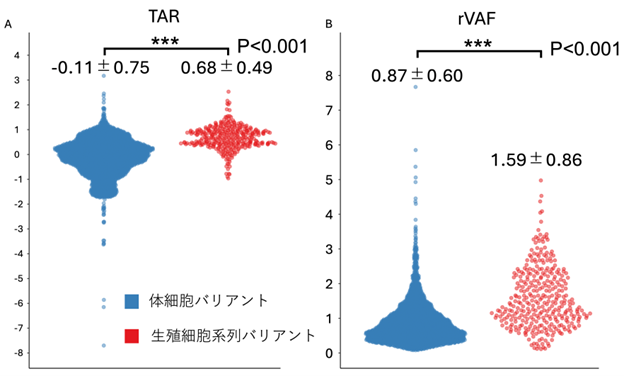
- TAR(Tumor Allele Ratio): 細胞内での正常な遺伝子とバリアントを有する遺伝子の比率を反映した指標
- rVAF(relative Variant Allele Frequency): 腫瘍に含まれるがん細胞の割合を補正して、バリアントの本来の頻度を推定する指標
これらの指標は生殖細胞系列バリアントと体細胞バリアントの区別に有用であることが分かりました(図2)。
3. 高精度な予測モデル(ノモグラム・AI)の構築
上記の新指標に加え、年齢、がん種、バリアントが一般集団で検出される頻度などの情報を組み合わせ、ロジスティック回帰モデル(ノモグラム注8)および機械学習モデル注9(LightGBM, Random Forest)を開発しました(図3A)。 検証の結果、本モデルの生殖細胞系列バリアントの予測精度(ROC曲線注10のAUC注11)は0.96~0.97に達し、ESMO規準(0.85)や国内の既存規準(小杉班規準 0.88)を有意に上回りました(図3B)。また、決定曲線分析(Decision Curve Analysis)によると、ノモグラムを用いて生殖細胞系列の可能性が高いバリアントのみを抽出し確認する追加検査を行うことで、1.6~1.8%の患者さんに臨床的純便益注12があることが示されました(図3C)。
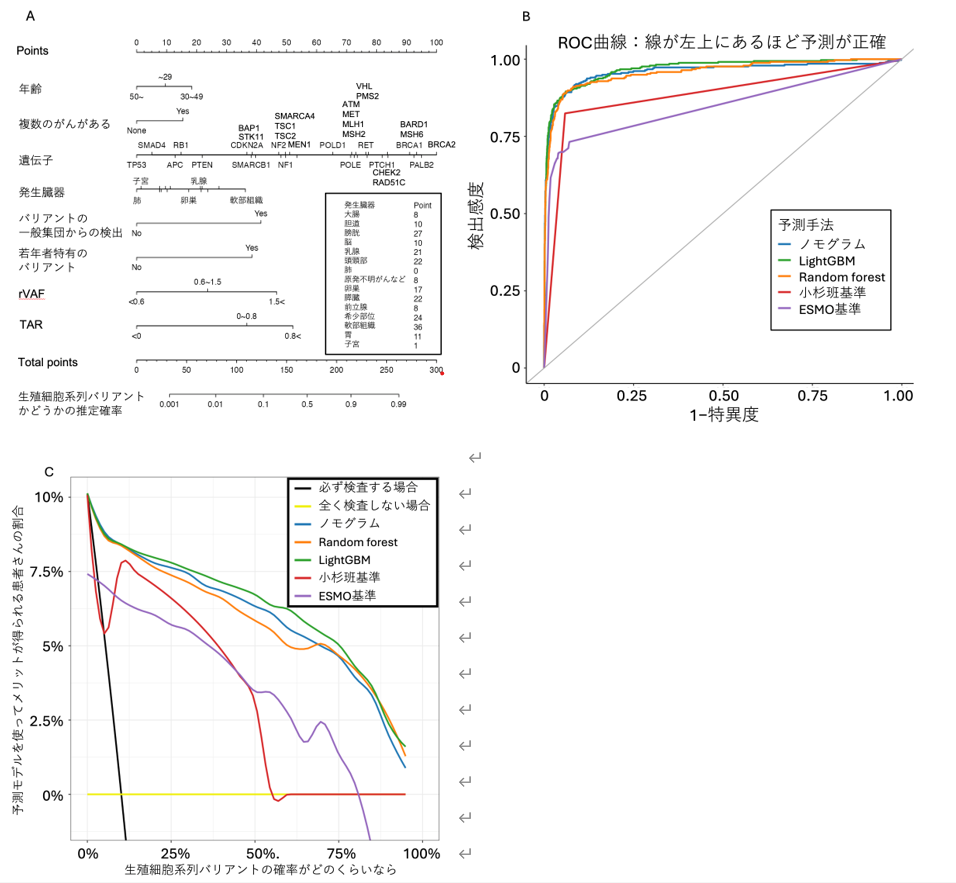
図3:(A) ノモグラムによる生殖細胞系列バリアントの推定。新規指標であるrVAFやTARを含めた様々な要因が判定に寄与していました。各項目のポイントの合計点から生殖細胞系列バリアントかどうかの推定確率が求まります。(B) 新たに開発した予測モデルと既存のESMO規準・小杉班規準の精度比較(ROC曲線)。予測モデルが常に左上に位置しており、高い予測能を示していることが分かりました。(C) 全ての病的バリアントについて必ず確認検査をする場合や全く検査をしない場合と比べて、ESMO規準や小杉班規準を用いた生殖細胞系列バリアントの確認検査対象の選別は患者さんの価値観によらず純便益が得られ有益でした。さらに本研究で開発した予測モデルを用いると、追加で1.2-1.6%の患者さんに純便益をもたらすことがわかりました。
展望
本研究で開発した生殖細胞系列バリアントの予測モデル(ノモグラム・AI)は、Tumor-onlyパネルの結果から、どの患者さんに遺伝学的検査(確認検査)を推奨すべきかについて、より科学的な検討を行うための指標を提供します。 このような予測モデルは、不要な追加検査を減らして患者さんの負担を軽減すると同時に、本当に検査が必要な患者さんを見逃さず、適切な遺伝カウンセリングや予防的措置(リスク低減手術注13やサーベイランス注14)へとつなげるための参考情報として、臨床判断に貢献することが期待されます。
今回、開発した予測モデルは、Webアプリケーション「U3-Nomogram」として無償公開しています。なお、本アプリケーションは研究用途(Research Use Only)として設計されており、研究コミュニティでの検証と学術利用を目的とし、臨床診断・医療判断・遺伝カウンセリングの決定などに用いることはできません。 URL: https://www.felis-portal.com/U3Nomogram (外部サイトにリンクします)
今後、より多くの遺伝子や異なるパネル検査へ対応した予測モデルを開発し、がんゲノム医療の質の向上とプレシジョン・メディシン注15の発展に貢献していきます。
論文情報
雑誌名
Clinical Cancer Research
タイトル
Germline pathogenic variant prediction model for tumor-only sequencing based on Japanese clinicogenomic database
著者
Masachika Ikegami1,2,3,8,#, Liuzhe Zhang4,8, Makoto Hirata5, Tatsuro Yamaguchi6, Shinya Oda7, Shinji Kohsaka2,3, Hiroyuki Mano2,3, Toshihide Hirai1, Hiroshi Kobayashi4
所属
- Department of Musculoskeletal Oncology, Tokyo Metropolitan Cancer and Infectious Diseases Center, Komagome Hospital, Tokyo, Japan.
- Division of Cellular Signaling, National Cancer Center Research Institute, Tokyo, Japan.
- Center for Cancer Genomics and Advanced Therapeutics (C-CAT), National Cancer Center, Tokyo, Japan.
- Department of Orthopaedic Surgery, The University of Tokyo, Tokyo, Japan.
- Department of Genetic Medicine and Services, National Cancer Center Hospital, Tokyo, Japan.
- Department of Clinical Genetics, Tokyo Metropolitan Cancer and Infectious Diseases Center Komagome Hospital, Tokyo, Japan.
- Cancer Genetics Laboratory, Clinical Research Institute, NHO Kyushu Cancer Center, Fukuoka, Japan.
- Equally contributed.
# Corresponding author
DOI
10.1158/1078-0432.CCR-25-2985
掲載日
2025年12月17日
URL
https://aacrjournals.org/clincancerres/article-abstract/doi/10.1158/1078-0432.CCR-25-2985(外部サイトにリンクします)
研究費
- 研究費名(支援先):日本学術振興会
研究事業名:科学研究費助成事業 若手研究 # 22K15571
研究課題名:がん遺伝子パネル検査を受けた全症例におけるシークエンスエラーの実態を解明する
研究代表者名:国立がん研究センター研究所 細胞情報学分野 池上 政周 - 研究費名(支援先):日本学術振興会
研究事業名:科学研究費助成事業 若手研究 # 24K18565
研究課題名:包括的がんゲノムプロファイリング検査を活用した希少がんの最適治療戦略の解明
研究代表者名:国立がん研究センター研究所 細胞情報学分野 池上 政周 - 研究費名(支援先):東京都立駒込病院
研究事業名:都立病院臨床研究 # R04030304
研究課題名:がん遺伝子パネル検査を受けた全症例におけるシークエンスエラーの実態を解明する
研究代表者名:東京都立駒込病院 骨軟部腫瘍科 池上 政周 - 研究費名(支援先):東京都立駒込病院
研究事業名:都立病院臨床研究 # R05040312
研究課題名:軟部肉腫の遺伝子変異に基づく最適治療戦略の探索
研究代表者名:東京都立駒込病院 骨軟部腫瘍科 池上 政周
用語解説
注1 がん遺伝子パネル検査
がん細胞の多数の遺伝子を一度に調べ、遺伝子バリアントを検出する検査です。患者さん一人ひとりのがんの特徴を明らかにし、そのタイプに効果が期待できる治療薬(分子標的薬など)を見つけることを目的としています。
注2 遺伝性腫瘍症候群
生まれつき特定の遺伝子にバリアントがあり、がんを発症しやすい体質のことです。親から子へ受け継がれる可能性があり、若くして発症する、血縁者にがんが多い、複数のがんにかかるといった特徴があります。
注3 バリアント
バリアントとは、DNAの文字列(設計図)の「違い」のことです。細胞のゲノムに含まれるDNAには生まれつき小さな違いがあったり、がん細胞になる過程で新たな変化が加わったりします。その違いの多くは体に影響しませんが、中には病気に関係するものもあり、これを病的バリアントといいます。
注4 標準治療
科学的根拠に基づき、現在利用できる最良の治療法として推奨されているものです。効果と安全性が確認された、多くの患者さんにとって第一選択となるベストな治療法を指します。
注5 アレル頻度
採取した検体のDNA全体の中で、特定の遺伝子バリアントが含まれている割合のことです。数値が50%に近いと生殖細胞系列バリアントの可能性が高いと推測する重要な手がかりになります。
注6 遺伝性乳がん・卵巣がん症候群
相同組換え修復遺伝子(損傷を受けたDNAを修復する遺伝子)に生まれながらの病的バリアントを持つ遺伝性腫瘍症候群で、親から子へと遺伝する確率は性別に関係なく50%です。乳がんや卵巣がんに加えて、膵がんや前立腺がんの発症リスクが高くなります。
注7 Lynch(リンチ)症候群
ミスマッチ修復遺伝子(細胞分裂におけるDNA複製エラーを修復する遺伝子)に生まれながらの病的バリアントを持つ遺伝性腫瘍症候群で、親から子へと遺伝する確率は性別に関係なく50%です。大腸がんや子宮内膜がんなど様々な悪性腫瘍の発症リスクが高くなります。
注8 ノモグラム
ノモグラムは、個々の患者さんの年齢や遺伝子といった情報を図の線に当てはめ、点数を足していくだけで病気のなりやすさや治療の効果などを簡単に予測できる表です。
注9 機械学習モデル
機械学習モデルは、たくさんのデータから「こういう特徴ならこうなりやすい」というパターンを学び、新しい人のデータでも結果を予測する仕組みです。
注10 ROC曲線
ROC曲線(ROC = Receiver Operating Characteristic)は、検査や予測モデルが「病気の人」と「病気でない人」をどれだけ上手に区別できるかを示すグラフです。判定の規準を厳しくしたり緩くしたりしたとき、当たりやすさ(感度)と誤って陽性にする割合(偽陽性率)の関係がどう変わるかを線で表します。線が左上に近いほど、区別の性能が高いと考えます。
注11 AUC
AUC(Area Under the Curve)はROC曲線の下の面積のことで、区別の上手さを1つの数字で表した指標です。値は0.5~1.0の間になり、0.5は「ほぼ当てずっぽう」、1.0に近いほど「生殖細胞系列バリアントと体細胞バリアントを正確に見分けられる」ことを意味します。複数の検査やモデルを比べる際は、AUCの値が大きいほど性能が良いと判断します。
注12 純便益
純便益(net benefit)は、ある検査や予測モデルを使ったときの「得」と「損」をまとめて比べる考え方です。生殖細胞系列バリアントであると確定して適切な治療や予防につながるというメリットから、不要な確認検査やその費用といったデメリットを差し引き、全体として患者さんにどれだけプラスかを数字で示します。例えば100人中何人に実質的な利点があるか、という形で解釈できます。
注13 リスク低減手術
BRCA1遺伝子やBRCA2遺伝子の病的バリアント保持者に対して、がんが発症する前に予防として乳腺や卵巣・卵管を切除する手術。
注14 サーベイランス
定期的に検査や診察を行い、がんの早期発見に努めること。
注15 プレシジョン・メディシン
遺伝子情報や生活環境などの個人差を詳細に分析し、患者さん一人ひとりに最も適した治療や予防を行う医療のことです。がんゲノム医療のように、個人の体質に合わせて精密に個別化された医療を指します。
お問い合わせ先
研究に関するお問い合わせ
国立研究開発法人国立がん研究センター研究所
細胞情報学分野 主任研究員 池上 政周
電話番号:03-3542-2511(代表)
Eメール:maikegam●ncc.go.jp
広報窓口
国立研究開発法人国立がん研究センター
企画戦略局 広報企画室
電話番号:03-3542-2511(代表)
Eメール:ncc-admin●ncc.go.jp
国立大学法人東京大学
医学部附属病院 パブリック・リレーションセンター(担当:渡部、小岩井)
電話番号:03-5800-9188(直通)
E-メール:pr●adm.h.u-tokyo.ac.jp
地方独立行政法人東京都立病院機構東京都立駒込病院
総務課
電話番号: 03-3823-2101(代表)
Eメール: km_soumu●tmhp.jp
独立行政法人国立病院機構九州がんセンター
事務部管理課 管理課長
電話番号:092-541-3231
Eメール:umisaki.kenya.ca●mail.hosp.go.jp
