トップページ > 研究組織一覧 > 分野・独立ユニットグループ > がん治療学研究分野 > 研究成果の概要 > 既存薬の再定義
既存薬の再定義
メインテーマ概要
既存薬の再定義とは
本ページでは、すでに臨床で広く使われている既存薬を、特定のバイオマーカー(ARID1A 欠損)を持つ患者さんに最適化して届ける ── ドラッグ・リポジショニング に関する研究成果を紹介します。
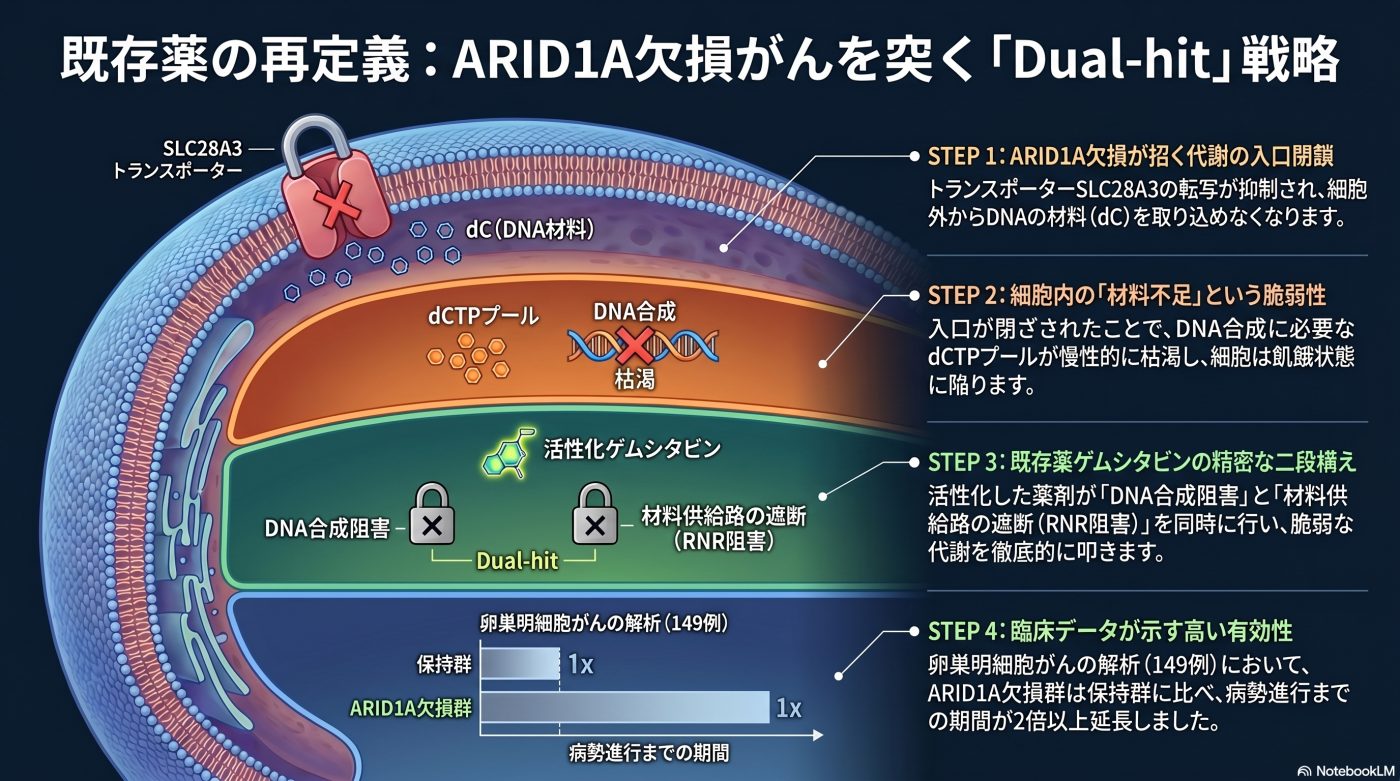
既存薬の再定義 は、研究室の合成致死戦略における 臨床応用への橋渡しを意識したアプローチ です。クロマチンリモデリング因子 ARID1A の機能喪失型変異は、卵巣明細胞がん(OCCC、約 50%)や びまん性胃がん(スキルス胃がんを含む、約 25%)など、標準化学療法が効きにくい難治性がんで高頻度に認められます。私たちは、この遺伝子変異が引き起こす ピリミジン代謝の脆弱性 を、既存薬 ゲムシタビン(核酸代謝阻害剤)が Dual-hit メカニズム で選択的に突くことを解明してきました。
ゲムシタビンは膵臓がん・尿路上皮がん・非小細胞肺がん・卵巣がんなどで広く使われている 既承認の抗がん剤 であり、安全性プロファイル・薬物動態が確立されています。「ARID1A 欠損というバイオマーカーで選別した患者さんに、既存薬を最適化して届ける」という個別化医療(プレシジョン・メディシン)の枠組みを、強固な分子根拠とともに提示することが、本テーマの目的です。
研究室の研究系譜での位置づけ
本テーマは、研究室の合成致死戦略における 臨床応用への橋渡しを意識したアプローチ です。研究室では、ARID1A 欠損がんに対して、本テーマ(ピリミジン代謝 × 既存薬)と並行して、グルタチオン代謝脆弱性(グルタチオン代謝 × 新規創薬)、データ駆動型探索(USP8 を介した合成致死)の 3 つの異なるアプローチ を進めています。
本テーマは、これら 3 つの中で 「すでに承認されている既存薬」を出口として持つ唯一のアプローチ であり、臨床応用への道筋の短さに独自の意義があります。背後の科学的設計思想 ── エピゲノム制御因子の欠損が代謝トランスポーター遺伝子の転写を抑制し、特定の代謝経路にボトルネックを生む ── は、グルタチオン代謝脆弱性 で示された SLC7A11 サイレンシングを介した GSH 合成の綻び と同じ構造を、ピリミジン代謝の文脈で再現 したものです。いずれも、ARID1A 欠損により代謝トランスポーター遺伝子の転写が低下し、特定の代謝基質の供給不足が生じる という共通構造を持ちます。
このページに掲載する研究
- サブテーマ 1: ARID1A 欠損卵巣明細胞がん × ゲムシタビン ── Kuroda et al., Gynecol Oncol, 2019。本テーマの 起点となる発見。6 種類の抗がん剤スクリーニングによる選択的感受性の同定と、149 例の後ろ向き臨床データ による裏付け
- サブテーマ 2: ARID1A 欠損びまん性胃がん × Dual-hit 機構 ── Hirano et al., Mol Cancer Res, 2026。SLC28A3 サイレンシングと Dual-hit メカニズムの解明、腹膜播種マウスモデルでの抗腫瘍効果
サブテーマ 1: ARID1A 欠損卵巣明細胞がん × ゲムシタビン ── 起点となる発見と臨床データによる裏付け
研究要約
|
項目 |
内容 |
|---|---|
|
対象がん |
卵巣明細胞がん(OCCC: Ovarian Clear Cell Carcinoma)── 日本人女性に比較的多く、プラチナ製剤を中心とする標準化学療法に抵抗性を示しやすい組織型。約 50% の症例で ARID1A 欠損 が認められる |
|
遺伝子背景 |
ARID1A 欠損 ── SWI/SNF クロマチンリモデリング複合体(cBAF サブタイプ)の構成因子の機能喪失 |
|
標的・経路 |
既存薬ゲムシタビン(核酸代謝阻害剤)/ピリミジン代謝経路 |
|
作用機序 |
ARID1A 欠損 → ピリミジン代謝の脆弱化 → ゲムシタビンに対する選択的高感受性 → アポトーシス誘導(詳細な Dual-hit 機構はサブテーマ 2 で解明) |
|
創薬上の意義 |
既存薬ゲムシタビンが ARID1A 欠損 OCCC に選択的に有効 であることを発見。149 例の後ろ向き臨床データ で前臨床知見と整合する PFS 延長を示し、ドラッグ・リポジショニングへの道筋を提示 |
|
検証段階 |
6 種類の抗がん剤スクリーニング(in vitro、ARID1A 欠損 vs 保持の比較)/ARID1A の shRNA ノックダウンによる因果検証/国立がん研究センターおよび連携病院の OCCC 患者 149 例の後ろ向き臨床データ解析/多剤耐性後の Partial Response 症例の併記 |
|
創薬段階 |
既承認薬(ゲムシタビン)の ARID1A 欠損患者層への最適化 が研究課題。実用化には大規模な前向き臨床試験が必要 |
|
代表論文 |
このサブテーマの要点
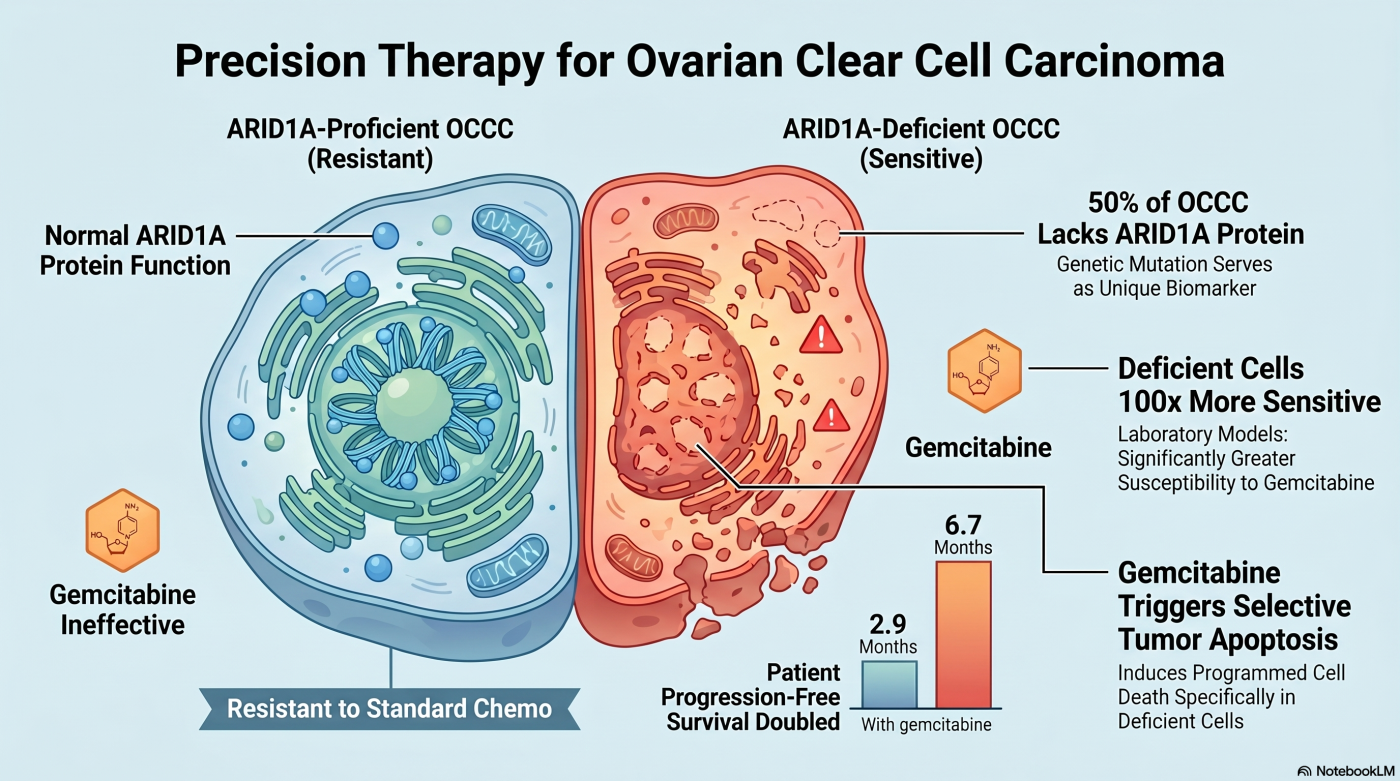
私たちは、独自の卵巣明細胞がん細胞株パネルを用いた 6 種類の殺細胞性抗がん剤の比較スクリーニング により、ARID1A 欠損細胞が、ゲムシタビンに対して選択的に高い感受性を示す ことを報告しました(Kuroda et al., Gynecol Oncol, 2019)。卵巣明細胞がんで使用される他の 5 剤(シスプラチン、カルボプラチン、パクリタキセル、ドキソルビシン、エトポシド)では同様の選択性は認められず、ゲムシタビンのみが ARID1A 欠損型に対して保持型の 10~100 倍の感受性 を示しました。
さらに、国立がん研究センターおよび連携病院の卵巣明細胞がん患者 149 例の後ろ向き臨床データ を解析し、再発後にゲムシタビン単剤治療を受けた患者群において、ARID1A 欠損群が保持群に比べて病勢進行までの期間(PFS)が有意に延長 していることを示しました。これは、前臨床知見(細胞株での感受性差)と実臨床の結果(PFS の差)が同じ方向を向いていることを示す重要な裏付けです。
本研究は、本テーマの 起点 となった成果であり、後のサブテーマ 2 における Dual-hit メカニズムの解明(Hirano et al., Mol Cancer Res, 2026)へとつながりました。
背景
卵巣明細胞がん(OCCC)は、卵巣がんの組織型のうち日本人女性に比較的多いサブタイプであり、プラチナ製剤を中心とする標準化学療法が効きにくい ことが長年の課題でした。再発例では治療選択肢が限られ、新しい治療標的の発見が強く求められてきました。ARID1A は、卵巣明細胞がんの約半数で機能喪失型変異が認められる、最も高頻度のドライバー遺伝子の一つです。
ARID1A は機能喪失型変異であり、「失われた機能を直接補う治療薬」を作ることは原理的にできません。私たちは、この困難を乗り越えるアプローチとして、「失われた遺伝子の代わりに、失われたことで生まれた『代謝の綻び』を突く」 という戦略を選びました。本研究では、その綻びをすでに臨床で広く使われている既存薬で突く ── すなわち ドラッグ・リポジショニング という出口を選んだことが、最大の特徴です。
新薬開発には膨大な時間とコストがかかりますが、すでに承認されている既存薬を、特定のバイオマーカー(ARID1A 欠損)で選別した患者さんに最適化して届ける という道筋であれば、既存の安全性・薬物動態情報を活用できる利点 があります。これが、私たちがドラッグ・リポジショニングに取り組む現実的な理由です。
発見
6 種類の抗がん剤スクリーニングによる選択的感受性の同定
私たちは、卵巣明細胞がんの標準・再発治療で使用される 6 種類の殺細胞性抗がん剤(ゲムシタビン、シスプラチン、カルボプラチン、パクリタキセル、ドキソルビシン、エトポシド)を、ARID1A 欠損型と保持型の細胞株パネルで比較しました。その結果、ゲムシタビンのみが ARID1A 欠損細胞に対して選択的に高い殺細胞効果(ARID1A 保持細胞の 10~100 倍の感受性) を示すことを発見しました。他の 5 剤では同様の選択性は認められませんでした。
ARID1A の有無がゲムシタビン感受性に関与
ARID1A の shRNA ノックダウン により、ARID1A 保持細胞でもゲムシタビン感受性が亢進することを確認しました。これは、ARID1A の有無がゲムシタビン感受性に因果的に関与することを支持する所見 です。また、ARID1A 欠損細胞では、ゲムシタビン投与後に アポトーシスマーカー(cleaved PARP、cleaved caspase-3 等)の上昇が顕著に認められ、選択的な細胞死誘導が成立していることを確認しました。
なお、この時点では「なぜ ARID1A 欠損細胞だけがゲムシタビンに感受性を示すのか」という分子機序は未解明でした。この問いは、後のサブテーマ 2(Hirano et al., Mol Cancer Res, 2026)で深掘りされ、Dual-hit メカニズム として整理されました。
作用機序
サブテーマ 1 の段階では、ARID1A 欠損細胞がゲムシタビンに選択的に高感受性を示す現象は確認されていたものの、その分子機序は未解明でした。「ARID1A 欠損 → ピリミジン代謝の脆弱化 → ゲムシタビン感受性」という枠組みは、後のサブテーマ 2 において、SLC28A3 サイレンシングと Dual-hit メカニズム として詳細に解明されました(詳細は サブテーマ 2「作用機序」 を参照)。
検証
後ろ向き臨床データによる PFS の延長(n = 149)
私たちは、国立がん研究センターおよび連携病院の卵巣明細胞がん患者 149 例の後ろ向き臨床データ を解析しました。解析対象 149 例のうち、再発後にゲムシタビン単剤治療を受けた患者群を対象に比較 し、ARID1A 欠損群は ARID1A 保持群に比べて、治療後の病勢進行までの期間(PFS)が有意に延長 していました。
PFS 中央値: 6.7 ヶ月(ARID1A 欠損群)vs 2.9 ヶ月(ARID1A 保持群)、P = 0.02
これは、後ろ向き解析という研究デザイン上の限界はあるものの、前臨床の知見(細胞株での感受性差)と実臨床の結果(PFS の差)が同じ方向を向いている ことを示す、重要な裏付けデータです。
多剤耐性後の Partial Response 症例(Case Report)
論文中では、術後補助化学療法(パクリタキセル + カルボプラチン)および一次治療(エトポシド + イリノテカン)に抵抗性を示した多剤耐性の患者さんが、ARID1A 欠損を有していたために二次治療として ゲムシタビン を使用したところ、Partial Response(部分奏効) を認めた事例も報告されています。
これは単一症例の生物学的観察であり、群間比較とは性質の異なるデータですが、「ARID1A 欠損というバイオマーカーで選別された患者さんでは、他剤に抵抗性であってもゲムシタビンが奏効し得る」という仮説と整合する所見として、前臨床から臨床への橋渡しを示唆する事例です。
創薬・臨床への展望
本サブテーマの臨床的意義は、149 例の後ろ向き臨床データ によって、前臨床知見と実臨床の結果が整合することを示した点にあります。想定される対象患者層は、ARID1A 欠損卵巣明細胞がんの女性患者さん となります。
ただし、本研究は 後ろ向き解析 であり、その結果を 大規模な前向き臨床試験(プロスペクティブ試験)で検証する ステップが、なお必要です。「すでに使える既承認薬」と「ARID1A 欠損患者さんへの最適化された使い方が確立されている」は別物であり、保険診療として確立された治療法として推奨できる段階ではありません。
私たちは、本研究を起点として、Dual-hit メカニズムの分子機序解明(→ 本ページ「サブテーマ 2」参照)、適応拡大の対象がん種の検討、合理的併用療法の探索 等の方向への展開を進めています。
関連論文
- Kuroda T, Ogiwara H*, Sasaki M, Takahashi K, Yoshida H, Kiyokawa T, Sudo K, Tamura K, Kato T, Okamoto A, Kohno T. Therapeutic preferability of gemcitabine for ARID1A-deficient ovarian clear cell carcinoma. Gynecol Oncol. 2019;155(3):489–498. PubMed → 既存薬ゲムシタビンが、ARID1A 欠損卵巣明細胞がんに対して選択的に高い感受性を示すことを発見した最初の報告。国立がん研究センターおよび連携病院の卵巣明細胞がん患者 149 例の後ろ向き臨床データ で、ARID1A 欠損群が保持群に比べて PFS(中央値 6.7 ヶ月 vs 2.9 ヶ月、P = 0.02)の有意な延長を示した。多剤耐性後の Partial Response 症例(Case Report)も併記。
サブテーマ 2: ARID1A 欠損びまん性胃がん × Dual-hit 機構 ── 分子機序の解明と腹膜播種モデル
研究要約
|
項目 |
内容 |
|---|---|
|
対象がん |
びまん性胃がん(DGC: Diffuse-type Gastric Cancer、スキルス胃がんを含む)── 腹膜播種を伴いやすく、5-FU を含む既存化学療法の効果が十分でない症例も多い、治療選択肢が限られる難治性がん。約 25% の症例で ARID1A 欠損 が認められる |
|
遺伝子背景 |
ARID1A 欠損 ── SWI/SNF クロマチンリモデリング複合体(cBAF サブタイプ)の構成因子の機能喪失(サブテーマ 1 と共通) |
|
標的・経路 |
既存薬ゲムシタビン(核酸代謝阻害剤)/SLC28A3(高親和性ヌクレオシドトランスポーター)/ピリミジン代謝(dCTP プール、de novo 経路、salvage 経路)/RNR(リボヌクレオチド還元酵素) |
|
作用機序 |
ARID1A 欠損 → SLC28A3 サイレンシング → 細胞外 dC 取り込みの低下 → 細胞内 dCTP プールの慢性的枯渇 → ゲムシタビンの Dual-hit(Hit 1: dFdCTP の DNA 取り込みによる chain termination、Hit 2: dFdCDP による RNR 阻害)→ アポトーシス誘導 |
|
創薬上の意義 |
ARID1A 欠損がんにおけるゲムシタビン選択的有効性の 主要な分子メカニズム(Dual-hit) を解明。SLC28A3 サイレンシング が機能的な仲介因子であることを実証し、メカニズム上の論理に基づくドラッグ・リポジショニングの基盤を確立 |
|
検証段階 |
in vitro(メタボローム解析による dCTP プール枯渇の実測、トランスクリプトーム解析、SLC28A3 強制発現実験)/腹膜播種マウスモデル での抗腫瘍効果/ARID1A の shRNA ノックダウン・再構築実験 |
|
創薬段階 |
サブテーマ 1 と共通の 既承認薬ゲムシタビン を使用。前向き臨床試験への橋渡しが今後の課題 |
|
代表論文 |
このサブテーマの要点
私たちは、難治性の びまん性胃がん(DGC)モデルに対象を広げ、統合的オミクス解析(メタボローム解析およびトランスクリプトーム解析)によって、サブテーマ 1 で見出されたゲムシタビン選択的有効性の 主要メカニズム を詳細に解明しました(Hirano et al., Mol Cancer Res, 2026)。
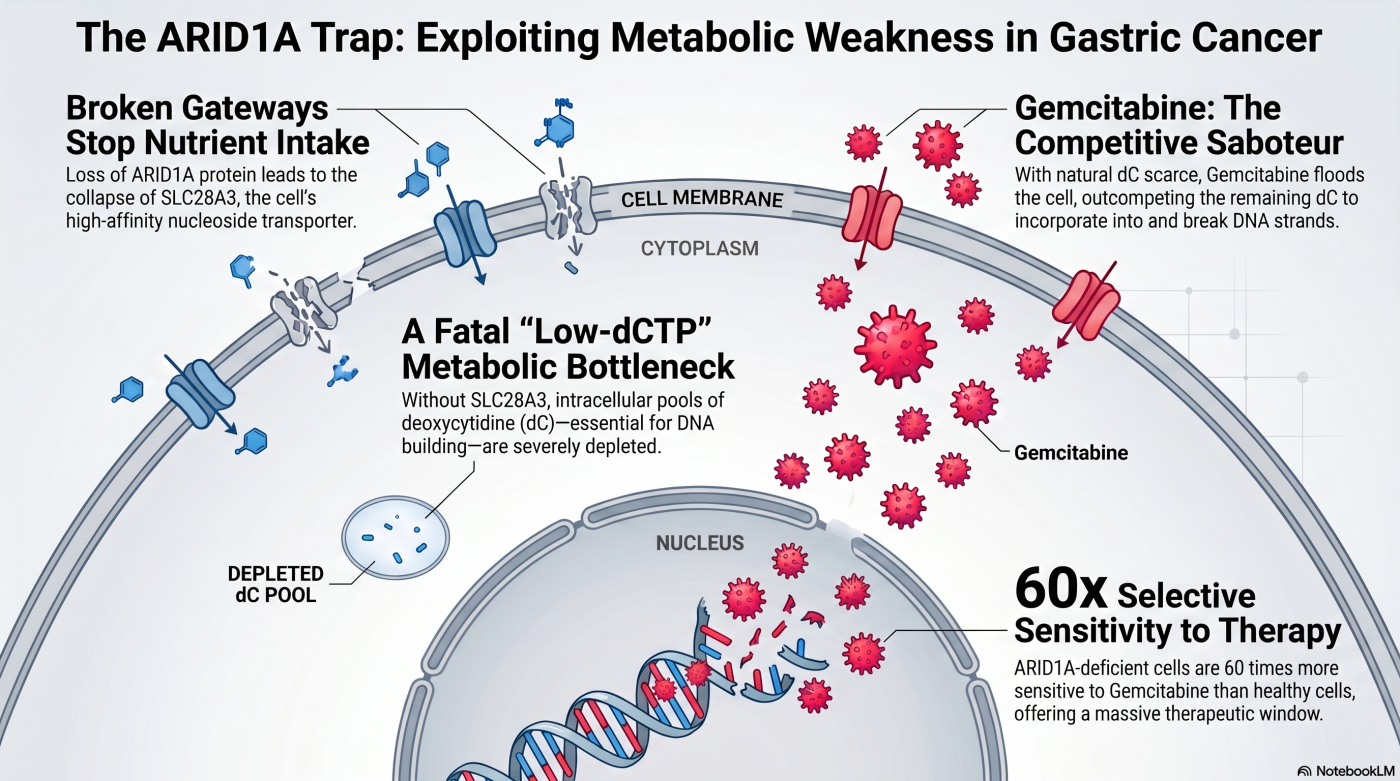
中核となる発見は、ARID1A が欠損したびまん性胃がん細胞では、高親和性ヌクレオシドトランスポーター SLC28A3 の転写がサイレンシングされ、細胞内 dCTP プールが慢性的に枯渇している という機序です。この 「材料不足」の脆弱な代謝環境 に、既存薬ゲムシタビンが Dual-hit(DNA 鎖伸長阻害と RNR 阻害の同時阻害)で付け込み、選択的なアポトーシスを誘導します。
さらに、腹膜播種マウスモデル(びまん性胃がんで臨床医にとって最大の壁となる病態)において、ARID1A 欠損型では ゲムシタビン投与により有意な腫瘍増殖抑制効果が確認されました。本研究により、サブテーマ 1 で発見された現象が メカニズム上の論理 で裏付けられ、メカニズムに基づくドラッグ・リポジショニングの基盤が確立されました。
背景
びまん性胃がん(DGC)は、腹膜播種を伴いやすく、5-FU を含む既存化学療法の効果が十分でない症例も多い、治療選択肢が限られる難治性がん です。スキルス胃がん は、胃壁全体にがんがびまん性に浸潤し、腹腔内に広く転移するため、外科的切除も化学療法も奏効しにくい ことが知られています。ARID1A は、びまん性胃がんの約 4 分の 1 で機能喪失型変異が認められる、頻度の高いドライバー遺伝子の一つです。
サブテーマ 1 で示された ARID1A 欠損 OCCC に対するゲムシタビン選択的有効性は、他の ARID1A 欠損がんにも応用できる普遍的な現象である可能性 を示唆していました。私たちは、対象を OCCC から DGC へ広げると同時に、未解明だった分子メカニズムの解明にも取り組みました。
発見
SLC28A3 サイレンシングによる細胞内 dCTP プールの枯渇
私たちは、ARID1A 欠損 DGC 細胞において、高親和性ヌクレオシドトランスポーター SLC28A3(CNT3、Concentrative Nucleoside Transporter 3)の転写が著しく低下(サイレンシング)していることを トランスクリプトーム解析 で突き止めました。これにより、
- 細胞外からの デオキシシチジン(dC) の取り込みが慢性的に制限される
- DNA 合成の材料である 細胞内 dCTP プール が恒常的に枯渇する(メタボローム解析 で直接実測)
- すなわち、ピリミジン代謝において 「材料不足」のボトルネック状態 が生じる
この機序は、グルタチオン代謝脆弱性(テーマ5)で示された「ARID1A 欠損 → SLC7A11 サイレンシング → システイン供給の綻び」と 同じ構造 が、ピリミジン代謝でも成立していることを意味します。ARID1A は、複数の代謝トランスポーター遺伝子のプロモーター領域に結合し、その転写を維持する役割を共通して担っていることが、研究室の一連の研究から浮かび上がってきています。
作用機序
既存薬ゲムシタビンは、まさにこの脆弱な代謝環境に作用します。
通常、細胞内には天然の基質(dC)が豊富に存在し、ゲムシタビンの細胞内取り込み・リン酸化と競合します。しかし、ARID1A 欠損細胞では dC が枯渇しているため、ゲムシタビンは競合を受けずに細胞内に取り込まれ、効率的に活性化代謝物(dFdCTP/dFdCDP)に変換 されます。活性化されたゲムシタビン代謝物は、以下の 2 経路を同時に攻撃(Dual-hit) します。
Hit 1 ── DNA 合成阻害(chain termination)
枯渇した dCTP の代わりに、dFdCTP(ゲムシタビン三リン酸体)が DNA に取り込まれます。dFdCTP の取り込みは、DNA 鎖伸長を停止させる「マスクされた鎖終結」を引き起こし、DNA 複製を強力に阻害します。
Hit 2 ── RNR 阻害による de novo 経路の遮断
同時に、dFdCDP(ゲムシタビン二リン酸体)が リボヌクレオチド還元酵素(RNR) を阻害します。RNR は de novo 経路で dNDP(特に dCDP)を産生する律速酵素であるため、その阻害は細胞内が自前で dCTP を補充する経路をも遮断します。
救済経路(salvage pathway)の遮断 ── 逃げ場のない状態
通常のがん細胞であれば、Hit 1 が成立しても、Hit 2 で de novo 経路が阻害されても、細胞は 天然の dC を細胞外から取り込む救済経路(salvage pathway) で対応できます。しかし、ARID1A 欠損細胞では SLC28A3 サイレンシングによって救済経路自体が絶たれている ため、dCTP 供給を補う経路が重層的に制限され、アポトーシスが誘導されます。
このメカニズムは、ゲムシタビンが ARID1A 欠損細胞で選択的に有効である理由を、薬剤の作用機序のレベルで合理的に説明する 枠組みとなりました。一方、ARID1A が保たれている細胞では SLC28A3 発現が維持され、救済経路が機能するため、ゲムシタビンの影響は相対的に小さくなります。これが、がん細胞選択性が得られる可能性 の理論的根拠となります。
検証
細胞株モデル(in vitro)でのメカニズム実証
- ARID1A 欠損型のびまん性胃がん細胞株 は、ARID1A 保持型に比べてゲムシタビンに対して高い感受性を示すことを確認
- メタボローム解析 により、ARID1A 欠損細胞での 細胞内 dCTP プールの慢性的な枯渇 を直接実測
- トランスクリプトーム解析 により、SLC28A3 の発現が ARID1A 欠損型で著しく低下 していることを確認
- ARID1A の shRNA ノックダウンおよび再構築実験 により、ARID1A の有無が SLC28A3 発現を制御することを支持する所見を得た
- SLC28A3 の強制発現 を行うと、ARID1A 欠損細胞のゲムシタビン感受性が解除されることを確認し、SLC28A3 が機能的な仲介因子 であることを実証
腹膜播種マウスモデル(in vivo)での抗腫瘍効果
びまん性胃がんで臨床上の最大の課題である 腹膜播種マウスモデル を構築し、ARID1A 欠損型の腹膜播種モデルにおいて、ゲムシタビン投与群は対照群と比較して有意な腫瘍増殖抑制効果 を示しました。ARID1A 保持型のモデルでは、同等の選択性は認められず、本効果が ARID1A 欠損依存的であることが確認されました。本実験条件下では、体重変化や主要臓器の組織病理学的所見において、顕著な毒性は観察されませんでした。
これらの in vitro/in vivo データは、前臨床モデルにおいて Dual-hit メカニズムが機能していることを、独立した複数の実験系で確認した 結果です。
創薬・臨床への展望
本サブテーマは、ARID1A 欠損 DGC に対する 既存薬ゲムシタビンの選択的有効性のメカニズム的根拠 を提供するものです。想定される対象患者層は、ARID1A 欠損びまん性胃がん(スキルス胃がんを含む)の患者さん となります。
ゲムシタビンはすでに膵臓がん・尿路上皮がん・非小細胞肺がん・卵巣がんなどで広く使われている 既承認薬 であり、既承認適応における安全性プロファイル・用法用量の情報が蓄積 されています。「ARID1A 欠損というバイオマーカーで選別した患者さんへの最適化された使い方の確立」は、本サブテーマで提示した分子メカニズムを基盤として、今後の臨床研究の重要な方向性となります。
研究室では、本概念を基盤として、ARID1A 欠損が認められる他のがん種(膵臓がん、子宮体がん、食道がん など)においても SLC28A3 サイレンシングとピリミジン代謝脆弱性が成立するかを検証 し、適応拡大の可能性を評価していく方向を進めています。また、ピリミジン代謝関連分子の阻害剤 や グルタチオン代謝阻害剤 との合理的併用療法の探索、ARID1A 欠損患者層を選別するためのバイオマーカー検査(遺伝子検査または免疫染色)の整備、等の方向への展開を進めています。
関連論文
- Hirano H, Makinoshima H, Ogiwara H*. ARID1A Deficiency in Diffuse-Type Gastric Cancer Promotes a Pyrimidine Metabolic Vulnerability. Mol Cancer Res. 2026. PubMed → ARID1A 欠損びまん性胃がんで、ピリミジントランスポーター SLC28A3 のサイレンシングが細胞内 dCTP プールの枯渇を引き起こすことを解明。既存薬ゲムシタビンが Dual-hit メカニズム で選択的にがん細胞を死滅させることを実証し、腹膜播種マウスモデルでの抗腫瘍効果も示した。
キーターム
本ページ全体で使用する主要用語の解説です。
- 既存薬の再定義(ドラッグ・リポジショニング、Drug Repositioning/Drug Repurposing): 既存の医薬品を、本来の適応とは異なる疾患・患者層に新たに適用する ための研究開発戦略。新薬開発に比べて、既存の安全性・薬物動態情報を活用できる利点がある。本研究では、ゲムシタビンを「ARID1A 欠損」というバイオマーカーで選別した患者層に最適化することを目指す
- ゲムシタビン: シチジン類似体の核酸代謝阻害剤。膵臓がん・尿路上皮がん・非小細胞肺がん・卵巣がんなどで広く使われている既承認の抗がん剤。細胞内に取り込まれた後、dFdCTP として DNA に取り込まれて DNA 合成を阻害し、また dFdCDP として リボヌクレオチド還元酵素(RNR) を阻害して de novo 経路の核酸合成も遮断する
- ARID1A: SWI/SNF クロマチンリモデリング複合体の構成因子。卵巣明細胞がん(約 50%)、びまん性胃がん(約 25%)、子宮体がん(約 20%)等で機能喪失型変異が認められる、主要なドライバー遺伝子
- SLC28A3(CNT3、Concentrative Nucleoside Transporter 3): 細胞外から デオキシシチジン(dC) などの天然ヌクレオシドを細胞内に取り込む 高親和性ヌクレオシドトランスポーター。発現低下は、細胞内 dCTP プール(DNA 合成の材料)の慢性的な枯渇を意味する
- Dual-hit メカニズム: 本研究で解明した、ゲムシタビンによる 2 経路同時阻害 の細胞死誘導機構。Hit 1: 枯渇した dCTP の代わりに DNA に取り込まれて DNA 合成を阻害(chain termination)/Hit 2: RNR を阻害して de novo 経路 での核酸合成も遮断 ── ARID1A 欠損細胞では救済経路(salvage pathway)も遮断されているため、逃げ場のない状態となる
- 救済経路(Salvage pathway): 細胞外から取り込んだ天然のヌクレオシドを再利用して核酸合成の材料を補充する経路。SLC28A3 はこの経路の重要な担い手であり、その発現低下は salvage pathway の遮断を意味する
- リボヌクレオチド還元酵素(RNR): de novo 経路で dNDP(dCDP 等)を産生する律速酵素。ゲムシタビン二リン酸体 dFdCDP の主要な阻害標的の一つ
- バイオマーカー: 治療効果や疾患の状態を予測・評価するための、測定可能な生物学的指標。本研究では ARID1A 欠損 が「ゲムシタビンが効きやすい患者さんを選別する」予測バイオマーカーとして機能する
本ページの研究段階について
本ページで紹介する研究はいずれも、現時点では 前臨床研究および後ろ向き臨床データの段階の成果 です。ゲムシタビン自体は膵臓がん・尿路上皮がん・非小細胞肺がん・卵巣がんなどに対する既承認の抗がん剤ですが、「ARID1A 欠損患者さんに対するゲムシタビン投与」を、保険診療として確立された治療法として推奨できる段階ではありません。サブテーマ 1 で示された PFS の延長は 後ろ向き解析 によるものであり、本知見の臨床応用には、大規模な前向き臨床試験(プロスペクティブ試験) による検証が必要です。
関連ハイライト・ページ
- グルタチオン代謝脆弱性 ── ARID1A 欠損がんに対するもう一つの代謝アプローチ。SLC7A11 サイレンシング → GSH 合成の綻び を突く戦略。本ページの「SLC28A3 サイレンシング → ピリミジン代謝の綻び」と 同じ構造 を共有する姉妹研究
- データ駆動型探索 ── ARID1A 欠損卵巣明細胞がんに対するもう一つの治療標的「USP8 を介した合成致死」。同じ対象患者層に対する並行研究系譜
- 従来型合成致死 ── 1 対 1 対応型 の合成致死戦略。研究室のパラログ合成致死研究の起点
- パラログ同時阻害法 ── 1 対 2 対応型 の合成致死戦略。新規化合物の創出による創薬出口
- 次世代型合成致死 ── 2 対 n 対応型 への概念拡張
- 研究ハイライト(親) ── 6 つの研究テーマの俯瞰
- 研究プロジェクト ── 対象がん種別の研究プロジェクト(Project A-2: 卵巣明細胞がん、Project B-2: びまん性胃がん を含む)
- 論文業績 ── 全論文・総説・受賞歴
最終更新日: 2026-05-15

