トップページ > 研究組織一覧 > 分野・独立ユニットグループ > がん治療学研究分野 > 研究成果の概要 > データ駆動型探索
データ駆動型探索
メインテーマ概要
データ駆動型探索とは
本ページでは、公共のがん細胞株データベース(DepMap など)を独自視点で再解析し、独自に整備した希少がん細胞株パネルでの検証と統合することで、希少がん・難治がんに対する合成致死標的を抽出する 研究成果を紹介します。
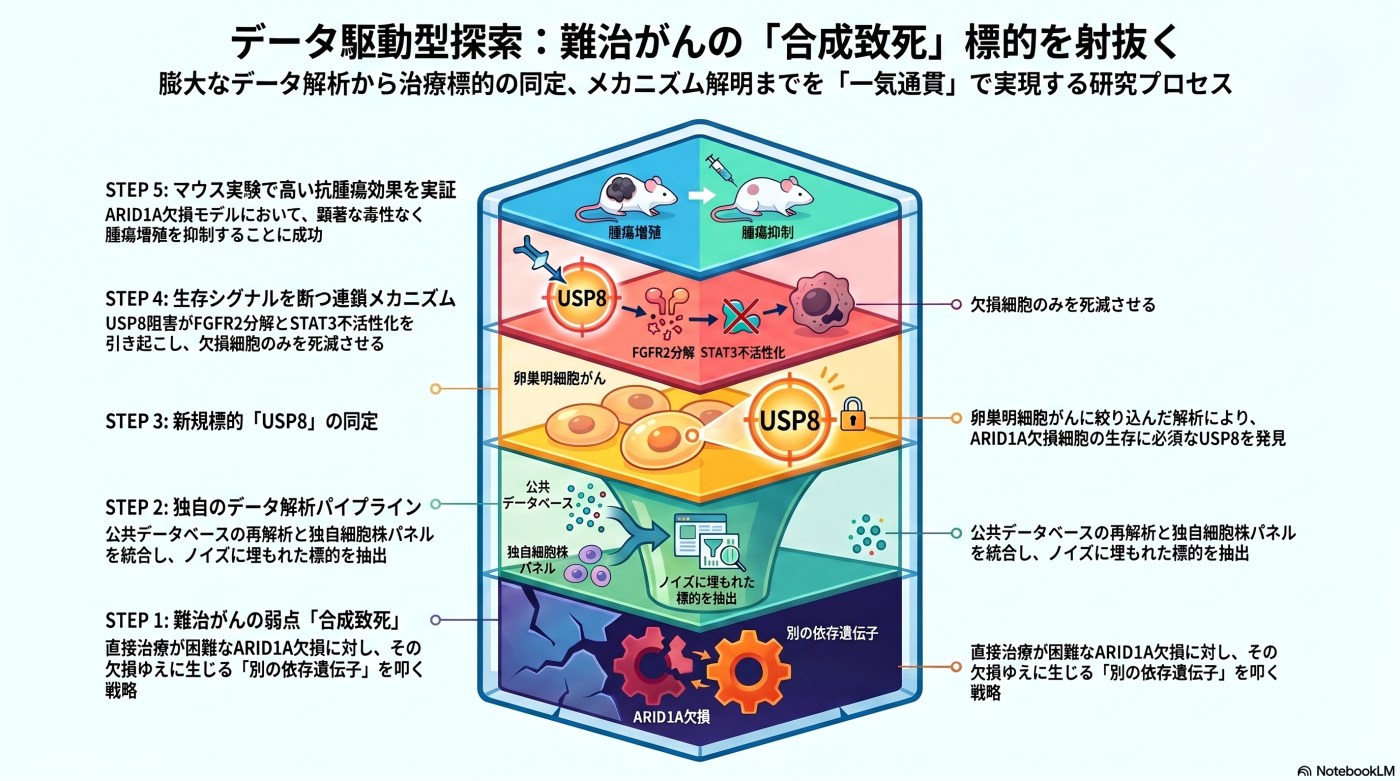
データ駆動型探索 は、研究室が確立した独自アプローチの一つです。膨大な公共データから治療標的の候補を計算機的に予測し、独自細胞株パネルでの実験的検証、そしてメカニズムの完全解明までを 一気通貫 で実施することを特徴とします。
私たちの解析パイプラインには、以下の 3 つの独自視点 が組み込まれています。
- がん種を絞り込んだ再解析(pan-cancer ではなく context-specific 解析)
- 独自細胞株パネルとの統合解析(DepMap に未収載の希少がん細胞株を補完)
- 機能補完を考慮した経路レベルでの解釈(単一遺伝子の依存性だけでなく、同一経路・パラログ・代償経路を含めて候補を評価)
これらの視点により、公共データの網羅性と独自細胞株パネルの疾患特異性を組み合わせ、希少がん・難治がんに固有の依存性を抽出します。
研究室の研究系譜での位置づけ
本テーマは、研究室の研究系譜において 2025 年に主要な研究成果として結実した、新しい主軸 の一つです。一方で、その基盤は 2019 年以降に整備してきた 独自細胞株パネル(グルタチオン代謝脆弱性 研究で活用)と、SWI/SNF 欠損がんに関する生物学的知見 の蓄積にあります。本テーマは、研究室の他の主軸(パラログ同時阻害法・グルタチオン代謝脆弱性・既存薬の再定義)と並行する 横断的な探索エンジン として機能しています。
このページに掲載する研究
- サブテーマ 1: ARID1A 欠損卵巣明細胞がん × USP8 ── Saito et al., NPJ Precis Oncol, 2025。データ駆動型探索の 代表的成果。標的同定から作用機序の解析、前臨床有効性実証まで一気通貫で達成
- (今後)サブテーマ 2 以降: 別の対象がん種・別の標的に対するデータ駆動型探索の研究成果を、論文公開に応じて順次追加予定
サブテーマ 1: ARID1A 欠損卵巣明細胞がん × USP8 ── データ駆動型探索の代表的成果
研究要約
|
項目 |
内容 |
|---|---|
|
対象がん |
卵巣明細胞がん(OCCC: Ovarian Clear Cell Carcinoma)── 日本人女性に特に多く、標準化学療法に抵抗性を示しやすい組織型。約 50% の症例で ARID1A 欠損 が認められる |
|
遺伝子背景 |
ARID1A 欠損 ── SWI/SNF クロマチンリモデリング複合体の構成因子の機能喪失 |
|
標的・経路 |
USP8(Ubiquitin Specific Peptidase 8、脱ユビキチン化酵素)/FGFR2-STAT3 シグナル経路(FGFR2 タンパク質の安定性制御を介する受容体型チロシンキナーゼシグナル) |
|
作用機序 |
USP8 阻害 → FGFR2 のユビキチン化亢進 → FGFR2 の分解 → STAT3 リン酸化の低下 → ARID1A 欠損細胞のアポトーシス誘導 |
|
創薬上の意義 |
データ駆動型探索(DepMap 再解析 + 独自細胞株パネル統合)により、ARID1A 欠損 OCCC に対する新規合成致死標的を 世界に先駆けて同定。標的同定から主要メカニズムの解明・前臨床有効性実証までを一気通貫で達成 |
|
検証段階 |
DepMap データ再解析(がん種絞り込み)/独自細胞株パネルでの CRISPR/Cas9 スクリーニング(MAGeCK 解析)/in vitro(ARID1A 欠損 vs 保持での選択的応答)/in vivo(マウス xenograft モデルでの腫瘍増殖抑制)/ARID1A 再発現による依存性解除実験 |
|
創薬段階 |
研究用化合物(DUB-IN-3 ほか)を用いた概念実証段階/USP8 選択的阻害剤の創薬開発は今後の展開 |
|
代表論文 |
このサブテーマの要点
私たちは、データ駆動型探索パイプラインを ARID1A 欠損卵巣明細胞がん(OCCC)に適用し、脱ユビキチン化酵素 USP8 を新規合成致死標的として同定しました(Saito et al., NPJ Precis Oncol, 2025)。
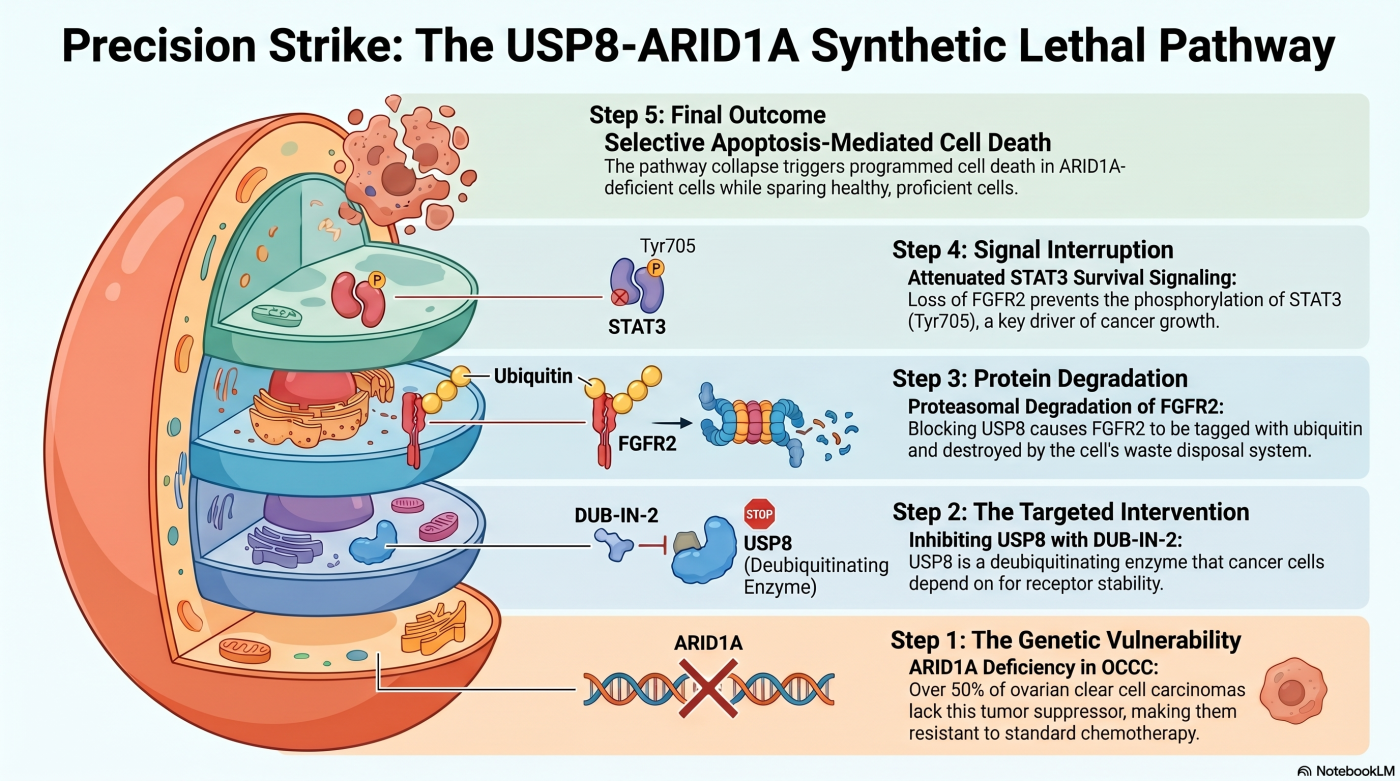
USP8 は、線維芽細胞増殖因子受容体 2(FGFR2)のユビキチン化を制御し、その安定性を保つ役割を担っています。ARID1A 欠損 OCCC 細胞は、FGFR2 を起点とする STAT3 シグナル経路 に強く依存して生存しており、USP8 阻害により FGFR2 が分解されると、STAT3 シグナルが減弱し、ARID1A 欠損細胞でアポトーシスが強く誘導されます。
本研究の特徴は、標的同定(USP8)から作用機序の解析(FGFR2 分解 → STAT3 不活性化 → 細胞死)、前臨床有効性の実証までを、同じ研究室の中で一気通貫で実施した 点にあります。データ駆動型探索が「予測して終わり」ではなく、創薬につながる科学的基盤として機能することを示した代表的成果です。
背景
卵巣明細胞がん(OCCC)は、卵巣がんの組織型のうち、日本人女性に特に多い ことが知られているサブタイプです。日本では卵巣がん全体の約 25%、欧米では約 5~10% を占めるとされ、地域的な発症頻度の差が大きいがんです。
このがんは、プラチナ製剤やタキサン製剤を中心とする標準化学療法に対して抵抗性を示しやすい ことが、長年にわたる臨床上の大きな課題でした。再発時の有効な分子標的薬も限られており、「日本人女性に多いにもかかわらず、治療選択肢が限られている」という、深刻なアンメットメディカルニーズを抱えた疾患です。
その遺伝子学的特徴として、ARID1A 遺伝子の機能喪失型変異 が約 50% の症例で認められます。ARID1A は、SWI/SNF クロマチンリモデリング複合体の構成因子の一つで、遺伝子発現を制御する重要な役割を担っています。しかし、ARID1A は機能喪失型変異であるため、「失われた機能を直接補う治療薬」を作ることは原理的にできません。
そこで私たちが着目したのが、合成致死戦略です ── ARID1A が欠損したことで、がん細胞だけが特異的に依存するようになる「もう一つの遺伝子」を見つけ出し、そこを治療標的とする ── という発想です。問題は、その「もう一つの遺伝子」をどう見つけるかでした。
発見
Step 1: がん種を絞り込んだ DepMap 再解析
DepMap には、約 1,100 種類のがん細胞株における全遺伝子の生存必須性データが収録されています。一般的な解析では、すべてのがん細胞株を一括で扱う pan-cancer 解析 が行われますが、この方法では がん種特有の脆弱性が「ノイズに埋もれて」見えなくなる という限界があります。
私たちは、「卵巣がん細胞株のみ」「肺がん細胞株のみ」「肉腫細胞株のみ」といった組織型別の絞り込み解析(context-specific re-analysis)を、解析パイプラインの最初のステップに据えました。これにより、組織型ごとに異なるエピゲノム背景・代謝環境の中で、ARID1A 欠損が引き起こす依存性の文脈差を捉えることができます。
Step 2: ARID1A 欠損 vs 保持での比較解析
絞り込んだがん種内で、ARID1A が欠損しているがん細胞群 と ARID1A が保たれているがん細胞群 を比較し、欠損群でのみ Dependency Score が顕著に低い(依存性が強い)遺伝子を抽出します。この比較解析の結果、卵巣がん細胞株に絞った解析で、USP8 が ARID1A 欠損群でのみ強い依存性を示す遺伝子としてトップ層に浮上 しました。この所見は pan-cancer 解析では検出できなかったもので、組織型を絞り込んだ独自視点の有効性を示しています。
Step 3: 独自細胞株パネルでの直交検証
DepMap のがん細胞株パネルは、希少がん・日本人特有のがんを十分にはカバーしていません。そこで私たちは、独自に整備した ARID1A 欠損型卵巣明細胞がん細胞株パネル を用いて、CRISPR/Cas9 ノックアウトスクリーニングによる 直交検証(orthogonal validation)を実施しました。スクリーニングデータの解析には MAGeCK(Model-based Analysis of Genome-wide CRISPR-Cas9 Knockout)アルゴリズムを用い、独自パネル由来の細胞株でも USP8 の依存性が再現されることを確認しました。
公共データ(DepMap)だけでは希少がん細胞株のカバー不足が課題となり、独自データだけでは統計的検出力が不足します。両者を統合することで、希少がん・難治がんに対する治療標的を高い信頼性で抽出できる ── これが、私たちのデータ駆動型探索の独自性の核心です。
作用機序
USP8 阻害が ARID1A 欠損細胞を選択的に死滅させる分子機構は、以下の連続的な現象として明らかになりました。
USP8 ↔ FGFR2 ── 受容体型チロシンキナーゼの安定性制御
通常の細胞において、USP8 は FGFR2(線維芽細胞増殖因子受容体 2)に結合したユビキチン鎖を除去することで、FGFR2 が分解経路に送られるのを防いでいます。すなわち、USP8 は FGFR2 の「分解からの保護役」 として機能しています。
USP8 を阻害すると、FGFR2 のユビキチン化が亢進し、FGFR2 が分解経路に乗ることで急速に細胞内から消失します。この現象自体は ARID1A 欠損 vs 保持を問わず観察されるものの、その下流の影響に決定的な違い がありました。
ARID1A 欠損細胞は FGFR2-STAT3 シグナルへの依存度が高い
ARID1A 欠損卵巣明細胞がん細胞では、生存・増殖シグナルの維持を FGFR2 経由のシグナル伝達 に強く依存していました。具体的には、FGFR2 の下流シグナルである STAT3 経路の活性 が、ARID1A 欠損細胞の生存に重要な役割を担っていることが、複数の独立した実験系で確認されました。
USP8 阻害により FGFR2 が分解されると、ARID1A 欠損細胞では STAT3 のリン酸化(活性化マーカー)が顕著に低下 し、これに連動して アポトーシス(細胞死) が誘導されました。一方、ARID1A が保たれている細胞では、FGFR2 が分解されても代替の生存シグナル経路によって補完され、細胞死には至りませんでした。
ARID1A 欠損は、エピゲノム制御を介して FGFR2-STAT3 軸への代償的依存 という生存戦略を細胞に強います。USP8 阻害は、この生存戦略の根を絶つ操作として機能します。ARID1A 欠損そのものを薬理学的に回復させることは困難ですが、その代償として生じる依存性は治療標的になり得ます ── これが、本研究で明らかになった合成致死性の生物学的本質です。
検証
細胞株モデル(in vitro)
卵巣明細胞がん細胞株パネル(ARID1A 欠損型 / ARID1A 保持型)に対して、USP8 阻害(siRNA ノックダウンおよび薬理学的阻害)を実施した結果、ARID1A 欠損型細胞は ARID1A 保持型細胞に比べて顕著に高い感受性 を示しました。USP8 阻害後の FGFR2 タンパク質量の急速な低下、STAT3 リン酸化の有意な低下、アポトーシスマーカー(cleaved caspase-3 等)の上昇 を、複数の独立した実験系で確認しています。
さらに、ARID1A の 再発現実験(ARID1A 欠損細胞に ARID1A を強制発現させる実験)により、USP8 阻害感受性が解除されることが確認されました。これは、ARID1A 欠損と USP8 依存性の因果的関連を支持する重要な所見 です。
マウス xenograft モデル(in vivo)
ARID1A 欠損卵巣明細胞がん細胞株を用いたマウス異種移植モデルにおいて、USP8 阻害剤投与群は対照群に比べて 有意な腫瘍増殖抑制効果 を示しました。ARID1A 保持型細胞由来の異種移植モデルでは、同等の用量での USP8 阻害剤投与でも顕著な抗腫瘍効果は観察されず、in vivo においても ARID1A 欠損依存的な治療効果 が再現されました。本実験条件下では、体重変化や主要臓器の組織病理学的所見において、顕著な毒性は観察されませんでした。
創薬・臨床への展望
本研究は、ARID1A 欠損卵巣明細胞がんに対する新規治療標的化 の科学的基盤を提供するものです。想定される対象患者層は、ARID1A 欠損卵巣明細胞がんの女性患者さん となります。
ARID1A 欠損 という明確な遺伝子バイオマーカーに基づき、「効く可能性が高い患者さんをあらかじめ選別し、USP8 を標的とする治療法の開発につなげる」 ── これが、本研究が目指す個別化医療(プレシジョン・メディシン)の枠組みです。卵巣明細胞がん(ARID1A 欠損 約 50%)は、明確なバイオマーカーで選別可能であり、個別化医療に直接乗せやすい対象です。
加えて、ARID1A 欠損は びまん性胃がん(約 25%)、子宮体がん(約 20%)など、卵巣以外のがんでも一定頻度で見られるため、本研究の射程は OCCC を超えて広がる可能性があります。
創薬モダリティに関しては、本研究では既知の研究用化合物(DUB-IN-3 等)を用いた 概念実証 を行いました。USP8 選択的阻害剤の創薬開発 は、論文公開範囲では研究レベルにあり、今後の課題となります。
研究室では、本概念を基盤として、ARID1A 欠損が認められる他がん種(びまん性胃がん、子宮体がんなど)でも同様の依存性が成立するかを検証し、適応拡大の可能性を評価していく 方向を進めています。また、データ駆動型探索の手法面では、公共データ、独自スクリーニング、マルチオミクスを統合した予測モデルの高度化 に取り組み、他の主軸(パラログ同時阻害法・グルタチオン代謝脆弱性・既存薬の再定義)との横断的な連携を進めています。
関連論文
- Saito R, Fukushima M, Sasaki M, Okamoto A, Ogiwara H*. Targeting USP8 Causes Synthetic Lethality through Degradation of FGFR2 in ARID1A-Deficient Ovarian Clear Cell Carcinoma. NPJ Precis Oncol. 2025;9(1):69. PubMed → ARID1A 欠損卵巣明細胞がんに対するデータ駆動型の合成致死標的として USP8 を同定し、USP8 阻害が FGFR2 の分解を介して選択的細胞死を誘導することを実証。データ駆動型探索の代表的成果。
関連プレスリリース
- 関連する研究室のプレスリリースとして、ARID1A 欠損がんにおけるグルタチオン代謝脆弱性に関する 2019 年 1 月 25 日の発表(グルタチオン代謝脆弱性 関連)があります。
キーターム
本ページ全体で使用する主要用語の解説です。
- データ駆動型探索: 公共のがん細胞株データベース(DepMap など)を独自視点で再解析し、独自に整備した希少がん細胞株パネルでの実験的検証と統合することで、治療標的を抽出する研究室の独自アプローチ
- DepMap(Cancer Dependency Map): 米国 Broad Institute が構築・公開している、約 1,100 種類のがん細胞株を対象とした全遺伝子の生存必須性データベース。CRISPR/Cas9 ノックアウトスクリーニング(Chronos スコア)と RNAi スクリーニング(DEMETER2 スコア)の二つのデータセットを提供している
- Dependency Score: DepMap で各遺伝子の生存必須性を表す指標。スコアが 0 付近は影響なし、マイナスほど生存必須性が強く、−1 付近は「common essential(多くの細胞株で必須となる遺伝子)」を意味する。特定のがん細胞群でのみ低スコアを示す遺伝子 こそが、コンテキスト依存的な合成致死標的の候補となる
- MAGeCK(Model-based Analysis of Genome-wide CRISPR-Cas9 Knockout): CRISPR/Cas9 ノックアウトスクリーニングデータから、統計的に有意な依存性遺伝子を抽出するアルゴリズム
- 直交検証(Orthogonal validation): ある手法・データソースで得られた結果を、独立した別の手法・データソースで確認する検証手法。本研究では、DepMap での予測を独自細胞株パネルでの CRISPR スクリーニングで検証
- ARID1A: SWI/SNF クロマチンリモデリング複合体の構成因子。OCCC(約 50%)、びまん性胃がん(約 25%)、子宮体がん(約 20%)等で機能喪失型変異が認められる、主要な発がん関連遺伝子
- USP8(Ubiquitin Specific Peptidase 8): 脱ユビキチン化酵素(DUB: Deubiquitinating enzyme)の一つ。標的タンパク質に結合したユビキチン鎖を取り除き、複数の受容体型チロシンキナーゼ(FGFR2、EGFR、c-Met 等)の安定性を制御する。ヒトには DUB が約 100 種類存在する
- FGFR2(Fibroblast Growth Factor Receptor 2): 線維芽細胞増殖因子受容体 2。受容体型チロシンキナーゼの一つで、複数のがん種で生存・増殖シグナルの中核を担う
本ページの研究段階について
本ページで紹介する研究は、現時点では 基礎研究・前臨床研究段階の成果 です。USP8 を標的とする治療薬は、現在臨床で使用可能な治療法ではありません。実用化には、阻害剤の創薬開発、安全性・薬物動態評価、臨床試験など、複数の段階が必要となります。
関連ハイライト・ページ
- パラログ同時阻害法 ── 1 対 2 対応型 の合成致死戦略。データ駆動型探索の方法論を、パラログペアの同時依存性スクリーニングへ拡張した研究系譜
- 従来型合成致死 ── 1 対 1 対応型 の合成致死戦略。研究室のパラログ合成致死研究の起点
- 次世代型合成致死 ── 2 対 n 対応型 への概念拡張。データ駆動型探索の手法(CRISPR スクリーニング、統合マルチオミクス解析)が本テーマでも活用されている
- グルタチオン代謝脆弱性 ── ARID1A 欠損がんに対する代謝脆弱性アプローチ。本研究と「ARID1A 欠損卵巣明細胞がんを共通の対象がん種とする」並行研究系譜
- 既存薬の再定義 ── ARID1A 欠損卵巣明細胞がんに対するゲムシタビンの選択的有効性。本研究と並行する研究系譜
- 研究ハイライト(親) ── 6 つの研究テーマの俯瞰
- 研究プロジェクト ── 対象がん種別の研究プロジェクト
- 論文業績 ── 全論文・総説・受賞歴
最終更新日: 2026-05-16

