トップページ > 研究組織一覧 > 分野・独立ユニットグループ > がん治療学研究分野 > 研究成果の概要 > パラログ同時阻害法
パラログ同時阻害法
メインテーマ概要
パラログ同時阻害法とは
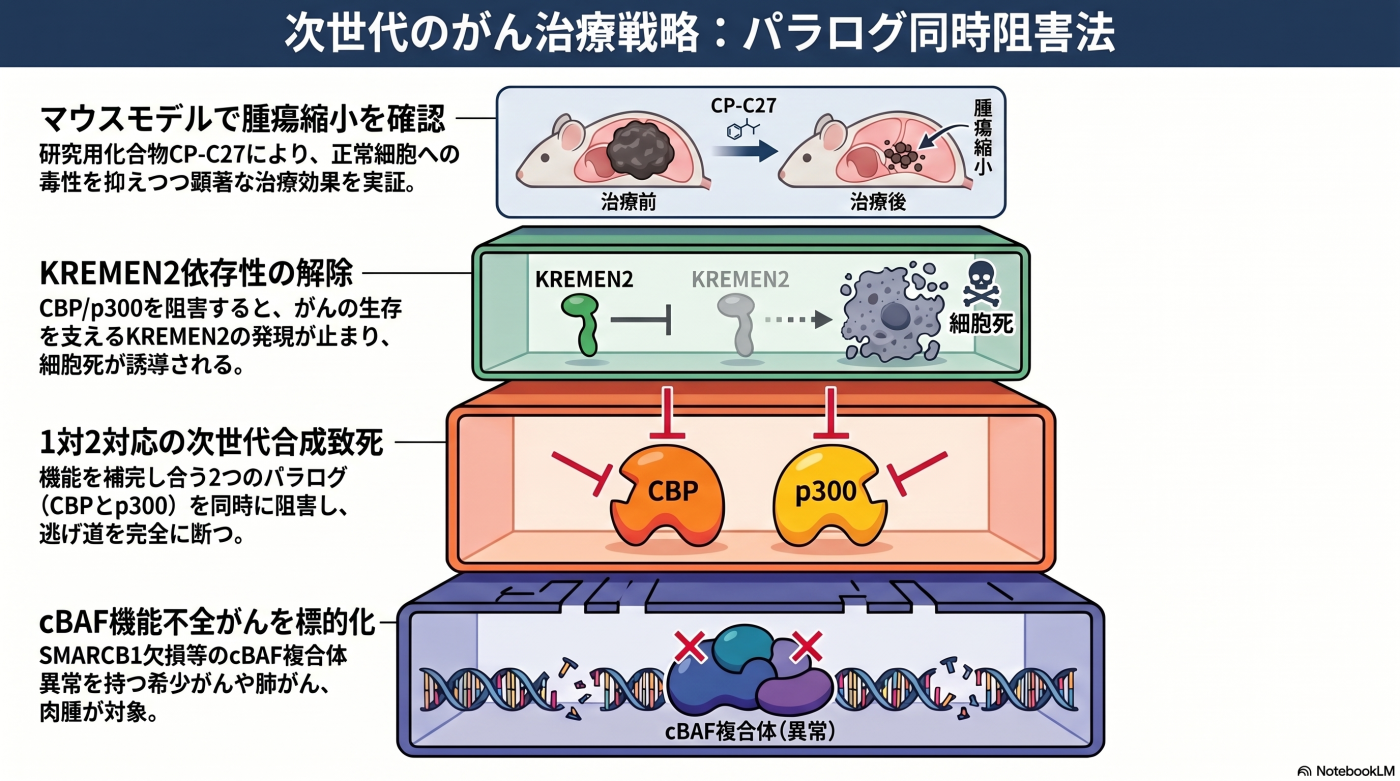
パラログ同時阻害法 は、私たちが提唱した 1 対 2 対応型 の合成致死戦略です。がん細胞で生じた 1 つの遺伝子異常 に対して、機能を補い合う 2 つのパラログ標的を同時に阻害 することで、正常細胞への影響を抑えながら、がん細胞を選択的に死滅させることを目指します。
パラログ(類似遺伝子)は互いの機能を補い合う 冗長性(redundancy) を持つため、片方のみの阻害では十分な治療効果が得られにくいことが、従来型の合成致死探索(1 対 1 対応型)における大きな壁となってきました。パラログ同時阻害法は、この冗長性を 設計段階から考慮し、補完経路を断ち切る ことで、これまで治療標的化が困難とされてきた がん抑制遺伝子の機能喪失型変異がん に対して、新たな道を拓くものです。
本テーマは、従来型合成致死(1 対 1 対応型)を概念的に拡張した 次世代型合成致死 の代表例 に該当します。
研究室の研究系譜での位置づけ
本テーマは、研究室が 2013 年 Cancer Res(BRG1/BRM)・2016 年 Cancer Discov(CBP/p300 addiction)で築いてきた 1 対 1 対応型のパラログ間合成致死(従来型合成致死)を、1 対 2 対応型へ拡張した中核的成果 です。2024 年 Nat Commun で SMARCB1 欠損がんに対する CBP/p300 同時阻害を報告し、その後、cBAF 欠損がんへの適応拡大、さらに 2 対 n 対応型 の 次世代型合成致死 へと展開しています。
このページに掲載する研究
- サブテーマ 1: SMARCB1 欠損希少がん × CBP/p300 同時阻害(Sasaki et al., Nat Commun, 2024)── パラログ同時阻害法の 概念確立
- サブテーマ 2: cBAF 欠損がんへの適応拡大(Sasaki et al., Cancer Res Commun, 2025)── 概念の 対象がん横断的な適応拡大
- (今後)サブテーマ 3 以降: 別のパラログペアでの 1 対 2 対応型研究を、論文公開に応じて順次追加予定
サブテーマ 1: SMARCB1 欠損希少がん × CBP/p300 同時阻害 ── パラログ同時阻害法の概念確立
研究要約
|
項目 |
内容 |
|---|---|
|
対象がん |
SMARCB1 欠損: 悪性ラブドイド腫瘍(小児発症の希少がん)、類上皮肉腫(若年成人~成人発症の希少肉腫) |
|
遺伝子背景 |
SMARCB1 欠損 ── SWI/SNF クロマチンリモデリング複合体(cBAF サブタイプ)の必須サブユニットの機能喪失 |
|
標的・経路 |
CBP(CREBBP)/p300(EP300)パラログペア/KREMEN2 脱抑制経路(H3K27 アセチル化を介する転写制御) |
|
作用機序 |
CBP/p300 同時阻害 → KREMEN2 プロモーターの H3K27ac 消失 → KREMEN2 転写停止 → KREMEN1 解放 → アポトーシス誘導 |
|
創薬上の意義 |
1 対 2 対応型(3 因子間)のパラログ同時阻害戦略を世界に先駆けて確立。これまで治療標的化が困難であったがん抑制遺伝子(SMARCB1)の機能喪失型変異がんに対する、新規治療標的化アプローチ |
|
検証段階 |
in vitro(細胞株での選択的細胞死)/in vivo(マウス移植モデルでの腫瘍増殖抑制・腫瘍縮小)/メカニズム解析(KREMEN2 脱抑制経路の生体内検証) |
|
創薬段階 |
研究用化合物 CP-C27(Sasaki et al., Nat Commun 2024 で公開済み)/製薬企業との共同創薬開発(詳細は知財・契約上の制約により非開示) |
|
代表論文 |
このサブテーマの要点
私たちは、SMARCB1 遺伝子が欠損した小児の 悪性ラブドイド腫瘍 や、若年成人に多い 類上皮肉腫 を対象に、ヒストンアセチル化酵素 CBP/p300 をパラログペアとして同時に阻害する戦略の合成致死性を確立しました(Sasaki et al., Nat Commun, 2024)。これは、1 対 2 対応型(3 因子間)の合成致死性をがん治療標的として実証した、研究室の代表的成果 です。
本研究の中核は、SMARCB1 欠損下で CBP と p300 が KREMEN2 遺伝子のプロモーターに集積し、KREMEN2 を異常に高発現させてがん細胞の生存を支えている という機序の解明です。CBP と p300 を同時に阻害すると、この KREMEN2 依存性が解除され、アポトーシスが誘導されます。
背景
私たちが本研究で取り組んだのは、いずれも 有効な分子標的治療の選択肢が限られている、希少がん・小児がん・若年成人がん です。
悪性ラブドイド腫瘍 は乳幼児期に発症する極めて稀ながんであり、類上皮肉腫 は若年成人~成人に好発する希少肉腫です。これらのがんでは ほぼ全例で SMARCB1 遺伝子が欠損 しており、これが 発がんの主要なドライバー異常 と考えられています。一方で、SMARCB1 自体は欠損(機能喪失)変異であり、従来の分子標的薬の概念では「打つべき標的がない」がんとして位置づけられてきました。
SMARCB1 は、SWI/SNF クロマチンリモデリング複合体(DNA を巻き付けたヒストンの構造を変えて、遺伝子のオン/オフを制御する分子装置)の構成因子の一つです。SWI/SNF 複合体には複数のサブタイプが存在し、その中でも cBAF(canonical BAF)複合体 は SMARCB1 を必須サブユニットとして含む 主要なサブタイプ です。cBAF 複合体の構成因子変異は 多くのヒトがんで認められる とされ、SMARCB1 欠損がんはその中でも cBAF 機能不全が最も顕著に表れる病型に該当します。
これらの SMARCB1 欠損がんは、標準的な化学療法・放射線療法に対して反応性が乏しい症例が多く、既存の分子標的薬で直接標的化できるドライバー異常に乏しく、再発・転移例の予後は不良な、治療選択肢が限られた難治性がん です。新たな治療選択肢の開発が、長く望まれてきました。
発見
パラログの冗長性を逆手に取る発想
ヒトの遺伝子には、機能が重複する パラログ(類似遺伝子) が広く存在し、互いの機能を補い合っています。この 冗長性(redundancy) は、従来型の合成致死探索(1 対 1 対応型)における大きな壁となってきました。欠損したパラログとは別の遺伝子 B を阻害しても、B にパラログ B' が存在する場合、B' が機能を補完してしまい、十分な治療効果が得られにくいためです。
パラログ同時阻害法は、この冗長性を逆手に取る戦略です。 補完経路を断ち切るため、B と B' の両方を同時に阻害します。
標的としての CBP/p300 ── パラログペアの代表例
私たちは、パラログ同時阻害法の最初の実証例として、ヒストンアセチル化酵素 CBP(CREBBP)と p300(EP300) に着目しました。両者は構造・機能ともに極めて酷似したパラログペアであり、細胞内で互いの機能を補い合っています。CBP または p300 の単独阻害では、もう一方による機能補完が残るため、十分な合成致死効果が得られにくいと考えられます。一方、両者を同時に阻害すると補完経路が断たれ、SMARCB1 欠損がん細胞で強い合成致死性が誘導されることを見出しました。
作用機序
なぜ SMARCB1 欠損がん細胞だけが、CBP/p300 同時阻害で特異的に死滅するのか ── 私たちは、その鍵が KREMEN2 遺伝子の異常な発現上昇 にあることを突き止めました。
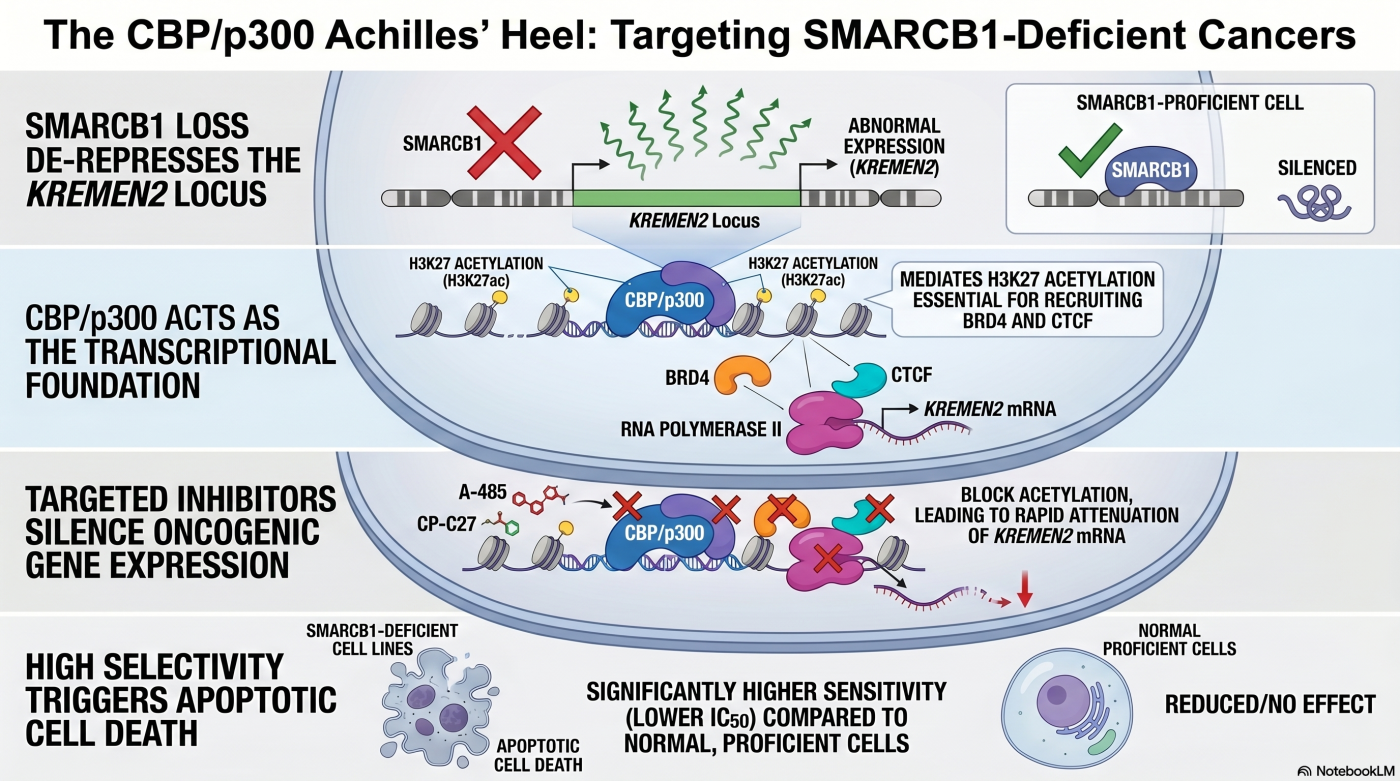
正常な状態(cBAF 機能あり): cBAF 複合体は KREMEN2 遺伝子のプロモーター領域に結合し、その発現を抑え込んでいます。KREMEN2 は普段、ほぼ発現していません。
がんの状態(cBAF 機能不全 = SMARCB1 欠損): SMARCB1 が欠損すると、cBAF 複合体による KREMEN2 の抑え込みが外れます(脱抑制)。代わりに、CBP と p300 が KREMEN2 プロモーターに集積し、ヒストン H3 の 27 番目のリジン(H3K27)をアセチル化することで、KREMEN2 を 異常に高発現 させます。高発現した KREMEN2 タンパク質は、細胞死を誘導する KREMEN1 と結合してその機能を阻害し、本来死ぬはずのがん細胞を生存させてしまいます。
CBP/p300 同時阻害時(治療時): CBP と p300 を同時に阻害すると、KREMEN2 のヒストンアセチル化が消失し、KREMEN2 の転写が停止 します。KREMEN2 タンパク質が消失することで、抑え込まれていた KREMEN1 が解放され、アポトーシス(細胞死)が誘導 されます。
すなわち、SMARCB1 欠損がん細胞は KREMEN2 高発現に依存して生存している と考えられます。CBP/p300 同時阻害(パラログ同時阻害法)は、この KREMEN2 依存性を解除することで、がん細胞の生存基盤を断つ治療戦略です。 このメカニズムは、SMARCB1 欠損がん細胞が 構造的に CBP/p300 へ依存(addiction) していることを示しており、SWI/SNF 機能が保たれた細胞では cBAF 複合体が直接 KREMEN2 を抑え込むため、CBP/p300 への依存度は相対的に低いと考えられます。これが治療ウィンドウ(がん細胞だけを選択的に死滅させられる安全域)の理論的根拠となります。
検証
研究用化合物 CP-C27 を用いた実証
私たちは、CBP と p300 の両方を強力かつ選択的に阻害する低分子化合物 CP-C27 を見出し、本研究のメカニズム検証に用いました。CP-C27 は Sasaki et al., Nat Commun 2024 で公開された 研究用化合物 であり、企業開発品とは独立した位置づけです。
細胞株モデル(in vitro)
CP-C27 は、SMARCB1 欠損 悪性ラブドイド腫瘍細胞株 および SMARCB1 欠損 類上皮肉腫細胞株 に対して、用量依存的かつ細胞種特異的なアポトーシスを誘導しました。一方、SMARCB1 が保たれた正常組織由来細胞や SMARCB1 非欠損のがん細胞株では、同濃度域で生存への影響がほぼ認められませんでした。これは、がん細胞選択性が得られる可能性 を支持する所見です。
マウス xenograft モデル(in vivo)
CP-C27 を SMARCB1 欠損腫瘍をマウスに移植したモデルに投与した結果、腫瘍増殖が明確に抑制 され、一部のモデルでは 腫瘍縮小 が観察されました。本実験条件下では、体重減少などの全身毒性は限定的でした。
メカニズムバリデーション
in vivo で抑制された腫瘍組織を解析したところ、KREMEN2 mRNA/タンパク質の発現低下、KREMEN2 プロモーター領域の H3K27ac の減少、アポトーシスマーカー(cleaved caspase-3 等)の上昇が確認されました。この結果は、in vitro で同定した KREMEN2 脱抑制経路が、in vivo 腫瘍モデルでも作動していることを支持します。
創薬・臨床への展望
本サブテーマは、SMARCB1 欠損希少がんに対する新規治療標的化の科学的基盤を提供するものです。想定される対象患者層は、悪性ラブドイド腫瘍の小児患者さん、類上皮肉腫の若年成人~成人患者さん となります。
創薬開発については、本研究で確立したメカニズム(CBP/p300 同時阻害 → KREMEN2 脱抑制阻止 → アポトーシス誘導)に基づき、製薬企業との連携のもと、公開可能な範囲で研究開発を進めています。具体的な企業開発品の社内コード名・開発フェーズ・契約条件等については、知財および契約上の制約により本ページでは記載していません。
研究室では、本概念を基盤として、cBAF 機能不全を共通項とする他のがん種への適応拡大(→ 本ページ「サブテーマ 2」参照)、cBAF 機能状態を反映する 層別化バイオマーカー の整備、既存の標準療法・免疫療法との合理的な併用療法の探索、治療応答性に影響する 耐性メカニズム の網羅的解析、等の方向への展開を進めています。
関連論文
- Sasaki M, Kato D, Murakami K, Yoshida H, Takase S, Otsubo T, Ogiwara H*. Targeting dependency on a paralog pair of CBP/p300 against de-repression of KREMEN2 in SMARCB1-deficient cancers. Nat Commun. 2024;15(1):4770. PubMed → パラログ同時阻害法(1 対 2 対応型の合成致死性)の概念確立。SMARCB1 欠損がんに対する CBP/p300 同時阻害の合成致死性を実証。
関連プレスリリース
- 2024 年 6 月 26 日: SMARCB1 遺伝子欠損型の小児・AYA 世代のがんに有望な治療標的と阻害剤を発見 → プレスリリース
サブテーマ 2: cBAF 欠損がんへの適応拡大 ── 共通病態に基づく対象がん横断的展開
研究要約
|
項目 |
内容 |
|---|---|
|
対象がん |
cBAF 欠損: 一部の非小細胞肺がん(SMARCA4 欠損 + SMARCA2 発現消失型)、滑膜肉腫(SS18-SSX 融合により cBAF 複合体機能が撹乱される病型) |
|
遺伝子背景 |
SMARCA4 欠損 + SMARCA2 発現消失、SS18-SSX 融合 ── 共通項として cBAF 複合体機能不全 |
|
標的・経路 |
サブテーマ 1 と共通: CBP/p300 パラログペア/KREMEN2 脱抑制経路 |
|
作用機序 |
サブテーマ 1 と共通: CBP/p300 同時阻害により KREMEN2 依存性を解除し、KREMEN1 を介したアポトーシスを誘導(詳細はサブテーマ 1「作用機序」を参照) |
|
創薬上の意義 |
パラログ同時阻害法の 対象がん横断的な適応拡大 を実証。cBAF 複合体機能不全を層別化概念として、複数のがん種に共通する治療標的化の枠組みとなる可能性 を提示 |
|
検証段階 |
in vitro(cBAF 欠損 非小細胞肺がん・滑膜肉腫細胞株での選択的細胞死)/in vivo(代表的なマウス移植モデルでの腫瘍増殖抑制) |
|
創薬段階 |
サブテーマ 1 と共通の研究用化合物 CP-C27 を使用 |
|
代表論文 |
Sasaki et al., Cancer Res Commun, 2025;5(1):24–38. PubMed |
このサブテーマの要点
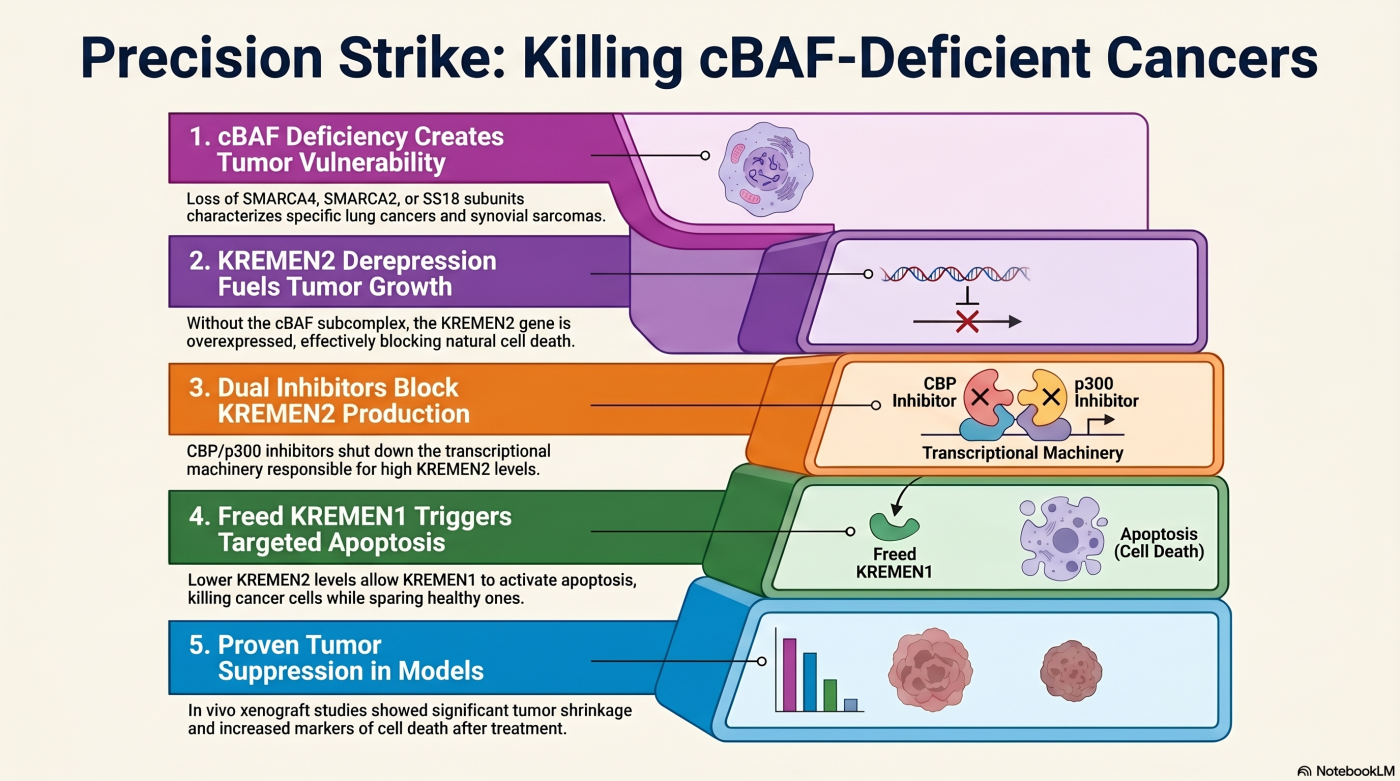
サブテーマ 1 で確立したパラログ同時阻害法(SMARCB1 欠損 × CBP/p300 同時阻害)は、cBAF 複合体機能不全という共通病態を持つ他のがん種にも適応できる ことが示されました(Sasaki et al., Cancer Res Commun, 2025)。
cBAF 機能不全を引き起こす遺伝子異常は SMARCB1 欠損だけにとどまらず、代表的な病型として SMARCA4 変異 + SMARCA2 発現消失型 非小細胞肺がん、SS18-SSX 融合により cBAF 複合体機能が撹乱される 滑膜肉腫 が挙げられます。これらに共通するのは、cBAF 複合体の本来の機能 ── クロマチンを正しく制御し、KREMEN2 のような、cBAF 欠損下で異常発現してがん細胞の生存に寄与する遺伝子 を抑え込む役割 ── が失われている点です。
本サブテーマは、「単一遺伝子の変異」ではなく「複合体の機能状態」を治療層別化の基準とする 新しい考え方を提示しています。
検証
私たちは、サブテーマ 1 で用いた研究用化合物 CP-C27 を、cBAF 欠損がん細胞株群に作用させました。
- SMARCA4/SMARCA2 欠損型 非小細胞肺がん細胞株 で 選択的細胞死 を確認
- SS18-SSX 融合 滑膜肉腫細胞株 でも 同様の合成致死応答 を確認
- 代表的なマウス移植モデルにおいても、腫瘍増殖抑制が確認されました
なお、作用機序(CBP/p300 同時阻害 → KREMEN2 脱抑制阻止 → アポトーシス誘導)はサブテーマ 1 と共通です。詳細は サブテーマ 1「作用機序」 をご参照ください。
創薬・臨床への展望
本サブテーマの結果は、「cBAF 複合体の機能不全」を層別化概念として、複数のがん種に共通する治療標的化の枠組みとなる可能性 を示しています。想定される対象患者層は、SMARCA4 欠損型非小細胞肺がんの成人患者さん、滑膜肉腫の若年~成人患者さん、その他 cBAF 複合体機能不全を共通項とする希少がん・難治がんの患者さん となります。
臨床での層別化(どの患者さんが本治療の恩恵を受けるか)にあたっては、単一遺伝子の変異だけでなく、cBAF 複合体としての機能状態を示すバイオマーカー が重要になると考えています。研究室では、この層別化バイオマーカーの整備を、サブテーマ 1 と並行して進めています。
関連論文
- Sasaki M, Kato D, Yoshida H, Shimizu T, Ogiwara H*. Efficacy of CBP/p300 Dual Inhibitors against De-repression of KREMEN2 in cBAF-Deficient Cancers. Cancer Res Commun. 2025;5(1):24–38. PubMed → パラログ同時阻害法を SMARCA4/A2 欠損 非小細胞肺がん・SS18-SSX 融合 滑膜肉腫へ適応拡大。
キーターム
本ページ全体で使用する主要用語の解説です。
- 1 対 2 対応型合成致死性(パラログ同時阻害法): 「がんでの 1 つの遺伝子異常」に対して「パラログペア(2 つの標的)を同時に阻害」する次世代型の合成致死戦略。3 因子間の関係に基づくため「3 因子間の合成致死性」とも表現される
- パラログ(Paralog): 進化の過程で 1 つの遺伝子が複製され、機能が類似する 2 つのコピーとして並存している遺伝子ペアまたはグループ。互いに機能を補い合うため、片方の阻害だけでは治療効果が出にくいことが多い
- SWI/SNF クロマチンリモデリング複合体: DNA を巻き付けたヒストンの構造を変えて、遺伝子のオン/オフを制御する分子装置。cBAF(canonical BAF)は SMARCB1 を必須サブユニットとして含む主要なサブタイプで、多くのヒトがんで構成因子の変異・欠損が認められる
- SMARCB1: cBAF 複合体の必須構成因子。悪性ラブドイド腫瘍・類上皮肉腫等の希少がん・小児がんでほぼ全例の欠損が認められる、発がんの主要なドライバー異常
- CBP / p300(CREBBP / EP300): ヒストン H3K27 をアセチル化する転写共役因子のパラログペア。構造・基質特異性ともに極めて酷似し、互いに機能を補い合う。本テーマの主標的
- KREMEN2 脱抑制: 本テーマで同定した合成致死の中核メカニズム。SMARCB1 欠損下で cBAF による KREMEN2 抑制が外れ、CBP/p300 が H3K27ac を介して KREMEN2 を異常発現させることで、がん細胞が KREMEN2 高発現に依存する状態
- cBAF 複合体機能不全: SMARCB1 欠損、SMARCA4 欠損 + SMARCA2 発現消失、SS18-SSX 融合 等によって生じる、cBAF 複合体のクロマチン制御機能の喪失状態。複数のがん種に横断的に認められる病態で、本テーマの層別化概念
- 研究用化合物 CP-C27: CBP と p300 の両方を強力かつ選択的に阻害する低分子化合物。Sasaki et al., Nat Commun 2024 で公開された研究ツール化合物であり、企業開発品とは独立した位置づけ
本ページの研究段階について
本ページで紹介する研究はいずれも、現時点では 基礎研究・前臨床研究段階の成果 です。CBP/p300 同時阻害を標的とする治療薬は、現在臨床で使用可能な治療法ではありません。実用化には、阻害剤・分解誘導剤の開発、安全性・薬物動態評価、臨床試験など、複数の段階が必要となります。
関連ハイライト・ページ
- 従来型合成致死 ── 1 対 1 対応型 の合成致死性、特に「パラログ間の合成致死性」に基づく治療法(本テーマの概念の起点)
- 次世代型合成致死 ── 2 対 n 対応型 への概念拡張(Dual SMARCA4/SMARCA2 欠損 × CHD3 阻害 等)。本テーマの系譜の発展形
- データ駆動型探索 ── 公共データから新規標的を抽出する独自アプローチ
- 研究ハイライト(親) ── 6 つの研究テーマの俯瞰
- 研究プロジェクト ── 独自の研究基盤1「パラログ同時阻害法」セクション
- 論文業績 ── 全論文・総説・受賞歴
最終更新日: 2026-05-16

