宇宙観測技術で分子イメージングの新技術を開発!-医学生物学研究での応用へ-
2022年4月5日
東京大学国際高等研究所カブリ数物連携宇宙研究機構
国立研究開発法人国立がん研究センター
理化学研究所
1. 発表のポイント
- 複数の放射性核種プローブを用いた小動物生体内の分子イメージングにおける従来の課題を解決し、多核種を同時かつ正確に画像化することに成功した。
- 宇宙観測用の半導体検出器を搭載した撮像装置を開発し、解析では超新星残骸などの天体観測データの解析で用いられる方法を適用した。
- 医学・生物学的研究の発展への寄与や、核医学検査への応用といった臨床医学への貢献も期待される。
2. 発表概要
東京大学国際高等研究所カブリ数物連携宇宙研究機構 (Kavli IPMU) 特任助教 / 国立がん研究センター先端医療開発センター外来研究員 の柳下 淳 (やぎした あつし) 氏をはじめとする Kavli IPMU や国立がん研究センター先端医療開発センター、理化学研究所、JAXA宇宙科学研究所などの研究者からなる研究グループ (補足を参照) は、複数の放射性核種をプローブ (トレーサー) として用いた小動物生体内における分子イメージング (注1) で従来問題となっていた画像のノイズの課題を解決し、多核種を同時にかつ正確に画像化することに成功しました。研究にあたり本研究グループは、宇宙観測用に用いられていたテルル化カドミウム (CdTe) 半導体検出器 (注2) を搭載した撮像装置を開発し、加えて解析手法にはフィッティングと呼ばれる超新星残骸などの天体観測データの解析で用いられるスペクトル解析方法を適用しました。つまり、今回の成果は宇宙物理学における技術や解析手法が基礎となり、小動物生体内の分子の動態を調べる新たなイメージング技術の開発に結びついた成果と言えます。医学・生物学的研究の発展への寄与や、核医学検査への応用といった臨床医学への貢献も期待されます。さらに近年、プローブの標識核種をがんなど病巣に対する治療効果のある放射性核種に変えることで、生体内での病巣の位置特定のみならず同時に治療を行うことのできる Radio-Theranostics (ラジオセラノスティクス) という新たな診療手法が話題となっています。本研究で開発したイメージング技術では、Radio-Theranosticsで用いられる治療薬の薬物動態イメージングへの展開も期待されます。
本研究成果は、世界的な学術雑誌出版社 Springer Nature が発行する医用生体工学専門誌ネイチャー・バイオメディカル・エンジニアリング (Nature Biomedical Engineering) に2022年4月4日付(日本時間4月5日午前0時)で掲載されました。
3. 発表内容
背景
生物学実験では、蛍光を発する蛍光物質をプローブ (トレーサー) として用い蛍光顕微鏡でイメージングすることで多くの分子を同時にかつミクロのレベルで詳細に観察できます。しかし、蛍光は組織に大部分が吸収されてしまうため細胞のみを取り扱うなど生体外の実験で用いるには有用ですが、動物の生体内の観察、とくに人間などの大型動物のイメージングには不向きです。そのため、動物生体内の分子イメージングでは、可視光と違い組織を透過しやすい放射線を発する放射性核種をプローブに用いたイメージングが行われます。放射線によるイメージングには主にポジトロン断層法(PET)と単一光子放射断層撮影(SPECT)があり、SPECT では複数の放射性核種のプローブを用いることが可能です。しかし、エネルギー (波長) が違う放射線を区別する能力 (エネルギー分解能)(図1)、画像のノイズとなるような放射線の混入、空間分解能、などの問題があり、複数の放射性核種のプローブを用いた分子イメージングにおいては、鮮明で正確かつ精細な画像を得ることが難しいという課題がありました。
研究手法・成果
東京大学国際高等研究所カブリ数物連携宇宙研究機構 (Kavli IPMU) 特任助教 / 国立がん研究センター先端医療開発センター外来研究員の柳下 淳 (やぎした あつし) 氏をはじめとする本研究グループは、低エネルギー領域の放射線を用いた小動物生体内のイメージングにおける従来の問題点を解決し、複数の放射性核種プローブを用いて鮮明・正確・精細な画像を得ることを目的に研究を進めました。
実験では、空間分解能が200μm (マイクロメートル) 程度となるように設計されたマルチピンホールコリメーター、および、高エネルギー分解能を有するテルル化カドミウム (CdTe) 半導体検出器を搭載し、「IPMU イメージャー」と名付けた Kavli IPMU が中心となり開発した SPECT 試作機であるプラナー (平面) イメージャーを撮像装置として用いました (図2)。CdTe 検出器は宇宙観測用のX線天文衛星ひとみ (ASTRO-H) に搭載されていたものと質的に同一のもので、低エネルギーの X 線に対し高いエネルギー分解能を有することが先行研究で明らかになっています。つまり、CdTe 検出器は医療の臨床現場などで用いられているシンチレーション検出器 (注3) に比べ複数の放射性核種を明瞭に区別することが可能です。しかし、エネルギーが非常に近接した放射線や散乱線など、他の放射線源からの放射線の混入を完全に除去することは不可能であり、画像上のノイズや定量された放射線量の正確性に問題がありました。
そこで本研究グループでは更に、超新星残骸などの天体観測データの解析で用いられるフィッティングと呼ばれるスペクトル解析方法(図3)を用いました。そうすることで、他の放射線源からの放射線も含め、検出された全ての放射線の由来を同定したのちに目的の放射線のみをイメージングすることで正確な定量性が保たれたノイズのない画像を取得することを試みました。
まずは模型で検証を行い、意図した結果が得られたことを確認したのちに実際にマウスで実験を行いました。実験では、テクネチウム-99m (99mTc)、 インジウム-111 (111In) 、ヨウ素-125 (125I) の3種類の放射性核種プローブを用いました。それぞれのプローブは、1-2mm程度の大きさであるリンパ節および甲状腺に集積するようにしました。具体的には、99mTcが耳近傍のリンパ節 (浅耳下腺リンパ節)、111In が顎の下のリンパ節 (下顎リンパ節)、125I が甲状腺に集積するようにしています (図4a)。そして、撮像の結果まず得られたスペクトルを見ると、核種からの放射線の他にも蛍光X線や散乱線など画像上のノイズとなる放射線が多く存在していることがわかります。しかし、これをフィッティングで解析することで、それぞれの成分に分離・同定することができました (図4b)。例えば、甲状腺に集積した125I をイメージングする場合、そのスペクトルが多く存在する26-29 keV (キロ電子ボルト) の放射線を利用してイメージングを行いますが、図4b で示すスペクトルからわかるように他の放射線 (26-29 keVの範囲では赤の点線で示す111Inからの放射線と、緑の点線で示す99mTcからの放射線が僅かに混入している) の混入があることから甲状腺以外のものも画像上で描き出されてしまっています (図4c)。しかし、フィッティングにより125Iのスペクトルのみを用いるとマウスの甲状腺のみ正しく描き出すことができました。つまり、本研究グループは、開発した撮像装置による撮像に加え、フィッティングの解析手法を用いることで、各核種を同時にかつ正確に画像化することに今回成功したのです (図4d)。
波及効果、今後の予定
本研究で開発したイメージング技術を用いることにより生体内での現象をより詳しく観察することが可能となりました。今回は SPECT 試作機での実験でしたが、既にフルスペックの SPECT 撮像装置は完成しており、本研究のイメージング技術を適用可能です。本研究で開発した技術は従来の課題を解決し、小動物生体内において複数の放射性核種プローブを用いて高空間分解能な画像を同時に得られることから、医学・生物学的研究への応用が可能です。加えて、放射性核種を用いたイメージング技術はすでに医学分野で病巣の位置特定および性状評価といった診断技術として活用されており、臨床医学への応用も期待されます。さらに近年では、確実な治療効果を上げられるとして Radio-Theranostics (ラジオセラノスティクス) という新たな診断と治療を一体化した手法が話題となっています。これは、イメージングプローブの技術を応用した診療手法であり、イメージングを行う際にプローブとなる標識核種をα (アルファ) 線やβ (ベータ) 線といった放射線を出す核種に変えることで、生体内のがんの場所への核種の到達を確認したうえで、その病巣を確実に治療することができます。この Radio-Theranostics治療に用いる治療用核種の中には γ (ガンマ) 線を放出するものも多くあり、治療薬が本当に病巣に届いて効いているのかをイメージングすることが理論的には可能です。100keV以下の低エネルギー領域のγ線の検出は、診療の現場で用いられている現行のシンチレーション検出器が苦手としますが、散乱成分を多く含むなどの特性は、CdTe 検出器は、散乱線成分を多く含む低エネルギー領域の放射線の検出を得意とします。つまり、本研究で開発したイメージング技術は、Radio-Theranosticsはじめ更なる臨床開発への貢献が期待されます。
補足
本研究は、Kavli IPMU に発足し2018年4月1日に本格的に活動を開始した「硬 X 線・γ線イメージング連携拠点」及び文部科学省 科学研究費助成事業 新学術領域研究 (2018–2022)「宇宙観測検出器と量子ビームの出会い。新たな応用への架け橋。」に参画する研究者の連携のもと生み出された成果です。この研究グループは、宇宙観測用に開発された硬X線・γ線検出器である CdTe 検出器の異分野への応用や研究課題解決に活用すべく活動しています。なお、「硬X 線・γ線イメージング連携拠点」は、慶應義塾大学医学部の協力のもとKavli IPMU とJAXA宇宙科学研究所の連携により、硬 X 線・γ線イメージング技術の核医学、特にがん研究への加速的応用を行うことを目標に立ち上げられ、現在では、様々な他機関の医学や薬学の研究者も連携し共に研究を行なっています。
「硬 X 線・ガンマ線イメージング連携拠点」立ち上げ時のプレスリリースについては、2018年3月26日 <基礎科学は役に立つ -「JAXA - Kavli IPMU/東京大学 硬X線・ガンマ線イメージング連携拠点」 本格始動 -> の Kavli IPMU の記事を参照
https://www.ipmu.jp/ja/20180326-ImagingHub(外部サイトにリンクします)
新学術領域研究 (研究領域提案型)「宇宙観測検出器と量子ビームの出会い。新たな応用への架け橋。」は下記リンクを参照https://member.ipmu.jp/SpaceTech_to_QuantumBeam/index.html(外部サイトにリンクします)
4. 用語解説
(注1) 分子イメージング
生体内において注目したい分子の動きや働きを画像化する手法。分子を可視化するための標識となる分子プローブ (トレーサー) とイメージャーと呼ばれる撮像装置が必要であり、分子プローブから発せられた可視光もしくは放射線といった固有の波長/エネルギーを有した電磁波をイメージャーで検出し、画像解析プログラムを経て画像化できる。手法によっては、複数の分子をそれぞれ別の色で可視化することも可能であり、それらの分子の生物学的意義を検討できる。更に、画像の分解能が高いとミクロの世界における特定分子の局在の様子や関係性までも研究することができる。
(注2) テルル化カドミウム (CdTe) 半導体検出器
カドミウム(Cd)とテルル(Te)からなる化合物半導体を用いた検出器。硬X線と呼ばれる高いエネルギーのX線や、γ線を吸収し、高い感度で検出できるという性質を持つ。1990年代に沖縄にあるアクロラド社が大面積のカドテル結晶の製造に成功。本研究グループに参加する Kavli IPMU の高橋忠幸 主任研究者が JAXA 宇宙科学研究所に所属していた当時、学生だった渡辺伸氏 (現 JAXA宇宙科学研究所助教, Kavli IPMU連携研究員) らと同社との共同研究により CdTe 検出器 の実用化に先鞭をつけた。
(注3) シンチレーション検出器
X 線や γ 線をはじめとする放射線が当たると蛍光を発するシンチレータと呼ばれる物質 (物質の種類により固体や液体の状態で用いる) とその蛍光から出た光子を増幅する光電子増倍管を組み合わせた検出器。素粒子物理学実験、医療機器など様々な分野で放射線測定装置として利用されている。
5. 発表雑誌
- 雑誌名: Nature Biomedical Engineering
- 論文タイトル: Simultaneous detection and spectral separation of multiple radionuclide tracers in vivo via a cadmium telluride diode detector
- 著者: Atsushi Yagishita (1,2), Shin’ichiro Takeda (1), Miho Katsuragawa (1), Tenyo Kawamura (3,1), Hideaki Matsumura (1), Tadashi Orita (1), Izumi O. Umeda (1), Goro Yabu (3,1), Pietro Caradonna (1), Tadayuki Takahashi (1), Shin Watanabe (4,1), Yousuke Kanayama (5), Hiroshi Mizuma (5), Kazunobu Ohnuki (2), Hirofumi Fujii (2)
- 著者所属:
1. Kavli Institute for the Physics and Mathematics of the Universe (Kavli IPMU, WPI), The University of Tokyo, 5-1-5, Kashiwanoha, Kashiwa, Chiba 277-8583, Japan
2. Exploratory Oncology Research and Clinical Trial Center, National Cancer Center, 6-5-1 Kashiwanoha, Kashiwa,Chiba 277-8577, Japan
3. Department of Physics, The University of Tokyo, 7-3-1 Hongo, Bunkyo, Tokyo 113-0033, Japan
4. Institute of Space and Astronautical Science (ISAS)/JAXA, 3-1-1 Yoshinodai, Chuo-ku, Sagamihara, Kanagawa 252-5210, Japan
5. Laboratory for Pathophysiological and Health Science, RIKEN Center for Biosystems Dynamics Research, 6-7-3 Minatojima-minamimachi, Chuo-ku, Kobe, Hyogo 650-0047, Japan - DOI: 10.1038/s41551-022-00866-6 (2022年4月4日掲載)
- 論文のアブストラクト (Nature Biomedical Engineering のページ)
https://www.nature.com/articles/s41551-022-00866-6(外部サイトにリンクします)
6. 問い合わせ先
報道に関する連絡先
東京大学国際高等研究所カブリ数物連携宇宙研究機構
広報担当 小森 真里奈
E-mail:press@ipmu.jp
TEL: 080-4056-2930 / 04-7136-5977
国立研究開発法人国立がん研究センター
企画戦略局 広報企画室(柏キャンパス)
E-mail:ncc-admin@ncc.go.jp
TEL:04-7133-1111
理化学研究所
広報室 報道担当
E-mail:ex-press@riken.jp
関連リンク
- 2018年3月26日 プレスリリース <基礎科学は役に立つ -「JAXA - Kavli IPMU/東京大学 硬X線・ガンマ線イメージング連携拠点」 本格始動 ->:Kavli IPMU の記事
https://www.ipmu.jp/ja/20180326-ImagingHub(外部サイトにリンクします) - 宇宙を見る目で「がん」を捉える ―異分野の壁を超えるイメージング技術―(Kavli IPMU前編):日本学術振興会 WPI Forumの記事
https://wpi-forum.jsps.go.jp/sousei/vol2-1/(外部サイトにリンクします) - 宇宙を見る目で「がん」を捉える―異分野の壁を超えるイメージング技術―(Kavli IPMU後編):日本学術振興会 WPI Forumの記事
https://wpi-forum.jsps.go.jp/sousei/vol2-2/(外部サイトにリンクします) - 新学術領域研究 (研究領域提案型)「宇宙観測検出器と量子ビームの出会い。新たな応用への架け橋。」
https://member.ipmu.jp/SpaceTech_to_QuantumBeam/index.html(外部サイトにリンクします)
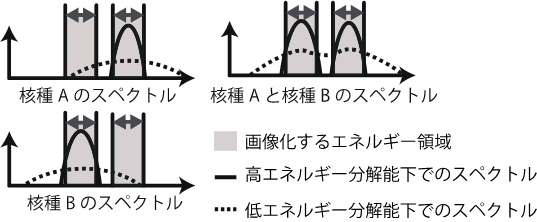
図1. エネルギー分解能を模式的に解説した図。図1左上は核種Aからの放射線のエネルギースペクトル。図1の左下は核種Bからの放射線のエネルギースペクトル。核種Aと核種Bが同時に存在していた場合のエネルギースペクトルは図1の右上のようになる。エネルギー分解能の低い検出器では点線で示すような2つの山を持ったなだらかなスペクトルとしてしか捉えられず、核種AとBのエネルギースペクトルを正確に測ることが出来ない。しかし、エネルギー分解能の高い検出器であれば、核種AとBのエネルギースペクトルを分離でき、それぞれの核種からのエネルギーを正確に測ることができる。(Credit:Yagishita et al.)
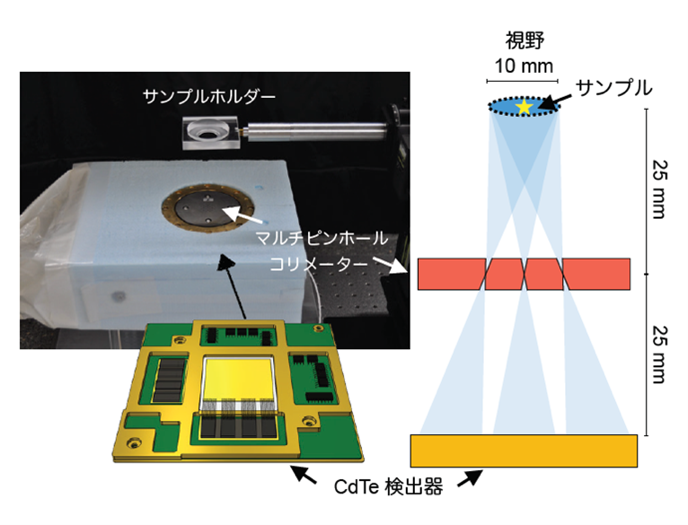
図2. 本研究で用いた撮像装置の写真と装置の模式図。CdTe検出器は写真中では見えていないが、マルチピンホールコリメーターの下の箱の中に収められている。(Credit:Yagishita et al./Kavli IPMU)
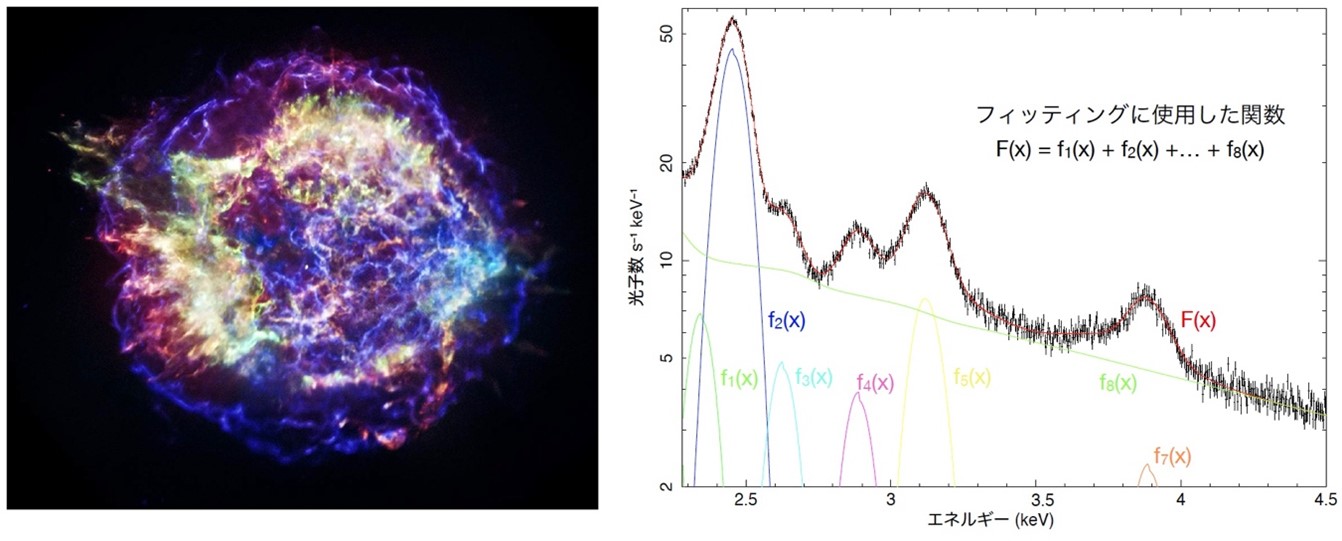
図3. 超新星残骸カシオペア A の観測データを用いたスペクトルフィットの概念図。図の左はチャンドラで捉えたX線で見たカシオペア Aの画像。右はすざく衛星のデータを用いて解析したX線エネルギースペクトル (*本概念図説明のため簡易に解析したものであり、実際の解析関数や手順は踏んでいないことに注意)。実際の解析では、右のX線エネルギースペクトルのデータに対して物理過程を考慮した関数をフィッティングする事で、超新星残骸のどの部分にどのような元素が分布しているかを明らかにすることができる。(左画像 Credit: NASA/CXC/SAO, 右図 Credit: Kavli IPMU)
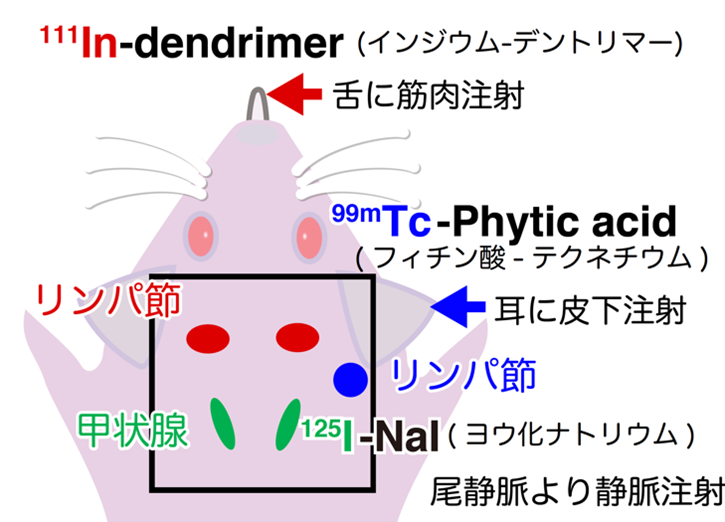
図4a. 実験で用いた生体のマウスのどの部位に3種類の放射性核種が集積するようにしたかを示した模式図。テクネチウム-99m (99mTc) が耳近傍のリンパ節(浅耳下腺リンパ節)、インジウム-111 (111In) が顎の下のリンパ節(下顎リンパ節)、ヨウ素-125 (125I) が甲状腺に集積するようにした。(Credit:Yagishita et al./Kavli IPMU)
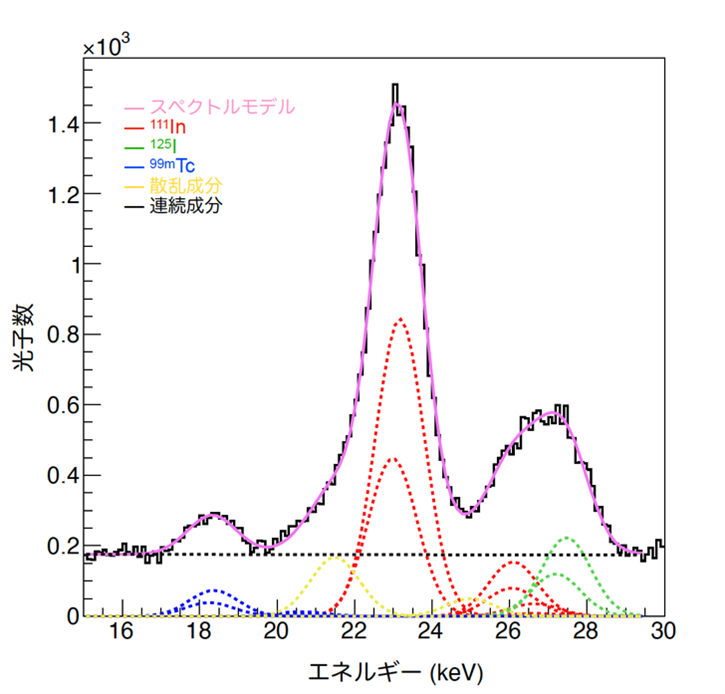
図4b. 撮像の結果まず得られたスペクトルと、フィッティングによってそれぞれの成分に分離・同定したスペクトル。撮像の結果まず得られた生の信号は黒線、その信号をまずフィッティングして滑らかな曲線のスペクトルとして表現したのがピンク色の線。その後、フィッティングによる更なる解析の結果、赤点線で示す111In、緑点線で示す125I、青点線で示す99mTc、黄色点線で示す散乱線、黒点線で示す連続成分に分離できた。(Credit:Yagishita et al./Kavli IPMU)
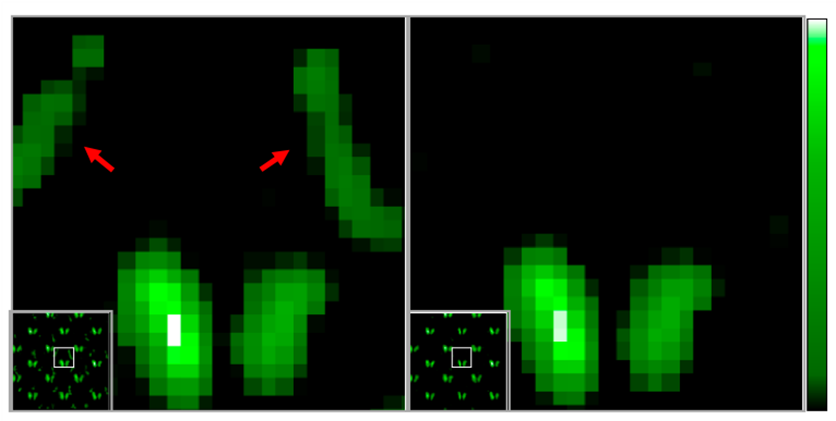
図4c. 生体のマウスに集積した核種を26-29 keV (キロ電子ボルト) の放射線を利用して撮像装置でイメージングした画像。甲状腺に集積した125I をイメージングすることを目的として26-29 keVを利用しているが、赤矢印で示すように下顎リンパ節に集積した111Inからの散乱線成分も画像化されてしまっている。(Credit:Yagishita et al.)
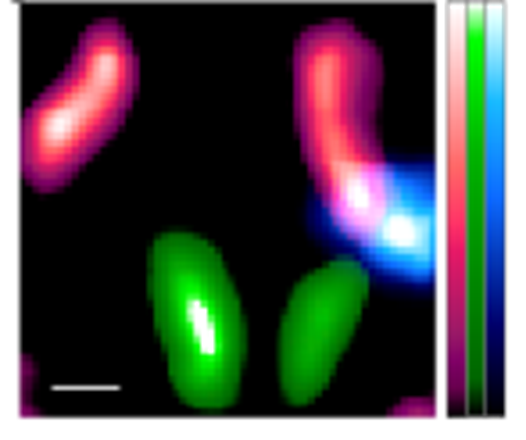
図4d. 各核種を同時かつ正確に画像化することに成功したことを示す図。フィッティングによって各核種を分離・同定したスペクトルの情報を利用し、図4cでイメージングした画像をそれぞれの核種からの放射線に分けて描き出すことができた。赤色の部位が111Inの集積した下顎リンパ節、青色の部位は99mTcの集積した浅耳下腺リンパ節、緑色の部位は125Iの集積した甲状腺である。図中左下の白線で示すスケールバーは1ミリメートル。(Credit:Yagishita et al.)
