DNAメチル化キャプチャ法を用いたDNAメチル化関連解析により腎細胞がんと関連する新規DNAメチル化バイオマーカー候補を発見
2022年5月18日
岩手医科大学いわて東北メディカル・メガバンク機構
慶應義塾大学医学部
国立がん研究センター
発表のポイント
- 岩手医科大学いわて東北メディカル・メガバンク機構(IMM)は、慶應義塾大学医学部および国立がん研究センターとの共同研究において、淡明細胞型腎細胞がん(clear cell renal cell carcinoma:ccRCC)*1に対する新規の血液DNAメチル化*2バイオマーカー*3の探索を行いました。
- ccRCC患者の血液由来DNAは国立がん研究センター受診者の方々から提供いただき、その対照群(コントロール群)を東北メディカル・メガバンク(TMM)計画*4地域住民コホート研究民*5参加者から選定し、DNAメチル化キャプチャ法*6によるDNAメチル化解析を行いました。
- 対照群に比べ、ccRCC群では染色体5番に位置するPCBD2/MTND4P12遺伝子上の6ヶ所のCpG部位*7が有意に低メチル化状態にあることを明らかにしました。
- 当該6ヶ所のCpG部位がccRCCの診断のバイオマーカーとして有用であるかを調べたところ、有用性の指標であるAUC-ROC値(Area under the receiver operating characteristic curve)*8が、探索段階で0.922、検証段階で0.871と、非常に高い値を示しました。
- 今回同定されたccRCC関連DNAメチル化バイオマーカー候補について、今後、ccRCCの進行度との相関を詳細に解析することで、新たな診断法や治療薬の開発につながることが期待されます。
概要
岩手医科大学いわて東北メディカル・メガバンク機構(IMM)生体情報解析部門の大桃秀樹 特任准教授、同部門部門長の清水厚志 教授、慶應義塾大学医学部病理学教室の金井弥栄 教授、同教室の新井恵吏 准教授、国立がん研究センター中央病院 藤元博行 副院長、同病院遺伝子診療部門 吉田輝彦 部門長らの研究グループは、主要な腎細胞がんである淡明細胞型腎細胞がん(ccRCC)患者50名と対照群50名の全血由来DNAにおけるDNAメチル化解析を行い、ccRCCに関連してDNAメチル化状態が変化するCpG部位を探索したところ、染色体5番のPCBD2/MTND4P12遺伝子上に位置する6ヶ所のCpG部位がccRCCの新規DNAメチル化バイオマーカーとなり得ることを発見しました。
さらに、別の独立したccRCC患者48名と対照群48名において、本バイオマーカーの有用性を検証したところ、ccRCCに対するDNAメチル化マーカーとして十分な有用性があることが示されました。本研究成果は、国際科学雑誌 Epigenetics Communications誌に2022年5月2日付(オンライン公開)で掲載されました(https://epicom.biomedcentral.com/articles/10.1186/s43682-022-00009-7(外部サイトにリンクします))。
研究背景
腎細胞がん(renal cell carcinoma:RCC)は、腎臓の実質に悪性細胞が発生したもので、全がんの4%、腎臓がんの80%を占めています。早期RCCの5年生存率は約93%ですが、転移性RCC患者の5年生存率は12%に留まることから早期発見が重要です。しかしながら、RCC発症初期には大きな症状はなく、健康診断や高血圧、糖尿病、肥満など他の病気の検査で偶然に発見されることが多い特徴をもつことからも早期発見は難しいとされています。RCCの70%以上は淡明細胞型腎細胞がん(ccRCC)に分類されます。そのため、ccRCCを早期に診断する有効なバイオマーカーも見つけることができれば、多くのRCC患者を早期に発見、治療することにつながることが期待されます。
これまでにゲノムワイド関連解析(Genome-wide association study: GWAS)*9やメタアナリシス*10によって、RCC発症に関わる遺伝子が複数同定されていますが、遺伝的背景で説明できるRCCは3~5%と言われています。一方、実際のRCCの発症は、喫煙、飲酒、肥満などの非遺伝的要因(環境要因)に起因して50歳以降に発症することが多いとされています。近年、非遺伝的要因(環境要因)によりDNAのメチル化状態が変化し、それに伴い遺伝子発現も変化することで疾患発症につながっていることが明らかになっており、DNAメチル化は新規バイオマーカーとして期待されています。
そこで本研究では、ccRCC患者群およびその患者群と性別・年齢をマッチングさせた健常対照者群の全血由来DNAを用いて、ターゲットバイサルファイトシーケンス法(Targeted-bisulfite sequencing; TB-seq)*11によるDNAメチル化解析を行い、エピゲノムワイド関連解析(Epigenome-wide association study;EWAS)*12によってccRCCに関連するDNAメチル化バイオマーカーを探索しました。
研究成果
本研究グループは、国立がん研究センターバイオバンク*13の50名のccRCC患者(ccRCC群)および、ccRCC患者と性別・年齢をマッチングさせたTMM計画地域住民コホート研究参加者50名(対照群)の全血由来DNAを用いて、TB-SeqによるDNAメチル化解析およびEWASを行いました(探索実験)。その結果、5番染色体のPCBD2(pterin-4 alpha-carbinolamine dehydratase 2)遺伝子とMTND4P12(mitochondrially encoded NADH: ubiquinone oxidoreductase core subunit 4 pseudogene 12)遺伝子上に位置する6ヶ所のCpG部位において、ccRCC群で有意に10%以上低メチル化していることが明らかになりました(p < 1.59 × 10-8、図1A-G)。
次に、その得られた結果が正しいかを検証するため、先のccRCC群や対照群とは別のccRCC患者と対照群をそれぞれ48名ずつ同センターバイオバンクと、TMM計画地域住民コホート研究参加者から全血由来DNAを準備し、TB-SeqおよびEWASを行いました(検証実験)。その結果、同様にPCBD2遺伝子およびMTND4P12遺伝子上に位置するCpG部位のDNAメチル化レベルが、ccRCC群において対照群と比べて有意に10%以上低下していました(p < 3.42 × 10-8)。
さらに、PCBD2/MTND4P12遺伝子上の6ヶ所のCpG部位がccRCCのバイオマーカーとして有用であるかを調べるために、臨床検査やバイオマーカーの有用性を検討する手法であるROC曲線による解析を行いました。その結果、6ヶ所のCpG部位の個々のDNAメチル化レベルよりも、6ヶ所のDNAメチル化レベルの合計を用いた方がccRCCのバイオマーカーとしての有用性が高いことが示されました(表1)。その有用性を示すAUC-ROC値(Area under the receiver operating curve)は、探索実験ではAUC-ROC = 0.922(図2A)、検証実験でAUC-ROC = 0.871(図2B)と共に高い有用性が示されました。
以上の結果から、PCBD2/MTND4P12遺伝子上の6ヶ所のCpG部位のDNAメチル化レベルの合計は、ccRCCに対する新規DNAメチル化バイオマーカーとして利用できる可能性が示唆されました。
まとめと展望
本研究は、DNAメチル化キャプチャ法を用いたDNAメチル化関連解析により、ccRCCに対する血液由来DNAに基づいた新規DNAメチル化バイオマーカー候補を同定しました。
今後は、本研究で同定したccRCCに対するDNAメチル化バイオマーカーが臨床応用できるよう、TMM計画で進めている前向きコホート研究の参加者などを対象として、未病または発症早期のccRCCを検出可能か、また腎摘手術後の予後マーカーとしても利用可能かなど調べたいと考えています。さらに、本研究は日本人を対象とした研究成果であるため、他の民族においても有用であるか検証が期待されます。
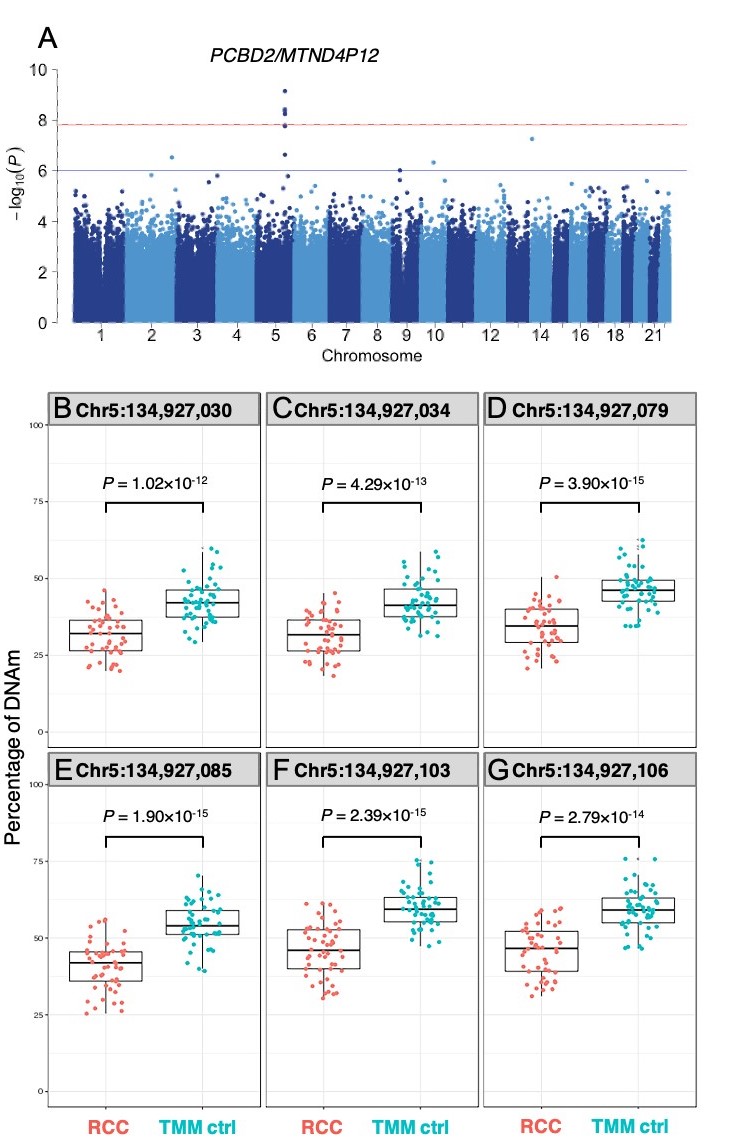
図1.探索実験におけるccRCCに対するEWAS結果に基づくManhattanプロット*14A)およびDNAメチル化レベルに基づくJitterプロット*15(B-G)
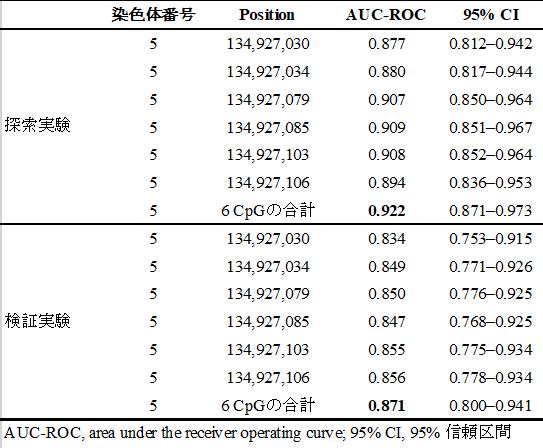
表1.AUC-ROC解析の結果
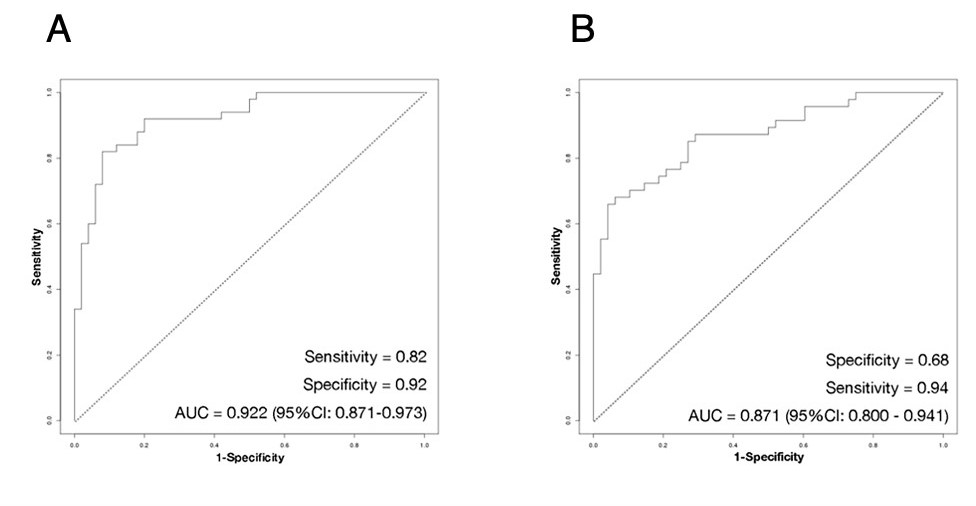
図2.PCBD2/MTND4P12遺伝子上の6ヶ所のCpG部位のDNAメチル化レベルの合計に基づくAUC-ROC解析の結果(CpG探索実験(A)、検証実験(B))
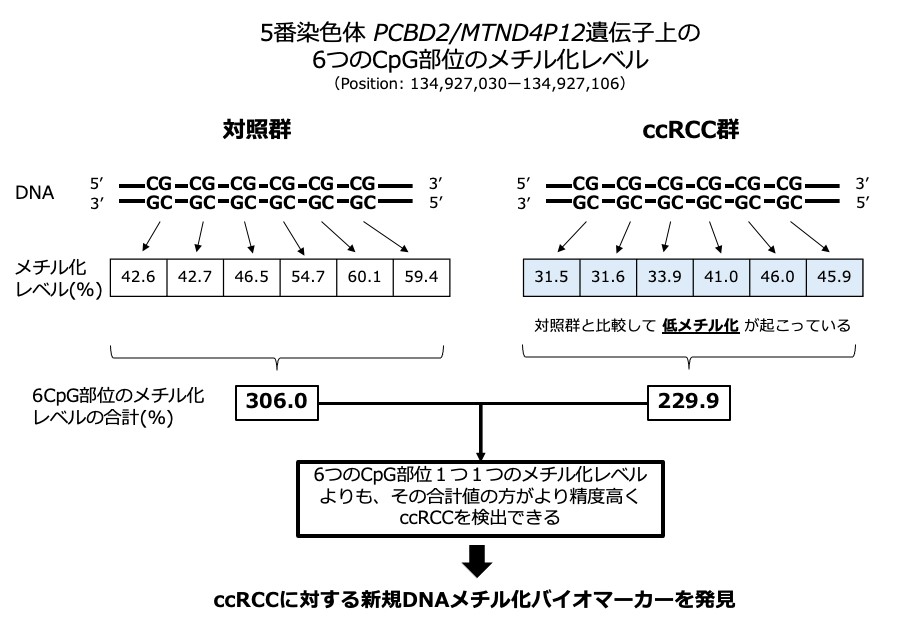
図3.本研究のコンセプト図
謝辞
本研究は、日本医療研究開発機構(AMED)の支援を受けて実施しました。本研究の実施にあたり、岩手医科大学は慶應義塾大学と研究開発契約を締結しており、また、本研究における慶應義塾大学の別研究開発契約先である国立がん研究センターの協力を得ております。
用語解説
*1 淡明細胞型腎細胞がん(clear cell renal cell carcinoma;ccRCC)
成人で最も一般的なタイプの腎がんで、腎がん患者の70%がccRCCに分類されると言われています。ccRCCは、病理所見において透明な腫瘍細胞が多くみられることが特徴です。
*2 DNAメチル化
DNAを構成する塩基A(アデニン)、C(シトシン)、G(グアニン)、T(チミン)のうち、主にCとGが並ぶ部位(CpG)のCにメチル基(-CH3)が付くことをいいます。発生時期の細胞の種類の決定や遺伝子発現の制御などに関与しており、生活習慣や環境化学物質の曝露などによって後天的に変化します。
*3 バイオマーカー
2001年にBiomarkers Definitions Working Groupによって、「通常の生物学的過程、病理学的過程、もしくは治療的介入に対する薬理学的応答の指標として、客観的に測定され評価される特性」と定義されています(Clin Pharmacol Ther. 69, 89-95)。今回の研究では「血液検査だけで、がんを早期発見できるバイオマーカー」開発を目指しています。
*4 東北メディカル・メガバンク(TMM)計画
東日本大震災からの復興事業として平成23年度から始められ、被災地の健康復興と、個別化予防・医療の実現を目指しています。
IMMと東北大学東北メディカル・メガバンク機構(ToMMo)を実施機関として、東日本大震災被災地の医療の創造的復興および被災者の健康増進に役立てるために、合計15万人規模の地域住民コホート調査および三世代コホート調査を平成25年より実施し、収集した試料・情報をもとにバイオバンクを整備しています。
東北メディカル・メガバンク計画は、平成 27 年度より、AMEDが本計画の研究支援担当機関の役割を果たしています。
*5 コホート研究
ある特定の集団を一定期間にわたって追跡し、生活習慣などの環境要因や遺伝的要因などと疾病発症との関係を解析するための研究。未来に向かって調査を進める研究を前向きコホート研究といいます。
*6 DNAメチル化キャプチャ法
解析対象とするターゲットの配列を集め(=キャプチャ)、その配列のDNAメチル化状態を解析する手法です。ターゲット配列については、試薬メーカーがデザインした既製品試薬が販売されていますが、研究者自身でデザインしメーカーに製造してもらうカスタム品による解析も可能です。本研究では、既製品とカスタム品の両方を使用して解析しました。
*7 CpG部位
CとGの2塩基が連続して並ぶDNAの領域をCpG部位と呼びます。CpG部位はDNAのメチル化を受けやすい部位として知られています。
*8 AUC-ROC値(Area under the receiver operating characteristic curve)
縦軸を真陽性率、横軸を偽陽性率として描かれたROC曲線の右下部分の面積をAUC-ROC値といい、検査の有用性(精度)の指標の一つです。AUC-ROC値は、最大値は1で、一般的に0.8以上を示すと有用性(精度)が高いと言われています。
*9 ゲノムワイド関連解析(Genome-wide association study; GWAS)
個人間の形質の違いと遺伝子多型の違いとの関連をゲノム全体に対して統計的に調べる方法です。
*10 メタアナリシス
複数の研究結果を統合して統計解析する手法のことで、個々の研究結果よりも信頼性の高い結果を得ることができます。科学的な根拠を示すエビデンスレベルは、最も高く位置付けられている解析手法です。
*11 ターゲットバイサルファイトシーケンス(Targeted-bisulfite sequencing; TB-seq)
DNAメチル化解析方法の1つです。全ゲノム中に約3,200万ヶ所以上存在するCpG部位のうち、数十万~数百万カ所を対象にDNAメチル化解析を行うことができる方法です。本研究では、メーカーが開発・販売している試薬と本研究グループが独自に開発した試薬の両方を使用してDNAメチル化解析を行いました。
*12 エピゲノムワイド関連解析(Epigenome-wide association study;EWAS)
エピゲノムとは、ゲノムに加えられた修飾のことで後天的に変化するもので、DNAメチル化はその1つです。EWASとは、主に疾患や生活習慣と関連してDNAメチル化状態が変化するCpG部位を探索する手法です。これにより、これまでも多くのDNAメチル化バイオマーカーが見つかっています。
*13 国立がん研究センターバイオバンク
国立がん研究センターバイオバンクは、中央病院(東京都中央区)、東病院(千葉県柏市)を受診された患者さんにご協力いただき、検査に使われた血液や組織、手術などで摘出された組織の残りと診療情報などを保管し、がん研究をはじめとする広い範囲の医学研究に活用する仕組みです。これまで、治療標的となる新たながん遺伝子の発見や阻害剤の特定など、がんの予防・診断・治療に関する数多くの研究が実施され、その論文の61%が国立がん研究センター外部の研究機関との共同研究の成果となっています。
*14 Manhattanプロット
横軸に染色体1番から染色体順にDNAメチル化部位を、縦軸に関連性の指標を示すP値の-log10をプロットしています。染色体上のDNAメチル化部位と疾患との関連を俯瞰する表示法です。P値の閾値は赤い線に設定しており、それより上にあるプロットは有意に疾患と関連があると見なします。
*15 Jitterプロット
当該CpG部位における個人ごとのメチル化レベルをプロットしたグラフです。各図中の四角は箱ひげ図と呼ばれ、四角内のやや太い横線は、各群におけるメチル化レベルの中央値を示しています。
論文情報
掲載雑誌
Epigenetics Communications(オンライン)
論文タイトル(英語)
Potential DNA methylation biomarkers for the detection of clear cell renal cell carcinoma identified by a whole blood-based epigenome-wide association study
論文タイトル(日本語)
全血由来DNAにおけるエピゲノム関連解析による淡明細胞型腎細胞がんの検出に有用なDNAメチル化バイオマーカー候補の同定
著者名(英語)
Hideki Ohmomo1,2, Shohei Komaki1, Yoichi Sutoh1, Tsuyoshi Hachiya1,2, Kanako Ono1, Eri Arai3, Hiroyuki Fujimoto4, Teruhiko Yoshida5, Yae Kanai3, Koichi Asahi1,6, Makoto Sasaki1,7, Atsushi Shimizu*1,2
*責任著者
著者名(日本語)
大桃 秀樹1,2、小巻 翔平1、須藤 洋一1、八谷 剛史1,2、小野 加奈子1、新井恵吏3、藤元 博行4、吉田 輝彦5、金井 弥栄3、旭 浩一1,6、佐々木 真理1,7、清水 厚志 *1,2
*責任著者
著者所属
- 岩手医科大学 いわて東北メディカル・メガバンク機構
- 岩手医科大学 医歯薬総合研究所 生体情報解析部門
- 慶應義塾大学 医学部 病理学教室
- 国立研究開発法人 国立がん研究センター 中央病院 泌尿器・後腹膜腫瘍科
- 国立研究開発法人 国立がん研究センター 中央病院 遺伝子診療部門
- 岩手医科大学 医学部 腎・高血圧内科
- 岩手医科大学 医歯薬総合研究所 超高磁場MRI診断・病態研究部門
DOI
10.1186/s43682-022-00009-7
問い合わせ先
研究内容に関して
岩手医科大学
いわて東北メディカル・メガバンク機構 生体情報解析部門
部門長 清水 厚志
報道に関して
いわて東北メディカル・メガバンク機構 広報・企画部門
部門長 遠藤 龍人
電話番号:019-651-5111(内線5509)
慶應義塾大学
信濃町キャンパス総務課
電話番号:03-5363-3611 Eメール:med-koho●adst.keio.ac.jp
国立がん研究センター
企画戦略局 広報企画室
電話番号:03-3542-2511 Eメール:ncc-admin●ncc.go.jp
