がんゲノム医療とは

正常の細胞は、核の中にカラダの設計図であるゲノムというものを持っています。このゲノムの中で、特にタンパク質に関係した部分を遺伝子と呼び、遺伝子には2万あまりの種類があることが分かっています。がんが生まれる主な原因はこの遺伝子の異常、すなわち遺伝子に傷が入ることだとされています。
そのため、最近は、がんの遺伝子を検査してこの傷を調べることで、特定のがんの診断や、追加治療の必要性の検討や、効果が高そうな薬物治療(抗がん剤)の選択の補助に用いることができるようになってきています。これを、がんのゲノム医療と呼び、以前から叫ばれている、個別化医療の一つで、このような個々の患者さんのがんの性質に合わせた治療が行えるようになってきています。
さらに詳しく知りたい方は、国立がん研究センターがん情報サービス「がんゲノム医療 もっと詳しく知りたい方へ」をご参考になさってください。
がんの薬物治療の選択に用いる遺伝子検査について
先に述べたがんの遺伝子の検査ですが、遺伝子の異常を検査して、特定の遺伝子異常を有しているがんに対して特に効果の高い薬物治療(抗がん剤)を選ぶことが出来るようになってきました。
すでに、日本の保険診療においても、10種類以上のがんに対して、がん組織や血液から抽出したがんの遺伝子を検査することで、患者さんにあった抗がん剤による薬物治療を選択することが出来るようになってきています。
治験などの臨床研究*の結果に基づいて安全性や有効性が確認された、現時点での薬物治療(標準治療)を選択するための検査のことを、コンパニオン検査と呼びます。
(*有効性や安全性に関する十分なデータがない薬の投与は、患者さんの病状などの条件をそろえて、有効性や安全性を評価する研究を行います。これを臨床研究といいます。その中で、薬事承認を目指したデータ収集を行うために製造販売を行う製薬企業が関与した臨床研究を、治験と呼びます。)
これまで、コンパニオン検査は1つの遺伝子のみ検査するものが中心でした。一部の肺がんでは、場合によっては4種類くらいのコンパニオン検査が必要となることがあります。
そこで、最近は一回の検査で、数十から数百の遺伝子が検査できる製品が登場しました。これを、がん遺伝子パネル検査と呼びます。
他にも、全エクソン検査や全ゲノム検査という、より広範なゲノムに関した検査も、研究されている状況です。(図1)
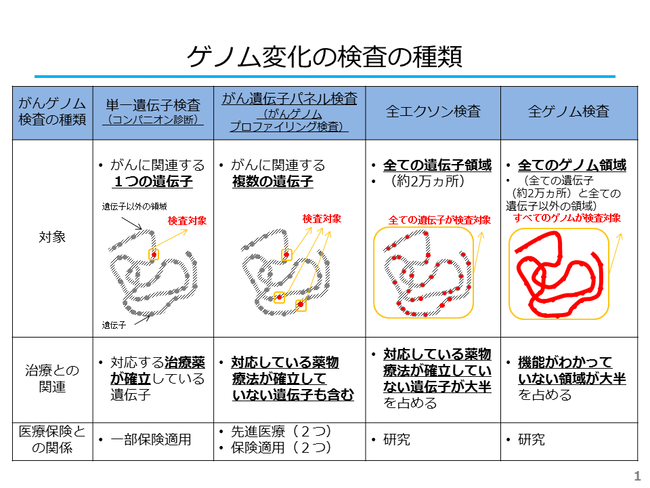
現時点では、保険診療で実施可能な検査はコンパニオン検査とがん遺伝子パネル検査であり、一般的には、がん遺伝子パネル検査とその結果に基づいた医療のことを指してがんゲノム医療といっています。
がん遺伝子パネル検査の医療現場での使い方とは
がん遺伝子パネル検査自体は、高い精度で数百に及ぶがんの遺伝子を一括で検査できるものですが、主な使い方は、コンパニオン検査を複数同時に行うことではありません。
現時点でのがん遺伝子パネル検査の主な使い方は、がんの遺伝子の特徴を調べること(がんゲノムプロファイリング検査)で、現在実施中の治験などの臨床研究を探すために用います。
がん遺伝子パネル検査の使い方として、がんの予後(どのくらいで調子が悪くなるか)を予測したり、難しい病気の診断にも用いることについても期待されていますが、現時点では、予後予測や診断のために用いる場合はほとんどありません。
あらかじめ、がんが有している遺伝子異常を調べることで、世の中に存在する治療薬の効きやすさを予想できるような遺伝子異常が見つかる場合があります。現在、がん遺伝子パネル検査を保険適用で行うことができるのは、標準治療が終了した、又は終了が見込まれる固形がん(白血病のような血液中を流れる血液のがんと異なり、塊をつくるがんの総称)の患者さんになります。標準治療は終了したけれど、何か治験など、少しでも有望な臨床研究があれば参加してみたいと考える患者さんが、その検査の対象となります。
現在、がん遺伝子パネル検査は、病院などで採取後に保存されているがん組織を検査会社に送付して、遺伝子異常を検査しています。遺伝子異常が見つかっても、がんの発育との関連があって治療薬が効きそうな見込みがある遺伝子異常(アクショナブルな遺伝子異常)でないと、治療対象という判断がなされません。
このように、がん遺伝子パネル検査の結果で見つかる遺伝子異常が、そのがんにとって病的意義があるのか、国内の治験などで対象となる薬はどこで投与可能か、さらにはその患者さんが生まれもった遺伝子の変化(がんの素因)ではないかなどといった点を検討することが必要です。検査会社から返ってきた検査結果をもとに、その遺伝子異常の意義については、専門家会議(エキスパートパネル)において検討されます。(図2)。
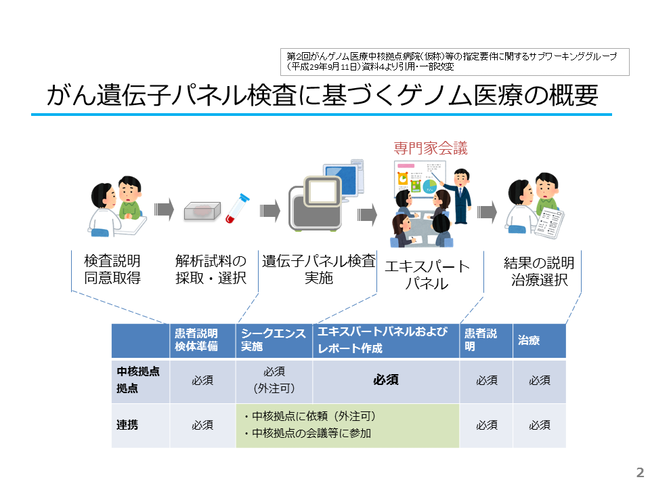
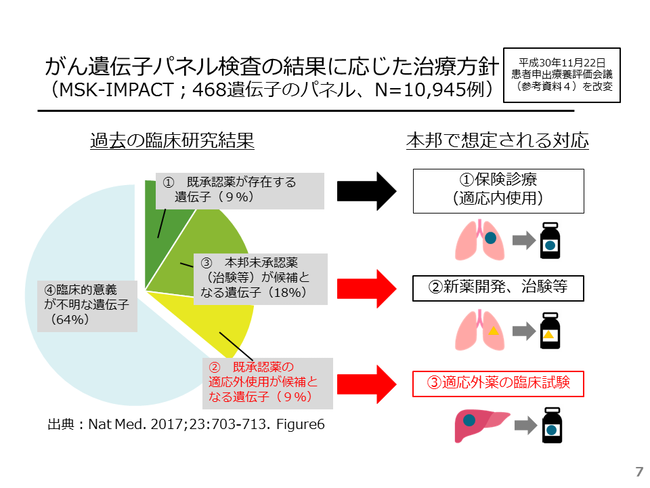
がん遺伝子パネル検査の結果、効果が期待できそうな医薬品が見つかる場合があり、国内の治験や臨床試験情報が付記されて、主治医のもとに検査結果が戻ってきます。例えば、NCCオンコパネルというがん遺伝子パネル検査の研究では、6割弱の方で効果が期待できそうな医薬品と関連した遺伝子の変化が見つかったとされます。(図3)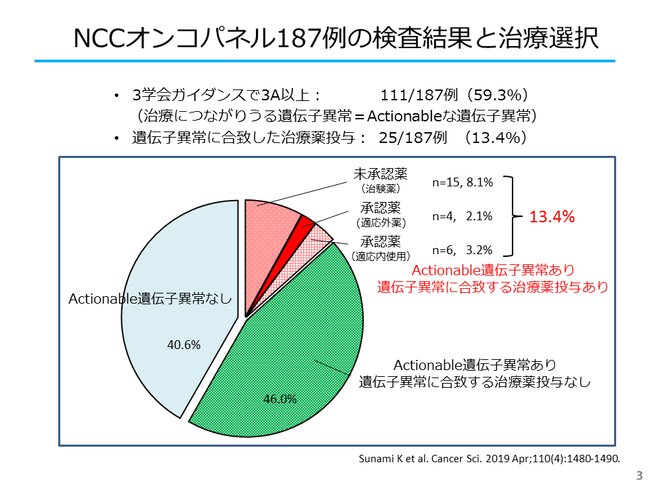
専門家会議の検討の結果、患者さんのがんに対して、保険診療で使用できる薬や、他のがんに保険診療で使用できる薬(適応外薬)や、まだ国内で流通していない薬(未承認薬)が治療候補として提案される可能性があります。国内で流通していない薬の場合は、治験があれば、それに参加することで、その薬を使用できる可能性があります。適応外薬を、患者さんのがんに対して使用することを適応外投与(適応外使用)といいますが、原則として保険診療で使用することは出来ません。そのため、もしそれを希望する場合には、治験や先進医療などの、適応外使用が許される、臨床試験に参加する必要があります。
がん遺伝子パネル検査が実施できる医療機関とは
がん遺伝子パネル検査は、全国全ての医療機関で実施できるわけではありません。がん遺伝子パネル検査のようなゲノム情報を扱う医療ができるのは、厚生労働省が指定した医療機関に限定されています。
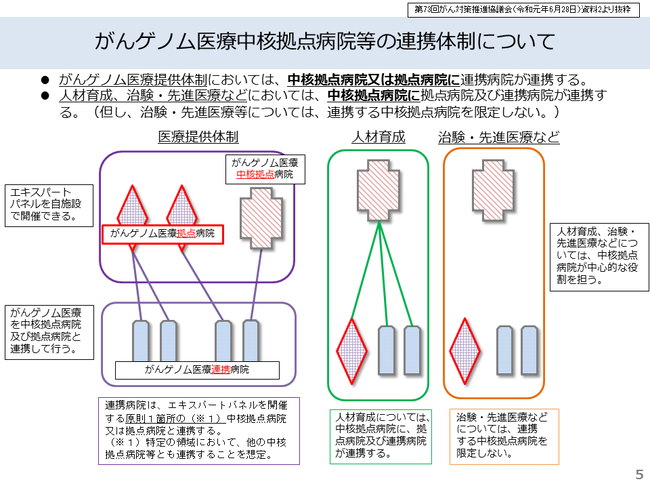
具体的には、がんゲノム医療中核拠点病院、がんゲノム医療拠点病院、がんゲノム医療連携病院の3種類の病院が全国に指定されており、これらの医療機関であれば、がん遺伝子パネル検査が実施可能です。(2019年10月時点では、上記3種類のいずれかに指定されている病院は、既に都道府県がん診療連携拠点病院、地域がん診療連携拠点病院のいずれかに指定されている病院になります。)
がんゲノム医療中核拠点病院、がんゲノム医療拠点病院、がんゲノム医療連携病院の3種類の病院の指定状況については、厚生労働省のホームページ「がん診療連携拠点病院等」がんゲノム医療中核拠点病院・がんゲノム医療連携病院の一覧表(外部サイトPDFにリンクします)や、第2回がんゲノム医療中核拠点病院等の指定に関する検討会(指定結果)(外部サイトにリンクします)にてご確認ください。
がんゲノム医療に関した政府の取り組みとがんゲノム情報管理センターとは
がんゲノム医療に関しては、政府も推進しています。特に、第3期がん対策推進基本計画(平成30年3月9日閣議決定)において、「がんゲノム医療」も取り組むべき重点項目の一つに位置づけられています。
具体的に、日本におけるがんゲノム医療のあるべき姿に向かって、どのような体制整備が必要であるかについて有識者によって検討されて、がんゲノム医療推進コンソーシアムという体制が必要だと提言されました。(図4)
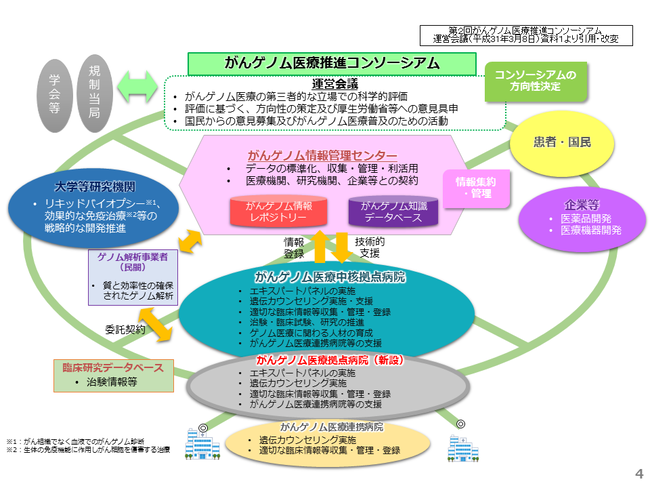
この中で、ゲノム医療を受ける患者さんに対して、がんゲノム医療を受けられる医療機関が必要とされています。また、その患者さんから判明した日本人のデータをがんゲノム情報管理センターに集約し、日本人におけるゲノム情報がどのように海外のヒトと異なるのかを研究したり、日本人独自の医薬品の開発などに向けて、大学等の研究機関や製薬企業等がその情報を元に研究を進めるという体制が必要とされています。
この考え方に沿って、前述したがんゲノム医療を受けられる病院の厚生労働省による指定(図5)や、がんゲノム医療情報管理センターの体制整備が進んでいます。
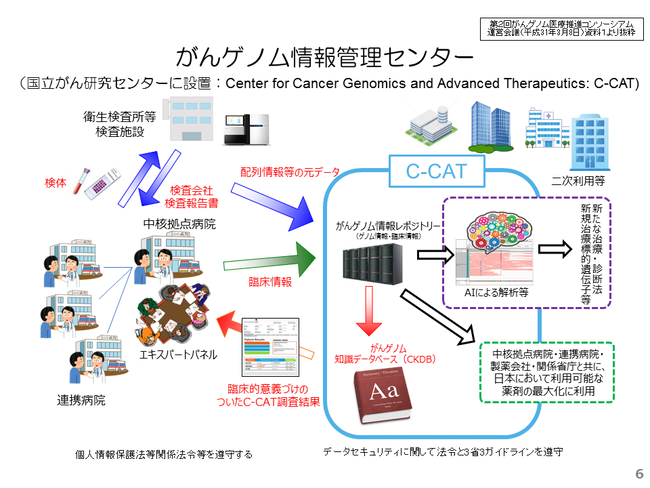
次に、がんゲノム医療情報管理センターの役割について説明します。
まず、これまで報告されている一つの遺伝子についても、全てががんに対する病的意義(がんの発生・成長や増殖等に関わるのかどうか)や、治療薬の効果が期待できるのかが十分分かっていない遺伝子の変化があります。もしかしたら、人種差によって日本人で特徴的な遺伝子の変化も存在するかもしれません。そのため、検査の結果判明した遺伝子変化について、その意味づけを海外の検査会社による検討や、海外のデータベースや報告だけに頼ると、日本人独自の情報が不足する可能性が心配されます。
このように、まだ多くのわかっていないことが存在するゲノム医療ですので、日本人のゲノム情報を集めて、海外からの報告との違いを検討したり、今後の医療の開発につなげる仕組みが必要であろうと考えられます。
がんゲノム情報管理センターには、日本人のゲノム情報の集約に加え、当該がん患者さんの臨床試験情報も集約することとなっています。一方で、C-CATにゲノム情報登録の同意を得た患者さんに対しては、検査結果をエキスパートパネルで検討する場合、C-CAT調査結果という報告書が送付されます。この調査結果には、その遺伝子異常に関連した、国内の臨床試験の実施状況の情報が記載されており、エキスパートパネルで検討する際に、患者さんの対象となる臨床試験情報が豊富になります。(図6)
ただし、こういったがんゲノム情報管理センターに対するゲノム情報の登録や、その利活用に関しては、患者さんの希望次第で拒否することも出来ます。その場合であっても、保険診療での検査実施は可能です。
がん遺伝子パネル検査の結果に基づく治療:治験
治験とは、その医薬品を日本国内の医療現場で使えるようにするために、日本政府から承認を得るためのデータを蓄積する臨床研究のことです。
治験の基礎知識や探し方については、新薬の治験と臨床試験のページをご確認ください。
がん遺伝子パネル検査の結果、治験として研究を行っている医薬品が候補であると判明することがあります。
治験などの臨床研究に参加することは、ご自身が、その医薬品の投与を受けられる可能性があることに加え、治験の医薬品が保険適用されれば、ご自身やご自身の大事な方を含む、将来の日本国民に対する利益につながる可能性があります。
当院で研究としてがん遺伝子パネル検査を行った成果としては、6割弱程度に臨床試験や治験の対象となる遺伝子異常が見つかりましたが、その結果に基づいた臨床試験・治験に入ることが出来た患者さんの割合は、8%程度でありました。これは、海外の類似した研究と同程度の割合でした。(図3)
保険外併用療養費制度、患者申出療養とは
わが国の公的医療保険のもとでは、原則として、保険適用の療養と、保険適用がされていない療養とを同時に併用することは許されていません。ただし、例外として、厚生労働大臣から、治験や先進医療といった評価療養、患者申出療養という制度の下で行うことが許された保険適用がなされていない療養については、例外的に保険診療と同時に併用することができます(保険外併用療養費制度といいます)。その、保険適用外の療養にかかる費用は、患者さんから徴収することが可能となっています。
詳しくは保険診療と保険外診療の併用について(厚生労働省)(外部サイトにリンクします)のホームページをご確認ください。
先に述べた患者申出療養とは、困難な病気と闘う患者の思いに応えるため、先進的な医療について、患者さんの申出を起点とし、安全性・有効性等を確認しつつ、身近な医療機関で迅速に受けられるようにするものです。患者さんの申出をもとに、臨床研究中核病院が臨床研究を立案し、患者さんの希望する療養を臨床研究として実施する制度です。
制度に関した詳細は、患者申出療養制度(厚生労働省)(外部サイトにリンクします)のページをご確認ください。
遺伝子パネル検査による遺伝子プロファイリングに基づく複数の分子標的治療に関する患者申出療養について
がん遺伝子パネル検査を行った場合、その結果に基づいて適応外薬が推奨される割合は、米国の研究データによると、8%程度とされています(図7)。先に説明したように、もし患者さんが適応外使用を希望する場合には、治験や先進医療などの、適応外使用が許される、臨床試験に参加する必要があります。
ただし、適応外薬が推奨されたものの、国内で実施可能な治験などの対象とならない方も一定の割合でいらっしゃいます。そのため、今回、国立がん研究センター中央病院が計画したのが、そのような治験などの対象とならない方へ治療機会を検討する臨床試験(研究)です。
対象となるがん遺伝子パネル検査は、保険診療又は先進医療で実施可能ながん遺伝子パネル検査で、検査結果に対する専門家会議によって、研究で使用可能な医薬品が推奨された場合に、その投与を検討できます。
この臨床試験(遺伝子パネル検査による遺伝子プロファイリングに基づく複数の分子標的治療に関する患者申出療養)は、2019年10月1日より開始となりました。開始時点では、8医薬品(セリチニブ、イマチニブメシル酸塩、エベロリムス、ダブラフェニブメシル酸塩、トラメチニブ ジメチルスルホキシド付加物、パゾパニブ塩酸塩、ニロチニブ塩酸塩水和物、ルキソリチニブリン酸塩)の医薬品が対象となっています。
現時点で、具体的に患者申出療養の対象となる医薬品の種類については臨床研究実施計画・研究概要公開システムをご確認ください。(図8)
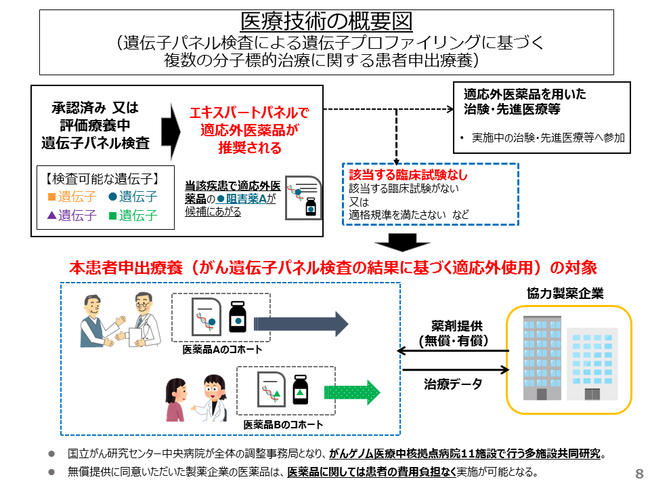
がん遺伝子パネル検査の結果により本研究の対象となっている医薬品が推奨された患者さんは、当院のような実施中の医療機関へ紹介をされることで、研究参加が検討されます。ただし、仮に、同じ医薬品や類似した医薬品が推奨されている場合であって、治験や先進医療が実施されている場合、一般的には治験等の方が、より薬事承認などにつながる研究になります。そのため、そういった治験を含めて総合的に検討の上、治療を検討します。
本試験を検討いただく際に、注意点がいくつかありますので、以下に列挙します。
- 本試験に参加するにあたっては、患者さんの病気に対して治療した成績が十分にはない適応外薬を投与することから、安全性が不明な部分も多くあります。未知の副作用が出現するかもしれません。そのため、患者さんにより安全に治療を受けていただくため、本研究に参加する患者さんの体調などの条件には、一定の制限を設けさせていただいています。
- 本試験に登録されても、すぐに医薬品が投与できるわけではありません。本試験に登録された後に、治療開始前に医薬品提供の製薬企業における再チェックが必要な場合があります。そのため、実際に投与が可能になるまで、1ヵ月半程度時間を要する可能性があります。原則として、その投与開始までの間、別の抗がん剤治療を受けていただくことはできません。
- 患者申出療養という国の制度の下で実施していただくため、がんゲノム情報センターに、既に実施されたがん遺伝子パネル検査のデータ提出、さらに過去から今後の治療データを登録することについて、同意していただくことが必要です。
- 本試験に参加することで、費用が必要になることがあります。本来は、今回対象となる医薬品と研究運用に関わる費用を、患者さんにご負担いただくことになります。複数の種類の医薬品があるとご説明いたしましたが、薬剤費にしたら4週間あたり約25万円から160万円強に相当する医薬品**までが対象になっています。しかし、本試験においては、2019年10月時点で対象となる医薬品は、全て製薬企業から無償提供されます。ただし、臨床試験実施に係る費用については、参加される患者さんお一人お一人から、別途いただくことになります。医療機関によって異なりますが、国立がん研究センター中央病院では、37万円程度、投与開始日に一括でご負担いただくことになります。
-
2023年4月時点では、全国のがんゲノム医療中核拠点病院12施設で実施しています。(今後、13施設に拡大予定)
-
定期診療・検査や入院などにかかる費用については、保険診療で行われます(ご自身の保険に応じた自費負担分は支払いが必要です)。
注2:2019年10月1日時点の薬価計算による試算
終わりに
がん遺伝子パネル検査が2019年6月より保険診療で実施可能となりました。しかし、実際にその結果として治療の選択肢に結びつく割合は1割弱の患者さんです。治験に参加できること、又は適応外薬の研究に参加できることで、少しでも多くの患者さんに治療の機会が提供できるよう、国立がん研究センター中央病院は、今後も研究センターとしての役割を担っていくつもりです。


